
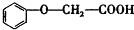 發生酯化反應的產物A是一種食用香料.甲分子為鏈狀結構且不含甲基.回答下列問題:
發生酯化反應的產物A是一種食用香料.甲分子為鏈狀結構且不含甲基.回答下列問題: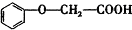 的分子式為C8H8O3.
的分子式為C8H8O3.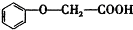 有多種同分異構體,其中屬于酯類,能使FeCl3溶液顯紫色,且苯環上的一氯代物有兩種的同分異構體的結構簡式為
有多種同分異構體,其中屬于酯類,能使FeCl3溶液顯紫色,且苯環上的一氯代物有兩種的同分異構體的結構簡式為 、
、 、
、 (其中一種)(任寫一種).
(其中一種)(任寫一種).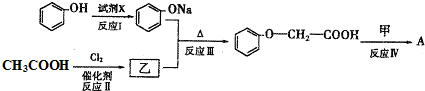
 .
. 分析 (1)根據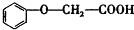 寫出其分子式;
寫出其分子式;
(2)由題意可知,甲與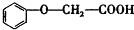 能發生酯化反應,所以甲中含有羥基,甲的分子式為C3H6O,則甲中有碳碳雙鍵;
能發生酯化反應,所以甲中含有羥基,甲的分子式為C3H6O,則甲中有碳碳雙鍵;
(3)屬于酯類,說明有酯基,能與FeCl3溶液發生顯色反應說明含有酚羥基,且有2種氯代物,苯環上有2個不同取代基且處于對位位置符合,結合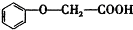 的結構可寫出其同分異構體的結構簡式;
的結構可寫出其同分異構體的結構簡式;
(4)苯酚和氫氧化鈉或鈉反應生成苯酚鈉,催化劑條件下,乙和氯氣反應生成丙,丙和苯酚鈉反應生成 ,結合反應信息可知,丙是ClCH2COOH,故乙為乙酸,CH2=CH-CH2-OH和
,結合反應信息可知,丙是ClCH2COOH,故乙為乙酸,CH2=CH-CH2-OH和 發生酯化反應生成A為
發生酯化反應生成A為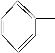 O-CH2COOCH2CH═CH2.
O-CH2COOCH2CH═CH2.
解答 解(1)根據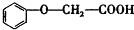 可知其分子式為C8H8O3,
可知其分子式為C8H8O3,
故答案為:C8H8O3;
(2)由題意可知,甲與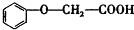 能發生酯化反應,所以甲中含有羥基,甲的分子式為C3H6O,則甲中有碳碳雙鍵;
能發生酯化反應,所以甲中含有羥基,甲的分子式為C3H6O,則甲中有碳碳雙鍵;
故答案為:羥基、碳碳雙鍵;
(3)屬于酯類,說明有酯基,能與FeCl3溶液發生顯色反應說明含有酚羥基,且有2種氯代物,苯環上有2個不同取代基且處于對位位置符合,結合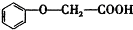 的結構可寫出其同分異構體為
的結構可寫出其同分異構體為 、
、 、
、 ,
,
故答案為: 、
、 、
、 (其中一種);
(其中一種);
(4)苯酚和氫氧化鈉或鈉反應生成苯酚鈉,催化劑條件下,乙和氯氣反應生成丙,丙和苯酚鈉反應生成 ,結合反應信息可知,丙是ClCH2COOH,故乙為乙酸,CH2=CH-CH2-OH和
,結合反應信息可知,丙是ClCH2COOH,故乙為乙酸,CH2=CH-CH2-OH和 發生酯化反應生成
發生酯化反應生成 O-CH2COOCH2CH═CH2和H2O,
O-CH2COOCH2CH═CH2和H2O,
①苯酚具有酸性但酸性弱于醋酸、碳酸,所以苯酚能和鈉、氫氧化鈉、碳酸鈉反應生成苯酚鈉,不能和碳酸氫鈉反應,
故答案為:B;
②由以上分析可知乙為CH3COOH,與氯氣發生取代反應生成ClCH2COOH,
故答案為:取代反應;CH3COOH;
③在催化劑、加熱條件下,CH2=CH-CH2-OH和 發生酯化反應生成A,反應方程式為:
發生酯化反應生成A,反應方程式為: ,
,
故答案為: .
.
點評 本題考查有機物的推斷,需要學生對給予的信息進行利用,較好的考查學生的閱讀能力、自學能力,題目難度中等,(4)注意根據有機物的結構與反應信息確定丙的結構突破口,答題時注意把握題給信息,注意養成仔細審題的良好習慣.


科目:高中化學 來源: 題型:選擇題
| A. | 只有① | B. | 只有①、③、④、⑤ | C. | 只有③、④、⑥ | D. | 只有①、③ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 向硝酸鈣溶液里滴加稀鹽酸得到pH=4的溶液中:2c(Ca2+)=c(NO3-) | |
| B. | 將0.2 mol•L-1NaA溶液和0.1 mol•L-1鹽酸等體積混合所得的堿性溶液中(A-為酸根離子): c(Na+)>c(A-)>c(C1-)>c(OH-) | |
| C. | 0.1 mol/LNaAlO2溶液中:c(Na+)>c(AlO2-)>c(OH-)>c(H+) | |
| D. | 濃度均為0.1 mol•L-1的CH3COOH、CH3COONa的混合溶液中:2c(OH-)=2c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3個 | B. | 4個 | C. | 5個 | D. | 6個 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
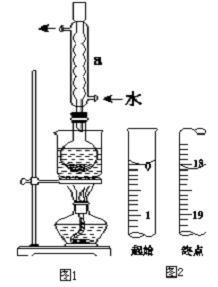 Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.
Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4種 | B. | 5種 | C. | 6種 | D. | 7種 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com