
工業上利用含有一定濃度的I2和CuSO4溶液的工業廢水制備飼料添加劑Ca(IO3)2,其生產流程如下:
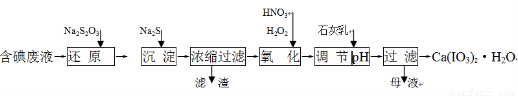
已知:Ca(IO3)2微溶于水,溶于硝酸;Ksp(CuI)=1.1×10-12, Ksp(Cu2S)=2.5×10-48;
氧化性: HNO3>IO3—>H2O2?
(1)“還原”過程中主要反應的化學方程式為:2Na2S2O3+I2 =??????? + 2NaI。?
(2)在還原過程還伴隨有CuI生成,寫出加入Na2S的離子反應方程式?????????????????????????? 。
(3)在氧化過程中先加入H2O2再加入濃硝酸,而不直接加入濃硝酸的目的是????????????????????? 。
(4)加入的石灰乳在溶液中反應而得到Ca(IO3)2,則要調節pH至????? (填“酸性” 或“中性”或“堿性”),原因是?????????????????????????????????????????????????????????????? 。
(5)Ca(IO3)2也可用電化學氧化法制取:先充分電解KI溶液,然后在電解后的溶液中加入CaCl2,最后過濾得到Ca(IO3)2。寫出電解時陽極發生的電極反應方程式 ????????????????????????? ,用該方法制取Ca(IO3)2,每1kg碘化鉀理論上可生產純度為97.8%Ca(IO3)2的質量為?????????????? ____kg(計算結果保留3位有效數字)。?
(1) Na2S4O6??? (2分)?
(2)2CuI(s)+S2—=Cu2S(s)+2I—?? (3分)?
(3)減少氧化過程中生成的氮的氧化物的污染? (2分)?
(4)中性? (2分)Ca(IO3)2在硝酸溶液中溶解,故要中和過量的酸;在堿性溶液中,會混有微溶的Ca(OH)2 造成產品不純。 (2分)?
(5)3H2O+I— -6e—=IO3—+6H+??? (3分) ;? 1.20(2分)
【解析】
試題分析: (1)該過程稱之為還原過程,可以肯定發生了氧化還原反應,所以根據方程式中的I的化合價降低可以知道,Na2S2O3 的中S的化合價升高,再根據Na、O原子守恒可以配平該方程式為2Na2S2O3+I2 = Na2S4O6+ 2NaI,還可以根據寫出的化學方程式用電子得失配平驗證。此處的難點關鍵在于缺項物質為中學階段沒接觸過的連四硫酸鈉,所以可能會出現想不到或是不敢寫的情況,只要大膽利用所學的原則配平就可以了。
(2)還原過程中已經說明有沉淀CuI生成了,所以加入Na2S還會發生反應,則應該是通過已知條件中的沉淀溶解平衡常數進行比較得出結論,比較之下Cu2S比 CuI更加難溶,所以此時會發生沉淀轉化,所以發生的反應方程式書寫要按照沉淀溶解平衡的格式書寫,方程式為2CuI(s)+S2—(aq)=Cu2S(s)+2I—(aq)。
(3)氧化步驟加入的H2O2 和濃硝酸起到氧化的目的,但是濃硝酸參與的反應容易產生氮氧化物污染環境,所以先加入過氧化氫。由于氧化性順序HNO3>IO3—>H2O2 ,所以加入的過氧化氫只能把I-氧化為IO3- ,要使I2繼續被氧化為IO3- ,還需要再加入濃硝酸,使濃硝酸反應更加完全,從而減少過程中氮氧化物的污染。
(4)加入石灰乳目的是反應得到Ca(IO3)2 ,且通過操作可以看出反應后要使Ca(IO3)2? 盡可能多得以晶體形式析出,而Ca(IO3)2溶于硝酸,所以必須調節pH值把過量的硝酸中和掉,且加入的石灰乳不能過量,過量則會混入石灰乳沉淀雜質,所以應該調節pH至中性。
(5)用KI溶液電解制備Ca(IO3)2 溶液,則I-需要發生氧化反應在陽極放電生成IO3-,電解液是非堿性的,所以根據O原子守恒,IO3—中的O一定來源于H2O中,從而生成了H+,所以電極反應式為:3H2O+I— -6e—=IO3—+6H+ ;計算碘化鉀的質量可以采用I原子守恒計算,所以有1/2n(KI)= n(Ca(IO3)2)=1000/166mol,m產品=M(Ca(IO3)2)×n(Ca(IO3)2)÷97.8%=390g/mol×1000/166mol÷97.8%≈1200g=1.20kg。
考點:本題考查的是化學工藝流程,涉及到了陌生的氧化還原反應缺項配平、沉淀轉化、環境問題、PH調節、電化學基礎、轉化計算等內容。


科目:高中化學 來源: 題型:閱讀理解
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
查看答案和解析>>
科目:高中化學 來源:物理教研室 題型:022
(1)海水中含有大量的氯化鈉。氯化鈉中的金屬元素位于元素周期表第 族。
(2)目前國際上實用的“海水淡化”主要技術之一是蒸餾法。蒸餾法是將海水變成蒸汽,蒸汽經過冷卻而得高純度淡水,由此可判斷蒸餾法是 (填物理變化、化學變化)
(3)工業上利用電解飽和食鹽水可制得重要化工產品,反應式為:
![]() 食鹽+H2O NaOH+H2+Cl2(未配平)。利用電解所得氣體制36.5%的濃鹽酸1000t,最少需要消耗食鹽
t。
食鹽+H2O NaOH+H2+Cl2(未配平)。利用電解所得氣體制36.5%的濃鹽酸1000t,最少需要消耗食鹽
t。
吸收
(4)近年來有人提出了一種利用氯堿工業產品及氯化鈉循環治理含二氧化硫廢氣并回收二氧化硫的方法,該方法的流程如下:

寫出②④的化學反應方程式:
、_____________________________________
上述亞硫酸氫鈉與甲醛經過一定反應,可以合成俗稱“吊白塊”(雕白粉)的物質。因吊白塊對人體有害,不能用于食品漂白。其結構簡式為:HOCH2SO3Na,根據其結構特點,吊白塊能發生的反應有:
A.皂化反應 B.聚合反應 C.與金屬鈉反應 D.氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
海水占地球總儲水量的97.2%。若把海水淡化和化工生產結合起來,既可以解決淡水資源缺乏的問題,又可以充分利用海洋資源。
(1)海水中含有大量的氯化鈉,氯化鈉中的金屬元素位于元素周期表第__________族。
(2)目前國際上使用的“海水淡化”主要技術之一是蒸餾法。蒸餾法是將海水變成蒸汽,蒸汽經過冷卻而得高純度淡水,由此可判斷蒸餾法是____________(填物理變化或化學變化)。
(3)工業上利用電解飽和食鹽水可制得重要化工產品,反應式為食鹽+H2O![]() NaOH+H2+Cl2(未配平)。該反應中食鹽的化學式是____________。利用電解所得氣體制36.5%的濃鹽酸1 000 t,最少需要消耗食鹽____________t。
NaOH+H2+Cl2(未配平)。該反應中食鹽的化學式是____________。利用電解所得氣體制36.5%的濃鹽酸1 000 t,最少需要消耗食鹽____________t。
(4)近年來有人提出了一種利用氯堿工業產品及氯化鈉循環治理含二氧化硫廢氣并回收二氧化硫的方法,該方法的流程如下:

寫出②④的化學反應方程式:____________________________________________。
上述亞硫酸氫鈉與甲醛經過一定反應可以合成俗稱“吊白塊(雕白粉)”的物質。因吊白塊對人體有害,不能用于食品漂白。其結構簡式為HOCH2SO3Na,根據其結構特點,吊白塊能發生的反應有____________。
A.皂化反應
B.聚合反應
C.與金屬鈉反應
D.氧化反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com