
【題目】如圖為碳元素的價類二維圖,結合圖中的物質部分轉化關系,完成下列問題:
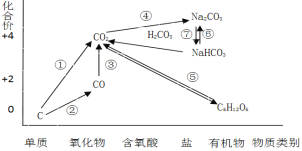
(1)下列說法正確的是 __________
a.要實現反應①一定要與氧化劑作用
b.要實現反應②一定要與還原劑作用
c.在一定條件下木炭與濃硝酸能實現 反應①轉化
d.反應⑤屬于非氧化還原反應
(2)下列有關碳及其化合物類別及性質說法不正確的是__________
a.CO不屬于酸性氧化物,具有還原性
b.CO2屬于酸性氧化物,可以與堿反應生成碳酸鹽
c.NaHCO3屬于弱酸的酸式鹽,既能與硫酸反應又能與NaOH反應
d.金剛石和石墨互為同素異形體,其物理性質和化學性質均相同
(3)高爐煉鐵的過程是將鐵礦石(Fe2O3)還原成金屬鐵的過程,實現了反應③的轉化,請寫出其反應的化學方程式,并用“雙線橋”表示電子的得失情況______________________________ 。
(4)化學活動課上,兩組同學分別用如圖所示甲、乙兩裝置探究“Na2CO3、NaHCO3與稀鹽酸的反應”。按下表中的試劑用量,在相同條件下,將兩個氣球中的固體粉末同時倒入試管中(裝置的氣密性已檢查)。請回答:
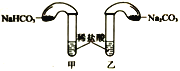
①兩組反應開始時,裝置___________(填“甲”或“乙”)中的氣球體積先變大,該裝置中反應的離子方程式是______________________。
②當試管中不再有氣體生成時,兩組實驗出現不同現象。
試劑用量 | 實驗現象 | 分析原因 | |
第A組 | 0.84gNaHCO3 1.06gNa2CO3 6ml 4mol·L-1鹽酸 | 甲中氣球與乙中氣球的 體積相等 | 甲、乙鹽酸均過量 n(NaHCO3)= n(Na2CO3) V(CO2)甲=V(CO2)乙 |
第B組 | 1.2gNaHCO3 1.2gNa2CO3 6ml 2mol·L-1鹽酸 | 甲中氣球比乙中氣球的體積大 片刻后,乙中氣球又縮小,甲中氣球的體積基本不變 |
|
按上表第A組原因分析方法,分析第B組實驗甲中氣球為比乙中氣球體積大的原因__________。用離子方程式表示第B組乙中氣球又縮小的原因:______________。
【答案】A C D  甲 H++HCO3-=CO2↑+H2O 甲、乙鹽酸均不足,消耗的n(NaHCO3)﹥n(Na2CO3) ,V(CO2)甲﹥V(CO2)乙 CO32-+CO2+H2O=2HCO3-
甲 H++HCO3-=CO2↑+H2O 甲、乙鹽酸均不足,消耗的n(NaHCO3)﹥n(Na2CO3) ,V(CO2)甲﹥V(CO2)乙 CO32-+CO2+H2O=2HCO3-
【解析】
(1)根據氧化還原反應的有關規律判斷;
(2)a. CO不屬于酸性氧化物,C元素化合價為+2價,具有還原性,故a正確;
b. CO2屬于酸性氧化物,可以與堿反應生成碳酸鹽,故b正確;
c. NaHCO3屬于弱酸的酸式鹽,既能與硫酸反應生成二氧化碳和水,又能與NaOH反應生成碳酸鈉,故c正確;
d. 金剛石和石墨互為同素異形體,其化學性質相似,物理性質有很大差異,故d錯誤;
(3)Fe2O3在高溫下可以被CO還原成Fe單質,Fe元素由+3價下降到0價,得到3個電子;
(4)①碳酸氫鈉和鹽酸反應的速率更快;
②按上表第A組原因分析方法,分析第B組實驗中反應物之間的數量關系,二氧化碳可以溶于碳酸鈉溶液中。
(1)a.①C ![]() CO2,C化合價升高作為還原劑,需要加入氧化劑才能實現,故a正確;
CO2,C化合價升高作為還原劑,需要加入氧化劑才能實現,故a正確;
b.①C ![]() CO,C化合價升高作為還原劑,需要加入氧化劑才能實現,故b錯誤;
CO,C化合價升高作為還原劑,需要加入氧化劑才能實現,故b錯誤;
c.木炭與濃硝酸在加熱的條件下可以生成二氧化碳,可以實現反應①轉化,故c正確;
d. 反應⑤中C化合價變化,屬于氧化還原反應,故d錯誤;
正確答案是ac;
(2)a. CO不屬于酸性氧化物,C元素化合價為+2價,具有還原性,故a正確;
b. CO2屬于酸性氧化物,可以與堿反應生成碳酸鹽,故b正確;
c. NaHCO3屬于弱酸的酸式鹽,既能與硫酸反應生成二氧化碳和水,又能與NaOH反應生成碳酸鈉,故c正確;
d. 金剛石和石墨互為同素異形體,其化學性質相似,物理性質有很大差異,故d錯誤;
題目要求選錯的,故選d;
(3)Fe2O3在高溫下可以被CO還原成Fe單質,Fe元素由+3價下降到0價,得到3個電子,用“雙線橋”表示電子的得失情況為:
(4)①碳酸鈉和鹽酸的反應可以分成兩步:第一步Na2CO3+HCl=NaHCO3+NaCl,第二步 NaHCO3+HCl=NaCl+H2O+CO2![]() ,而碳酸氫鈉只進行第二步反應,所以更快一些,故裝置甲中的氣球體積先變大,甲中發生的離子方程式是:H++HCO3-=CO2↑+H2O;
,而碳酸氫鈉只進行第二步反應,所以更快一些,故裝置甲中的氣球體積先變大,甲中發生的離子方程式是:H++HCO3-=CO2↑+H2O;
②根據化學方程式計算可知A組中NaHCO3和Na2CO3都已完全反應。B組中,n(Na2CO3)= ![]() =0.011mol,n(NaHCO3)=
=0.011mol,n(NaHCO3)= ![]() =0.014mol,n(HCl)=0.012mol,根據反應NaHCO3+HCl =NaCl + CO2↑+H2O和Na2CO3+2HCl=2NaCl+CO2↑+H2O可知,Na2CO3、NaHCO3都過量,NaHCO3產生的CO2較Na2CO3的多。因為氣體收集于氣球中,乙中CO2又與過量的Na2CO3溶液反應,故甲中氣球比乙中氣球的體積大片刻后,乙中氣球又縮小,甲中氣球的體積基本不變,分析原因為:甲、乙鹽酸均不足,消耗的n(NaHCO3)﹥n(Na2CO3) ,V(CO2)甲﹥V(CO2)乙;CO2與過量的Na2CO3溶液反應為:CO32-+CO2+H2O=2HCO3-。
=0.014mol,n(HCl)=0.012mol,根據反應NaHCO3+HCl =NaCl + CO2↑+H2O和Na2CO3+2HCl=2NaCl+CO2↑+H2O可知,Na2CO3、NaHCO3都過量,NaHCO3產生的CO2較Na2CO3的多。因為氣體收集于氣球中,乙中CO2又與過量的Na2CO3溶液反應,故甲中氣球比乙中氣球的體積大片刻后,乙中氣球又縮小,甲中氣球的體積基本不變,分析原因為:甲、乙鹽酸均不足,消耗的n(NaHCO3)﹥n(Na2CO3) ,V(CO2)甲﹥V(CO2)乙;CO2與過量的Na2CO3溶液反應為:CO32-+CO2+H2O=2HCO3-。


 陽光課堂課時作業系列答案
陽光課堂課時作業系列答案科目:高中化學 來源: 題型:
【題目】已知常溫下濃度為0.1mol·L-1的下列溶液的pH如下表:
溶質 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
下列有關說法正確的是
A. 在相同溫度下,同濃度的三種酸溶液的導電能力順序:H2CO3<HClO<HF
B. 若將CO2通入0.1 mol·L-1Na2CO3溶液中至溶液中性,則溶液中2c(CO32-)+c(HCO3-)=0.1 mol·L-1
C. 根據上表,水解方程式ClO-+H2O![]() HClO+OH-的水解常數K=10-7.6
HClO+OH-的水解常數K=10-7.6
D. 向上述NaClO溶液中通HF氣體至恰好完全反應時:c(Na+)>c(F-)>c(H+)>c(HClO)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容器中,反應3A(g)+B(s)![]() 2C(g)+2D(g) ΔH >0達到平衡后,改變以下條件,下列說法正確的是( )
2C(g)+2D(g) ΔH >0達到平衡后,改變以下條件,下列說法正確的是( )
A. 增大壓強,正、逆反應速率同等程度增大,平衡不移動
B. 升高溫度,正反應速率增大,逆反應速率減小,平衡向正方向移動
C. 增加A的濃度,平衡向正方向移動,平衡常數增大
D. 增加B的用量,正、逆反應速率不變,平衡不移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】自然界的氮循環如下圖所示,下列說法不正確的是( )

A.①中N2與O2反應生成NO
B.②中合成氨屬于人工固氮
C.③中氮元素只被氧化
D.氧元素參與了氮循環
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】維生素C是一種水溶性維生素(其水溶液呈酸性),它的化學式是C6H8O6,人體缺乏這樣的維生素能得壞血癥,所以維生素C又稱抗壞血酸。在新鮮的水果、蔬菜、乳制品中都富含維生素C,例如新鮮橙汁中維生素C的含量在500mg/L左右。某校課外活動小組測定了某牌子的軟包裝橙汁中維生素C的含量,下面是測定實驗分析報告。(請填寫有關空白)
(一)測定目的:測定××牌軟包裝橙汁中維生素C的含量。
(二)測定原理:C6H8O6+I2 →C6H6O6+2H++2I―
(三)實驗用品及試劑
(1)儀器和用品(自選,略)
(2)試劑:指示劑___(填名稱),濃度為7.50×10-3mol·L-1的I2標準溶液、蒸餾水等。
(四)實驗過程
(1)洗滌儀器,檢查滴定管是否漏液,潤洗后裝好標準碘溶液待用。
(2)用___(填儀器名稱)向錐形瓶中移入20.00mL待測橙汁,滴入2滴指示劑。
(3)用左手控制滴定管的___(填部位),右手搖動錐形瓶,眼睛注視___,直到滴定終點。滴定至終點時的現象是___。
(五)數據記錄與處理(請在下面設計并畫出數據記錄和數據處理的表格,不必填數據)。__

若經數據處理,滴定中消耗標準碘溶液的體積是15.00mL,則此橙汁中維生素C的含量是___mg/L。
(六)問題討論:
(1)滴定時能否劇烈搖動錐形瓶?為什么?_____
(2)從分析數據看,此軟包裝橙汁是否是純天然橙汁?___(填“是”或“不是”或“可能是”)。制造商最可能采取的做法是____(填編號):
A.加水稀釋天然橙汁 B.橙汁已被濃縮 C.將維生素C作為添加劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校學生化學實驗小組,為驗證非金屬元素氟的氧化性強于硫和氮,設計了一套實驗裝置:(部分加持裝置已略去)
(1)寫出A中反應的離子方程式 。
(2)B中出現黃色渾濁現象,產生此現象的離子方程式 。
(3)試從原子結構角度解釋氯的氧化性大于硫的原因 。
(4)D中干燥管中出現的現象及化學方程式 。
(5)有同學認為D中的現象并不能說明氯的氧化性大于氮,需要在C之前加裝洗氣裝置,請畫出其裝置圖 (并注明盛裝試劑)。
(6)還有什么方法能證明氧化性Cl2>S,用一種相關事實說明 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化亞銅(CuCl)是一種難溶于水的白色粉末,不溶于乙醇,可溶于濃鹽酸和氨水,在潮濕空氣中被氧化成綠色的堿式氯化銅[Cu2(OH)3Cl]。工業上常以海綿銅(主要成分是Cu,含有少量CuO)為原料生產CuCl,其工藝流程如下
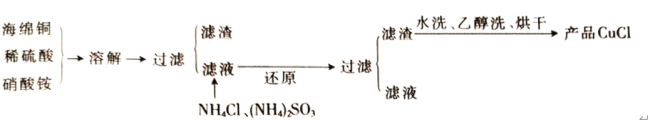
(1)配平“溶解”過程中發生的氧化還原反應的離子方程式:_________
Cu+ NO3-+ = Cu2++ NO↑+ H2O
(2)“還原”過程中,作還原劑的是__________(填化學式);寫出“還原”過程中發生反應的離子方程式:__________________________________。
(3)寫出CuCl在潮濕的空氣中被氧化的化學方程式:__________________________。
(4)析出的CuCl晶體水洗后要立即用無水酒精洗滌,并在真空干燥機內于70℃下干燥2h,冷卻密封包裝。密封包裝的原因是_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】右圖是一種試驗某氣體化學性質的實驗裝置,圖中B為開關。 如先打開B,在A處通入干燥氯氣,C中紅色布條顏色無變化;當關閉B時,C處紅色布條顏色褪去。則D瓶中盛有的溶液是( )
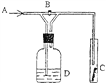
A. 濃H2SO4 B. 濃NaOH溶液
C. 飽和Na2SO4溶液 D. 石灰乳
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸銅是一種應用極其廣泛的化工原料;以下是某工廠用含鐵廢銅為原料生產膽礬(CuSO45H2O)和副產物石膏(CaSO42H2O)的生產流程示意圖:
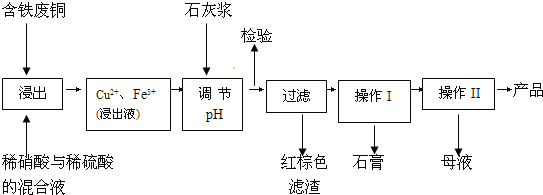
膽礬和石膏在不同溫度下的溶解度(g/100g水)見表。
溫度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
膽礬 | 32 | 44.6 | 61.8 | 83.8 | 114 |
請回答下列問題:
(1)紅棕色濾渣的主要成分是___;
(2)寫出浸出過程中生成硫酸銅的離子方程式___;
(3)操作I包括蒸發濃縮、__等操作,溫度應該控制在__℃左右;
(4)從溶液中分離出硫酸銅晶體的操作Ⅱ應為__、___、洗滌、干燥;晶體用無水乙醇作洗滌液而不用蒸餾水的原因是__;干燥時采用晾干,不用加熱烘干的原因是___。
(5)取樣檢驗是為了確認Fe3+是否除凈。有同學設計了以下兩種方案,在實驗室分別對所取樣品按下列方案進行操作:
方案一:取樣于試管→滴加KSCN溶液; 方案二:紙層析→噴KSCN溶液;
①你認為上述兩種方案設計更合理的是__;
②指出你認為不合理方案存在的問題是__。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com