
【題目】石油裂解氣主要含有丙烯、1,3-丁二烯等不飽和烴,以它們為原料可合成CR橡膠和醫藥中間體G,,合成路線如下:

已知:①B、C、D 均能發生銀鏡反應;
②
(1)A的順式異構體的結構簡式為___________________。
(2)C中含氧官能團的名稱是____________,反應①的反應類型為____________________。
(3)寫出E→ 反應的化學方程式:_________________________________。
(4)寫出同時滿足下列條件的醫藥中間體G的同分異構體的結構簡式: __________________。
①與D 互為同系物; ②核磁共振氫譜有三組峰。
(5)用簡要語言表述檢驗B中所含官能團的實驗方法:_______________________。
(6)以A為起始原料合成CR橡膠的線路為______________________(其它試劑任選)。
【答案】 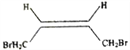 羥基、醛基 取代反應 HOOCCH2COOH+2C2H5OH
羥基、醛基 取代反應 HOOCCH2COOH+2C2H5OH![]() C2H5OOCCH2COOC2H5+2H2O OHC(CH2)4CHO、OHCCH(CH3)CH(CH3)CHO 取少量B于潔凈試管中,加入足量銀氨溶液,水浴加熱有銀鏡生成,證明B中有醛基;再加酸酸化,滴入少量溴的四氯化碳溶液,溶液褪色,證明含有碳碳雙鍵
C2H5OOCCH2COOC2H5+2H2O OHC(CH2)4CHO、OHCCH(CH3)CH(CH3)CHO 取少量B于潔凈試管中,加入足量銀氨溶液,水浴加熱有銀鏡生成,證明B中有醛基;再加酸酸化,滴入少量溴的四氯化碳溶液,溶液褪色,證明含有碳碳雙鍵 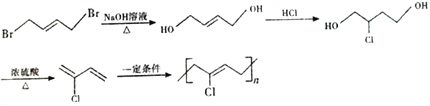
【解析】根據流程圖,1,3-丁二烯與溴發生1,4加成,生成A,A為1,4-二溴-2-丁烯(![]() );與氫氣加成后生成1,4-二溴丁烷(
);與氫氣加成后生成1,4-二溴丁烷(![]() );丙烯催化氧化生成B,B為CH2=CHCHO,C的相對分子質量比B大18,說明B與水加成生成C,C為
);丙烯催化氧化生成B,B為CH2=CHCHO,C的相對分子質量比B大18,說明B與水加成生成C,C為![]() ,催化氧化生成D(丙二醛),與銀氨溶液反應生成E(丙二酸),與乙醇酯化反應生成F(
,催化氧化生成D(丙二醛),與銀氨溶液反應生成E(丙二酸),與乙醇酯化反應生成F(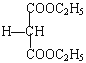 );根據信息,F(
);根據信息,F( )與
)與![]() 反應生成
反應生成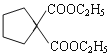 ,進一步反應生成G(
,進一步反應生成G(![]() )。
)。
(1)A為1,4-二溴-2-丁烯(![]() ),其順式異構體的結構簡式為
),其順式異構體的結構簡式為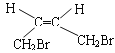 ,正確答案:
,正確答案: 。
。
(2) C為![]() ,含有的官能團有碳碳羥基、醛基;通過題給信息②可知,該過程發生了取代反應;正確答案:碳碳雙鍵、醛基; 取代反應。
,含有的官能團有碳碳羥基、醛基;通過題給信息②可知,該過程發生了取代反應;正確答案:碳碳雙鍵、醛基; 取代反應。
(3)有機物E為HOOCCH2COOH,與C2H5OH在濃硫酸加熱的條件下發生酯化反應,化學方程式:HOOCCH2COOH+2C2H5OH![]() C2H5OOCCH2COOC2H5+2H2O ;正確答案:HOOCCH2COOH+2C2H5OH
C2H5OOCCH2COOC2H5+2H2O ;正確答案:HOOCCH2COOH+2C2H5OH![]() C2H5OOCCH2COOC2H5+2H2O。
C2H5OOCCH2COOC2H5+2H2O。
(4)有機物G的分子式為C6H10O2, ①與D 互為同系物;有機物D為二元醛類;②核磁共振氫譜有三組峰,具有一定的對稱性;滿足條件的有機物可能的結構有2種:OHC(CH2)4CHO和OHCCH(CH3)CH(CH3)CHO;正確答案: OHC(CH2)4CHO和OHCCH(CH3)CH(CH3)CHO。
(5)有機物B CH2=CHCHO,含有醛基和碳碳雙鍵,由于醛基的還原性較強,先檢驗醛基,然后在檢驗碳碳雙鍵;具體操作如下:取少量B于潔凈試管中,加入足量銀氨溶液,水浴加熱有銀鏡生成,證明B中有醛基;再加酸酸化,滴入少量溴的四氯化碳溶液,溶液褪色,證明含有碳碳雙鍵 ;正確答案:取少量B于潔凈試管中,加入足量銀氨溶液,水浴加熱有銀鏡生成,證明B中有醛基;再加酸酸化,滴入少量溴的四氯化碳溶液,溶液褪色,證明含有碳碳雙鍵 。
(6)A為![]() ,在堿性環境下發生取代反應生成二元烯醇
,在堿性環境下發生取代反應生成二元烯醇![]() ,然后再與氯化氫發生加成生成
,然后再與氯化氫發生加成生成![]() ,該有機物在濃硫酸作用下發生消去反應生成
,該有機物在濃硫酸作用下發生消去反應生成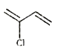 ;該有機物發生加聚反應生成高分子;具體流程如下:
;該有機物發生加聚反應生成高分子;具體流程如下: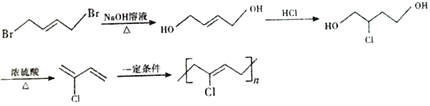 ;正確答案:
;正確答案: 。
。


科目:高中化學 來源: 題型:
【題目】A、B、C、D都是中學化學常見的物質,其中A、B、C均含同一種元素。在一定條件下相互轉化關系如下圖所示(部分產物已略去)。請按要求回答下列問題:
![]()
(1)若B、C為氧化物,B轉化為C時,質量增加25%,C能夠與水反應生成一種強酸,則B
轉化為C的化學方程式是_______________________;
(2)若D為某金屬單質,向C的溶液中滴加硝酸銀溶液,產生不溶于稀硝酸的白色沉淀,則B 的化學式是_____________;
(3)若D為強電解質溶液,A和C在溶液中反應生成白色沉淀B,則A和C反應的離子方程式是___________________符合條件的D物質可能是___________(填序號)。
①硫酸 ②醋酸 ③氫氧化鈉 ④一水合氨 ⑤氯化鋇
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某無色溶液里只含有下列7種離子中的某幾種:Mg2+ 、H+ 、Ag+ 、Na+ 、Cl- 、HCO3- 、OH- 。已知:該溶液能跟金屬鋁反應,且放出氫氣。試回答:
(1)若鋁跟溶液反應后只有AlO2-生成,則原溶液一定含有的大量離子是_______ ,發生該反應的離子方程式是__________;還可能含有離子是__________。
(2)若鋁跟溶液反應后只有Al3+生成,則原溶液中一定不能大量含有的離子是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關電解質溶液的說法正確的是
A. 向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中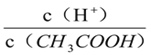 減小
減小
B. 將CH3COONa溶液從20℃升溫至30℃,溶液中![]() 增大
增大
C. 向鹽酸中加入氨水至中性,溶液中![]() >1
>1
D. 向AgCl、AgBr的飽和溶液中加入少量AgNO3,溶液中不![]() 變
變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用含三價釩(V2O3)為主的某石煤為原料(含有Al2O3、CaO等雜質),鈣化法焙燒制備V2O5,其流程如下:
![]()
【資料】:+5價釩在溶液中的主要存在形式與溶液pH的關系:
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要離子 | VO2+ | VO3 | V2O74 | VO43 |
(1)焙燒:向石煤中加生石灰焙燒,將V2O3轉化為Ca(VO3)2的化學方程式是______。
(2)酸浸: ① Ca(VO3)2難溶于水,可溶于鹽酸。若焙砂酸浸時溶液的pH=4,Ca(VO3)2溶于鹽酸的離子方程式是______。
② 酸度對釩和鋁的溶解量的影響如圖所示:酸浸時溶液的酸度控制在大約3.2%,根據如圖推測,酸浸時不選擇更高酸度的原因是______。

(3)轉沉:將浸出液中的釩轉化為NH4VO3固體,其流程如下:
![]()
① 浸出液中加入石灰乳的作用是______。
② 已知CaCO3的溶解度小于Ca3(VO4)2。向Ca3(VO4)2沉淀中加入(NH4)2CO3溶液,可使釩從沉淀中溶出。結合化學用語,用平衡移動原理解釋其原因:______。
③ 向(NH4)3VO4溶液中加入NH4Cl溶液,控制溶液的pH=7.5。當pH>8時,NH4VO3的產量明顯降低,原因是______。
(4)測定產品中V2O5的純度:
稱取a g產品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1 mL c1 mol·L1 (NH4)2Fe(SO4)2溶液(VO2+ + 2H+ + Fe2+ == VO2+ + Fe3+ + H2O)。最后用c2 mol·L1 KMnO4溶液滴定過量的(NH4)2Fe(SO4)2至終點,消耗KMnO4溶液的體積為b2 mL。已知 MnO4被還原為Mn2+,假設雜質不參與反應。則產品中V2O5的質量分數是______。(V2O5的摩爾質量:182 g·mol1)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組探究SO2氣體還原Fe3+,他們使用的藥品和裝置如下圖所示,下列說法不合理的是

A. 能表明I-的還原性弱于SO2的現象是B中藍色溶液褪色
B. 裝置C的作用是吸收SO2尾氣,防止污染空氣
C. 為了驗證A中發生了氧化還原反應,加入KMnO4溶液,紫紅色褪去
D. 為了驗證A中發生了氧化還原反應,加入用稀鹽酸酸化的BaCl2溶液,產生白色沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列三個化學反應均能發生:
X2+2W2+![]() 2X-+2W3+
2X-+2W3+
Z2+2X-![]() 2Z-+X2
2Z-+X2
2W3++2Y-![]() 2W2++Y2
2W2++Y2
則在相同條件下,下列三個反應也能發生的是( )
①Y2+2X-![]() 2Y-+X2 ②Z2+2Y-
2Y-+X2 ②Z2+2Y-![]() 2Z-+Y2 ③2W3++2Z-
2Z-+Y2 ③2W3++2Z-![]() 2W2++Z2
2W2++Z2
A. 只有① B. 只有② C. ①和② D. ②和③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是中學化學常用于混合物分離和提純的裝置,請根據裝置回答問題:
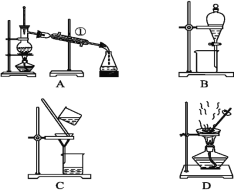
(1)從氯化鉀溶液中得到氯化鉀固體,選擇裝置____(填代表裝置圖的字母,下同);除去自來水中的Cl-等雜質,選擇裝置_________。
(2)從碘水中分離出I2,選擇裝置____,該分離方法的名稱為__________。
(3)裝置B在分液時為使液體順利下滴,應進行的具體操作是__________________________
(4)海水中蘊藏著豐富的資源,取少量海水按如下流程進行實驗:
海水![]() 粗鹽
粗鹽![]() 食鹽水
食鹽水![]() 氯化鈉晶體
氯化鈉晶體
粗鹽中含Ca2+、Mg2+、Fe3+、SO42-等雜質,需要提純后才能綜合利用。粗鹽提純的步驟有:①加入過量的Na2CO3溶液;②加入過量的BaCl2溶液;③加入過量的NaOH溶液;④調節溶液的pH等于7;⑤溶解;⑥過濾;⑦蒸發。正確的操作順序是____(填寫字母序號)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com