
分析 (1)在水溶液中和熔融狀態下均不能導電的化合物為非電解質,據此分析;
(2)在水溶液中或熔融狀態下能導電的化合物為電解質,據此分析;
(3)根據電解質的結構來分析.
解答 解:①NaHCO3晶體溶于水后能導電,故為電解質;②液態SO3在水溶液中能導電和其本身無關,在熔融狀態下又不導電,故為非電解質;③HF溶于水后能導電,故為電解質;④鹽酸是混合物,既不是電解質也不是非電解質;⑤蔗糖在水溶液中和熔融狀態下均不導電,故為非電解質;⑥銅是單質,既不是電解質也不是非電解質;⑦KOH固體在水溶液中和熔融狀態下均能導電,故為電解質;⑧氨水是混合物,既不是電解質也不是非電解質.
(1)在水溶液中和熔融狀態下均不能導電的化合物為非電解質,故為非電解質的為②⑤,故答案為:②⑤;
(2)在水溶液中或熔融狀態下能導電的化合物為電解質,故為電解質的是①③⑦,故答案為:①③⑦;
(3)碳酸氫鈉屬于強電解質,溶液中完全電離,碳酸氫鈉的電離方程式為:NaHCO3═Na++HCO3-;
HF是弱酸,電離離子方程式為:HF?H++F-;
KOH為強電解質,在溶液中能完全電離,電離方程式為:KOH=K++OH-;
故答案為:NaHCO3═Na++HCO3-;HF?H++F-;KOH=K++OH-.
點評 本題考查了電解質、非電解質的概念區分以及電離方程式的書寫,難度不大,應注意的是電解質和非電解質均為化合物.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 蒸發操作時,應使混合物中的水分完全蒸干后,再移走酒精燈停止加熱 | |
| B. | 蒸餾實驗中,溫度計的水銀球應插入液態混合物中 | |
| C. | 用酒精萃取溴水中的溴單質的操作可選用分液漏斗,而后靜置分液 | |
| D. | 蒸餾時,蒸餾時冷凝水從冷凝管下口進上口出 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
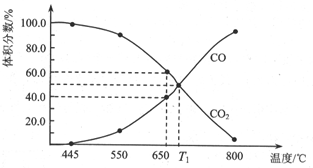 一定量的CO2與足量的C在恒容密閉容器中發生反應:C(s)+CO2(g)?2CO(g)△H.
一定量的CO2與足量的C在恒容密閉容器中發生反應:C(s)+CO2(g)?2CO(g)△H.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
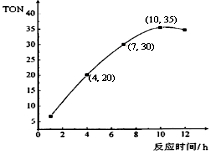 甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇轉化率通常不會超過1%,制約該反應走向工業化生產.
甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇轉化率通常不會超過1%,制約該反應走向工業化生產.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 達到化學平衡時,將完全轉化為NH3 | |
| B. | 達到化學平衡時,N2、H2和NH3的物質的量濃度一定相等 | |
| C. | 達到化學平衡時,N2、H2和NH3的物質的量濃度不再變化 | |
| D. | 達到化學平衡時,正反應速率和逆反應速率都為零 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
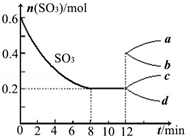 在一個2L的密閉容器中投入反應物,發生反應2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的變化如圖所示:
在一個2L的密閉容器中投入反應物,發生反應2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的變化如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定條件下水由氣態變為液態 | |
| B. | 高溫高壓條件下使石墨轉化為金剛石 | |
| C. | 有序排列的火柴散落 | |
| D. | CO點燃時生成CO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com