
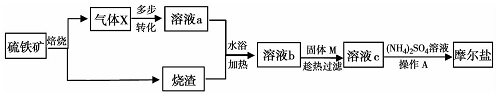
分析 由流程圖可知:硫鐵礦焙燒:4FeS+7O2$\frac{\underline{\;高溫\;}}{\;}$2Fe2O3+4SO2↑,則燒渣主要成分為Fe2O3,氣體X為二氧化硫,X經多步轉化為硫酸溶液,再與燒渣得到溶液b為硫酸鐵溶液,加入固體M得溶液c,c與硫酸銨得到摩爾鹽,則c為亞鐵離子的溶液,故固體M應為鐵粉,溶液c為硫酸亞鐵溶液,向其中加入硫酸銨經過蒸發濃縮、冷卻結晶、過濾、洗滌、干燥制得的硫酸亞鐵銨晶體,據此分析.
解答 解:硫鐵礦焙燒:4FeS+7O2$\frac{\underline{\;高溫\;}}{\;}$2Fe2O3+4SO2↑,則燒渣主要成分為Fe2O3,氣體X為二氧化硫,X經多步轉化為硫酸溶液,再與燒渣得到溶液b為硫酸鐵溶液,加入固體M得溶液c,c與硫酸銨得到摩爾鹽,則c為亞鐵離子的溶液,故固體M應為鐵粉,溶液c為硫酸亞鐵溶液,
(1)提高硫鐵礦反應速率的措施有粉碎硫鐵礦增大接觸面積,攪拌加速反應等;
故答案為:粉碎、攪拌等;
(2)氣體X為二氧化硫,則400℃時,催化劑作用下氣體X與空氣反應的化學方程式為:2SO2+O2$\frac{\underline{\;\;\;400℃\;\;\;}}{催化劑}$2SO3;
故答案為:2SO2+O2$\frac{\underline{\;\;\;400℃\;\;\;}}{催化劑}$2SO3;
(3)溶液b為硫酸鐵溶液,加入固體M得溶液c,c與硫酸銨得到摩爾鹽,則c為亞鐵離子的溶液,故固體M應為鐵粉,趁熱過濾的目的是避免溫度降低,硫酸亞鐵晶體析出而造成損失;
故答案為:鐵粉;趁熱過濾的目的是避免溫度降低,硫酸亞鐵晶體析出而造成損失;
(4)向硫酸亞鐵溶液中加入硫酸銨經過蒸發濃縮、冷卻結晶、過濾、洗滌、干燥制得的硫酸亞鐵銨晶體;摩爾鹽不溶于乙醇,故為了減少產品的溶解,且便于產品干燥,選擇乙醇洗滌晶體;
故答案為:冷卻結晶;減少產品的溶解,且便于產品干燥;
(5)①滴定終點利用高錳酸鉀溶液呈紫紅色做指示劑指示到終點;
故答案為:滴入高錳酸鉀溶液不褪色且半分鐘不變;
②高錳酸鉀與Fe2+的反應是MnO4-~Mn2+~5e-;Fe2+~Fe3+~e-;依據電子守恒,鐵離子和亞鐵離子前乘5,依據原子守恒和電荷守恒得到反應的離子方程式為:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
故答案為:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
③根據5Fe2+~MnO4-,則n(摩爾鹽)=n(Fe2+)=5n(MnO4-)=5×0.1000mol/L×0.01L=0.005mol,產品中摩爾鹽的質量為:0.005mol×392g/mol=1.96g,則該產品的純度為:$\frac{1.96g}{2g}×100%$=98%;
故答案為:98%.
點評 本題以莫爾鹽的制備為載體,考查物質分離提純、氧化還原反應滴定應用以計算、以及在新情境下綜合運用知識解決問題的能力等.題目有一定的難度.需學生具有扎實的基礎知識與靈活運用知識解決問題的能力.


 名牌中學課時作業系列答案
名牌中學課時作業系列答案 明天教育課時特訓系列答案
明天教育課時特訓系列答案 浙江新課程三維目標測評課時特訓系列答案
浙江新課程三維目標測評課時特訓系列答案 周周清檢測系列答案
周周清檢測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 苯分子中的6個碳原子之間的鍵完全相同,是一種介于碳碳單鍵和碳碳雙鍵之間獨特的鍵 | |
| B. | 將溴水加入苯中,溴水的顏色變淺,這是由于發生了加成反應 | |
| C. | 乙烷和丙烯的物質的最共1mol,完全燃燒后生成3molH2O | |
| D. | 主鏈上有5個碳原子的庚烷有5 種同分異構體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 做電解池的陰極,和外加電源的負極相連 | |
| B. | 做電解池的陰極,和外加電源的正極相連 | |
| C. | 做電解池的陽極,和外加電源的負極相連 | |
| D. | 做電解池的陽極,和外加電源的正極相連 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應③為放熱反應 | |
| B. | 當容器內濕埋不再變化時,上述各反應均達到化學平衡狀態 | |
| C. | 當混合氣體的密度不再變化時,上述各反應均達到化學平衡狀態 | |
| D. | 若反應①的平衡常數為K1,反應②的平衡常數為K2,則反應③的平衡常數K3=2K1•K2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發過程中用玻璃棒不斷攪拌 | |
| B. | 先用酒精燈加熱蒸發皿,再將濾液倒入蒸發皿中 | |
| C. | 當加熱至蒸發皿中有較多固體析出時停止加熱,利用余熱將液體蒸干 | |
| D. | 蒸發完成時,用坩堝鉗把蒸發皿移至石棉網上 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com