
 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案 期末好成績系列答案
期末好成績系列答案科目:高中化學 來源: 題型:閱讀理解
 CO2、SO2、NOx是對環境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應、減少酸雨和光化學煙霧的有效途徑.
CO2、SO2、NOx是對環境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應、減少酸雨和光化學煙霧的有效途徑.| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江西省吉安二中高二下學期教學競賽化學試卷(帶解析) 題型:填空題
(14分) CO2、SO2、NOx是對環境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應、減少酸雨和光化學煙霧的有效途徑。
(1)下列措施中,有利于降低大氣中的CO2、SO2、NOx濃度的是 (填序號)
| A.減少化石燃料的使用,開發新能源 |
| B.使用無氟冰箱,減少氟利昂排放 |
| C.多步行或乘公交車,少用私家車 |
| D.將工業廢氣用堿液吸收后再排放 |
 n(H+)= mol。
n(H+)= mol。 N2O4(g) △H<0的平衡常數K=13.3。
N2O4(g) △H<0的平衡常數K=13.3。 CH3OH(g),己知該反應在300OC時的化學平衡常數為0.27,該溫度下將2moI CO、3mol H2利2molCH3OH(g)充入容積為2 L的密閉容器中,此時反應將 。(填“向正反應方向進行”、“向逆反應方向進行”或“處于平衡狀態”)。
CH3OH(g),己知該反應在300OC時的化學平衡常數為0.27,該溫度下將2moI CO、3mol H2利2molCH3OH(g)充入容積為2 L的密閉容器中,此時反應將 。(填“向正反應方向進行”、“向逆反應方向進行”或“處于平衡狀態”)。查看答案和解析>>
科目:高中化學 來源:2012-2013學年四川省成都高新區高三9月統一檢測化學試卷(解析版) 題型:填空題
CO2 、SO2 、NOx 是對環境影響較大的氣體,控制和治理CO2、SO2、NOx 是解決溫室效應、減少酸雨和光化學煙霧的有效途徑。
(1)下列措施中,有利于降低大氣中的CO2、SO2、NOx 濃度的有 (填字母)
a.減少化石燃料的使用,開發新能源
b.使用無氟冰箱,減少氟里昂排放
c.多步行或乘公交車,少用專車或私家車
d.將工業廢氣用堿液吸收后再排放
(2)為了降低汽車尾氣對大氣的污染,有關部門擬用甲醇替代作為公交車的燃料。寫出用合成氣(CO和H2)生產甲醇的化學方程式 ,已知該反應合成1 mol液態甲醇吸收熱量131.9 kJ, 2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g) △H =-594.1 kJ·mol-1,請寫出液態甲醇燃燒生成二氧化碳和水蒸氣的熱化學方程式 。
(3)有人設想以下圖所示裝置用電化學原理將CO2、SO2 轉化為重要化工原料。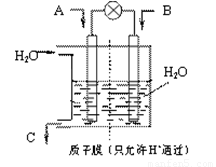
若A為CO2,B為H2,C為CH3OH,則通入CO2 的一極為 極;若A為SO2,B為O2,C為H2SO4。則負極的電極反應式為 ;
(4)①在研究氮的氧化物的轉化時,某小組查閱到以下數據:17℃、1.01×105 Pa時,
2NO2(g)
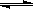 N2O4(g) △H <0的平衡常數 K=13.3,則該條件下密閉容器中N2O4
和NO2的混合氣體達到平衡時,若 c (NO2)
= 0.0300 mol·L-1,
N2O4(g) △H <0的平衡常數 K=13.3,則該條件下密閉容器中N2O4
和NO2的混合氣體達到平衡時,若 c (NO2)
= 0.0300 mol·L-1,
c (N2O4)= (保留兩位有效數字);
②改變上述體系的某個條件,達到新的平衡后,測得混合氣體中 c (NO2) = 0.04 mol·L-1, c (N2O4) = 0.007 mol·L-1,則改變的條件為 ;
查看答案和解析>>
科目:高中化學 來源:2013屆江西省高二下學期教學競賽化學試卷(解析版) 題型:填空題
(14分) CO2、SO2、NOx是對環境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應、減少酸雨和光化學煙霧的有效途徑。
(1)下列措施中,有利于降低大氣中的CO2、SO2、NOx濃度的是 (填序號)
A、減少化石燃料的使用,開發新能源
B、使用無氟冰箱,減少氟利昂排放
C、多步行或乘公交車,少用私家車
D、將工業廢氣用堿液吸收后再排放
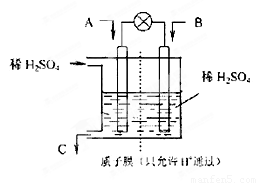
(2)有學者設想以右圖所示裝置用電化學原理將CO2、SO2轉化為重要化工原料。
①若A為CO2,B為H2,C為CH3OH,則正極的電極反應式為 ;
②若A為SO2,B為O2,C為H2SO4,則負極的電極反應式為 ;
當電路中有1 mol e-流過,正極區溶液中的H+的物質的量的變化量 n(H+)=
mol。
n(H+)=
mol。
(3)在研究氮的氧化物的轉化時,某小組查閱到以下數據:l7℃、l.01×l05Pa時,2NO2(g) N2O4(g)
△H<0的平衡常數K=13.3。
N2O4(g)
△H<0的平衡常數K=13.3。
①若該條件下密閉容器中N2O4和NO2的混合氣體達到平衡時,c(NO2)=0.0300mol.L-1,
則c(N2O4)= 。(保留兩位有效數字)
②若改變上述體系的某一個條件,達到新的平衡后,測得混合氣體中c(NO2)=0.04 mol.L-1,c(N2O4)=0.007 mol.L-1,則改變的條件為 。
(4)為了降低汽車尾氣對大氣的污染,有關部門擬用甲醇替代作為公交車的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g) CH3OH(g),己知該反應在300OC時的化學平衡常數為0.27,該溫度下將2moI CO、3mol H2利2molCH3OH(g)充入容積為2 L的密閉容器中,此時反應將
。(填“向正反應方向進行”、“向逆反應方向進行”或“處于平衡狀態”)。
CH3OH(g),己知該反應在300OC時的化學平衡常數為0.27,該溫度下將2moI CO、3mol H2利2molCH3OH(g)充入容積為2 L的密閉容器中,此時反應將
。(填“向正反應方向進行”、“向逆反應方向進行”或“處于平衡狀態”)。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年河北省保定市淶水縣祖沖之中學高二(上)期中化學試卷(化學反應原理)(解析版) 題型:解答題
 O2(g)═CO2(g)+2H2O(l)△H=-594.1kJ mol-1則表示液態甲醇燃燒熱的熱化學方程式為______.
O2(g)═CO2(g)+2H2O(l)△H=-594.1kJ mol-1則表示液態甲醇燃燒熱的熱化學方程式為______.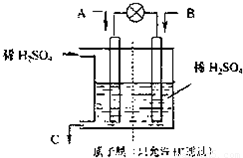
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com