
已知在常溫常壓下:
①2C H3OH(l)+3O2(g)=2CO2(g)+4
H3OH(l)+3O2(g)=2CO2(g)+4 H2O(l) ΔH=-1451.6kJ/mol
H2O(l) ΔH=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ/mol
(1)寫出甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式_______________
(2)某小組根據甲醇燃燒的反應原理,設計如圖所示的電池裝置:
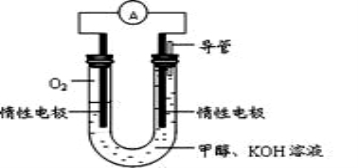
該電池正極的電極反應式____________________
工作一段時間后,測得溶液的pH______________(填增大、減小或不變),則該電池總反應的離子方程式__________________
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源:2016-2017學年天津市紅橋區高一上學期期中化學試卷(解析版) 題型:填空題
(1)寫出下列物質在水溶液中的電離方程式:
①Ba(OH)2: ;
②NaHSO4: ;
③寫出①②水溶液混合后恰好沉淀完全的離子方程式______________________
(2)砷及其化合物有毒,如砒霜(As2O3)有劇毒,環境監測和法醫學分析砒霜中毒的反應原理:As2O3+6Zn+12HCl=6ZnCl2+2AsH3↑+3H2O,①反應中還原劑是 ,被還原的元素是 ,(用化學式回答)若參加反應Zn的質量為19.5g,則生成的氣體在標準狀況下的體積為_________L,
②用雙線橋法標出上述反應中電子轉移的方向和數目。
(3)實驗室里需要純凈的NaCl溶液,但手邊只有混有Na2SO4、NH4HCO3的NaCl.某學生設計了如圖所示方案提取純凈的NaCl溶液.(已知:NH4HCO3 NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)
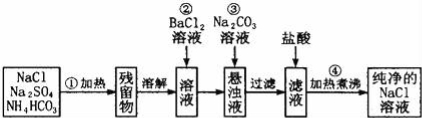
①150℃時,一定量的NH4HCO3完全分解后所得氣體的平均相對分子質量為 (保留至小數點后一位).
②操作③所得到的懸濁液與膠體的本質區別是 .
③進行操作②后,判斷SO42﹣是否已除盡方法是 .
④操作②加BaCl2溶液后生成沉淀,不必進行過濾就可進行操作③加碳酸鈉溶液,其理由是 .
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市河東區高二上學期期中質檢化學試卷(解析版) 題型:選擇題
下列過程中,需要增大化學反應速率的是
A.鋼鐵腐蝕 B.食物腐敗 C.工業合成氨 D.塑料老化
查看答案和解析>>
科目:高中化學 來源:2017屆貴州省高三上月考三化學試卷(解析版) 題型:實驗題
某化學興趣小組設計了如下實驗流程,用含有鋁、鐵和銅的合金廢料制取氯化鋁、綠礬晶體和膽礬晶體。
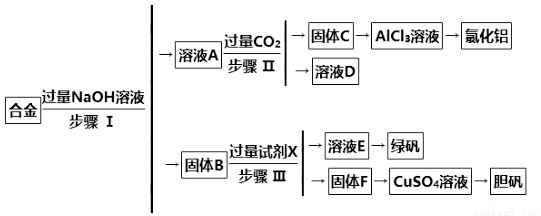
請回答:
(1)寫出綠礬的化學式:______ ____________。試劑X是 。
____________。試劑X是 。
(2)步驟Ⅰ、Ⅱ、Ⅲ中均需進行的實驗操作是____________。
(3)溶液E得到綠礬晶體的實驗操作 。
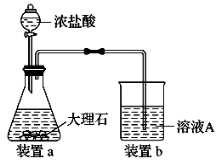
(4)進行步驟Ⅱ時,該小組用如圖所示裝置及試劑制取CO2并將制得的氣體通入溶液A中。一段時間后,觀察 到燒杯中產生的白色沉淀會逐漸減少。為了避免固體C減少,可采取的改進措施是__________。
到燒杯中產生的白色沉淀會逐漸減少。為了避免固體C減少,可采取的改進措施是__________。
(5)用固體F制備CuSO4溶液,可設計以下三種途徑:

寫出途徑①中反應的離子方程式:__________________________,
請選出你認為的最佳途徑并說明選擇的理由:______________________________。
查看答案和解析>>
科目:高中化學 來源:2017屆貴州省高三上月考三化學試卷(解析版) 題型:選擇題
設NA代表阿伏加德羅常數的數值.則下列有關敘述正確的是( )
A.1molFeI2與足量氯氣反應時轉移的電子數2 NA
B.在1L 0.1mol/L的Na2CO3溶液中,陰離子總數小于0.1NA
C.7.8g過氧化鈉用于呼吸面具中完全反應時轉移電子總數為0.1 NA
D.將1L 2mol/L的FeCl3溶液加入到沸水中,加熱使之完全反應,所得氫氧化鐵膠體粒子數為2NA
查看答案和解析>>
科目:高中化學 來源:2016屆內蒙古高三上學期期中化學試卷(解析版) 題型:選擇題
下列關于碳酸鈉和碳酸氫鈉的性質敘述正確的是( )
A、受熱時NaHCO3比Na2CO3穩定
B、等質量NaHCO3、Na2CO3分別與足量鹽酸反應,NaHCO3放出CO2更多
C、在水中NaHCO3比Na2CO3溶解度大
D、物質的量相等的NaHCO3和Na2CO3分別與足量鹽酸反應,放出CO2的物質的量之比為2:1
查看答案和解析>>
科目:高中化學 來源:2016屆內蒙古高三上學期期中化學試卷(解析版) 題型:選擇題
關于NA的說法正確 的是( )
的是( )
A、標準狀況下,2.24 L氯氣與足量氫氧化鈉溶液完全反應轉移電子數目為0.2 NA
B、向FeI2溶液中通入足量氯 氣,當有1 mol Fe2+被氧化時轉移電子數目為 NA
氣,當有1 mol Fe2+被氧化時轉移電子數目為 NA
C、在過氧化鈉與水的反應中,每生成0.1 mol氧氣,轉移電子數目為0.4 NA
D、常溫、常壓下1.6 g O2與O3的混合物中,氧原子數目為0.1 NA
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高二上期中化學卷(解析版) 題型:選擇題
下列說法正確的是
A.根據溶液中有CH3COOH、CH3COO-和H+即可證明CH3COOH達到電離平衡狀態
B.根據溶液中CH3COO-和H+的物質的量濃度相等即可證明CH3COOH達到電離平衡狀態
C.當NH3·H2O達到 電離平衡時,溶液中NH3·H2O、NH4+和OH-的濃度相等
電離平衡時,溶液中NH3·H2O、NH4+和OH-的濃度相等
D.H2CO3是分步電離的,電離程度依次減弱
查看答案和解析>>
科目:高中化學 來源:2016-2017學年云南省高二上期中化學卷(解析版) 題型:選擇題
已知某可逆反應在密閉容器中進行:A(g)+2B(g) 3C(g)+D(s) △H>0,A的轉化率與時間t關系如圖所示,圖中曲線a代表一定條件下該反應的過程。若使a曲線變為b曲線,可能采取的措施是(
3C(g)+D(s) △H>0,A的轉化率與時間t關系如圖所示,圖中曲線a代表一定條件下該反應的過程。若使a曲線變為b曲線,可能采取的措施是(  )
)

A.增大A的濃度或減少C的濃度
B.縮小容器的容積或加入 催化劑
催化劑
C.升高溫度或增大壓強
D.移走部分D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com