
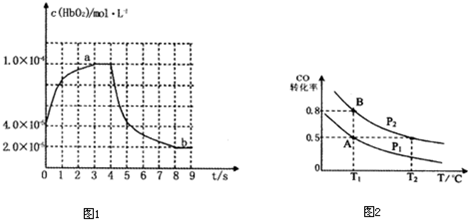
如右圖所示將4mol SO2和2mol O2混合置于體積可變的等壓容器中,在一定溫度下發生如下反應:2SO2(g)+O2(g) ![]() 2SO3(g);ΔH<0。該反應達到平衡狀態A時,測得氣體總物質的量為4.2 mol。若SO2、O2、SO3的起始物質的量分別用a、b、c 表示,回答下列問題:
2SO3(g);ΔH<0。該反應達到平衡狀態A時,測得氣體總物質的量為4.2 mol。若SO2、O2、SO3的起始物質的量分別用a、b、c 表示,回答下列問題:
 ⑴ 在達到平衡狀態A的容器中通入少量O2,體系中SO2的體積分數__減小__(填“增大”或“減小”或“不變”),若要使SO2的體積分數再變到與平衡狀態A相同,可采取的措施有: 或 。
⑴ 在達到平衡狀態A的容器中通入少量O2,體系中SO2的體積分數__減小__(填“增大”或“減小”或“不變”),若要使SO2的體積分數再變到與平衡狀態A相同,可采取的措施有: 或 。
⑵ 若起始時a=1.2mol,b=0.6mol,且達到平衡后各氣體的體積分數與平衡狀態A相同,則起始時c的取值為 。
⑶ 若要使反應開始時向逆反應方向進行,且達到平衡后各氣體的物質的量與平衡狀態A相同,則起始時c的取值范圍是 。
科目:高中化學 來源: 題型:閱讀理解
| 1 |
| 10000 |
| 1 |
| 10000 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 2009年12月7日一18日在丹麥首都哥本哈根召開的聯合國氣候會議,就未來應對氣候變化的全球行動簽署新的協議.而如何降低大氣中CO2的含量及有效地開發利用CO2,引起了全世界的普遍重視.為減小和消除CO2對環境的影響,一方面世界各國都在限制其排放量,另一方面科學家加強了對CO2創新利用的研究.
2009年12月7日一18日在丹麥首都哥本哈根召開的聯合國氣候會議,就未來應對氣候變化的全球行動簽署新的協議.而如何降低大氣中CO2的含量及有效地開發利用CO2,引起了全世界的普遍重視.為減小和消除CO2對環境的影響,一方面世界各國都在限制其排放量,另一方面科學家加強了對CO2創新利用的研究.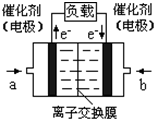 意圖,則a處通入的是
意圖,則a處通入的是查看答案和解析>>
科目:高中化學 來源: 題型:
實驗題:(本題共12分)
(1)用18.4mol/L的濃H2SO4配制100ml濃度為1mol/L的稀H2SO4,其操作可分為以下各步:
A.用量筒量取5.4ml濃H2SO4緩緩注入裝有約50ml蒸餾水的燒杯中,并用玻璃棒攪拌;
B.用約30ml蒸餾水,分成3次洗滌燒杯和玻棒,將每次洗滌液都注入容量瓶中;
C.將稀釋后的H2SO4小心倒入100ml容量瓶里;
D.檢查100ml容量瓶口部是否會發生滴漏;
E、用量筒加蒸餾水至容量瓶中液面接近刻度2cm處;
F、蓋緊瓶塞,反復顛倒振蕩,搖勻溶液;
G、用膠頭滴管向容量瓶里逐滴滴加蒸餾水至液面最低點和刻度線相平,試填空
①正確的操作順序為(用字母填寫) 。
②進行A步操作時,應選擇下列量器 (填序號)
a、10ml量筒 b、50ml量筒 c、100ml量筒
③如果對裝有濃H2SO4的量筒讀數如右圖所示,配制的稀H2SO4的濃度
將 (偏高、偏低、無影響)
④進入A步操作后,必須 后才能進行C操作。
(2)只從下列試劑中選擇實驗所需的試劑,采用兩種不同的方法區分0.1mol/L的H2SO4和0.01mol/LH2SO4溶液,簡述其操作過程:
試劑:紫色石蕊試液、酚酞試液、甲基橙試液、蒸餾水、BaCl2溶液、pH試紙、0.1mol/L Na2S2O3溶液
方法一:
。
方法二:
。
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
2009年12月7日~18日在丹麥首都哥本哈根召開的聯合國氣候會議,就未來應對氣候變化的全球行動簽署新的協議。而如何降低大氣中CO2的含量及有效地開發利用CO2,引起了全世界的普遍重視。為減小和消除CO2對環境的影響,一方面世界各國都在限制其排放量,另一方面科學家加強了對CO2創新利用的研究。
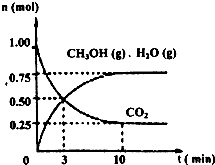
(1)目前工業上有一種方法是用CO2來生產燃料甲醇。為探究該反應原理,進行如下實驗:某溫度下,在容積為2L的密閉容器中,充入1mol CO2和3.25mol H2,在一定條件下發生反應,測得CO2、CH3OH(g)和H2O(g)的物質的量(n)隨時間變化如右圖所示:
① 從反應開始到平衡,氫氣的平均反應速
![]() (H2)=_______。
(H2)=_______。
②下列措施中一定不能使![]() (CH3OH)/ (CO2)增大的是_____。
(CH3OH)/ (CO2)增大的是_____。
A.降低溫度 B.縮小容器的容積
C.將水蒸氣從體系中分離 D.使用更有效的催化劑
(2)常溫常壓下,飽和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的電離及H2CO3的第二級電離,則H2CO3HCO3-+H+的電離平衡常數K=___________。(已知:10-5.6=2.5×10-6)。
(3)標準狀況下,將1.12L CO2通入100mL 1mol·L-1的NaOH溶液中,所得溶液中離子濃度由大到小的順序為
________________;
(4)如圖是乙醇燃料電池(電解質溶液為KOH溶液)的結構示意圖,則a處的通入的是_____________(填“乙醇”或“氧氣”),b處電極上發生的電極反應是___________
__________________________________________。
(5)CO2在自然界循環時可與CaCO3反應,CaCO3是一種難溶物質,其Ksp=2.8×10-9。CaCl2溶液與Na2CO3溶液混合可形成CaCO3沉淀,現將等體積的CaCl2溶液與Na2CO3溶液混合,若Na2CO3溶液的濃度為2×10-4mol/L,則生成沉淀所需CaCl2溶液的最小濃度為_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com