
| A. | 實驗①說明Na2S2O3溶液中水電離的c(OH-)=l0-8 mol.L-l | |
| B. | Na2S2O3溶液pH=8的原因用離子方程式表示為S2O32-+2H2O?Na2S2O3+2OH- | |
| C. | 生成的沉淀B可能是BaSO3或BaSO4,要進一步確認還需再加入稀硝酸驗證 | |
| D. | 實驗②說明Na2S2O3具有還原性 |
分析 常溫下,由pH=8$\underset{\stackrel{①}{←}}{pH試紙}$Na2S2O3溶液可知,pH=8,溶液水解顯堿性,c(H+)水=c(OH-)水=l0-6 mol.L-l,由Na2S2O3溶液$→_{同時加入氯化鋇溶液}^{②加入足量氨水}$白色沉淀B可知,發生S2O32-+5H2O+4Cl2+2Ba2+=2BaSO4↓+8Cl-+10H+,以此來解答.
解答 解:A.實驗①說明Na2S2O3溶液中水電離的c(OH-)=l0-6 mol.L-l,促進水的電離,故A錯誤;
B.Na2S2O3溶液pH=8的原因用離子方程式表示為S2O32-+H2O?HS2O3-+OH-,故B錯誤;
C.BaSO3與硝酸發生氧化還原反應生成BaSO4,不能加硝酸驗證,故C錯誤;
D.實驗②發生S2O32-+5H2O+4Cl2+2Ba2+=2BaSO4↓+8Cl-+10H+,S元素的化合價升高,說明Na2S2O3具有還原性,故D正確;
故選D.
點評 本題考查性質實驗方案的設計,為高頻考點,涉及鹽類水解、氧化還原反應等,把握反應原理及物質的性質為解答的關鍵,側重分析與實驗能力的考查,題目難度不大.


科目:高中化學 來源: 題型:解答題
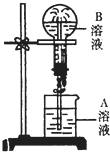 如圖為噴泉實驗裝置圖.
如圖為噴泉實驗裝置圖.| 實驗編號 | A溶液顏色 | B溶液顏色 | A溶液中溶質 |
| ① | 無色 | 紅色 | 酚酞 |
| ② | 黃色 | 紅褐色渾濁 | Fe3+(FeCl3等) |
| ③ | 紫色 | 藍色 | 石蕊 |
| ④ | 無色 | 乳白色渾濁 | Al3+或Mg2+(AlCl3、MgCl2等) |
 NH3•H2O
NH3•H2O NH4++OH-,溶液呈堿性,遇酚酞顯紅色.實驗②反應的離子方程式為Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.
NH4++OH-,溶液呈堿性,遇酚酞顯紅色.實驗②反應的離子方程式為Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可用CCl4萃取碘酒中的碘 | |
| B. | 做焰色反應實驗時,透過藍色鈷玻璃,觀察到火焰顏色為紫色,證明被檢驗物為一定為鉀鹽 | |
| C. | 不慎將濃堿溶液沾到皮膚上,要立即用大量水沖洗,然后涂上2%~5%的硼酸溶液 | |
| D. | 室溫下,濃度為0.1mol•L-1Na2S2O3和H2SO4溶液,分別取5mL與10mL混合,10mL與10mL混合,可驗證Na2S2O3濃度對反應速率的影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 新能源汽車的推廣與使用有助于減少光化學煙霧的產生 | |
| B. | 為了防止月餅等富脂食品氧化變質,常在包裝袋中放入生石灰 | |
| C. | “碳納米泡沫”倍稱為第五形態的單質碳,它與石墨弧稱為同位素 | |
| D. | 海水淡化能解決淡水供應危機,向海水中加入凈水劑明礬可以使海水淡化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 外電路電子的移動方向:A→電源→B | |
| B. | 氣體X在反應中通常體現還原性 | |
| C. | 電極D為惰性電極,E為活潑電極 | |
| D. | 電極D的電極反應式為C6H6+6H++6e-═C6H12 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向銀氨溶液中加入鹽酸:[Ag(NH3)2]++OH-+3H+=Ag++2NH4++H2O | |
| B. | 在少量Mg(OH)2懸濁液中加入氯化銨濃溶液:Mg(OH)2+2NH4+=2NH3•H2O+Mg2+ | |
| C. | 向硫酸鐵溶液中加入硫化鈉溶液:2Fe3++3S2-+6H2O=2Fe(OH)3↓+3H2S↑ | |
| D. | NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+=H2O+BaCO3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電池工作時,鋅失去電子 | |
| B. | 電池正極的電極反應式為2MnO2+H2O+2e-═Mn2O3+2OH- | |
| C. | 外電路中每通過0.2mol電子,鋅的質量理論上減少13g | |
| D. | 電池工作時,電子由負極通過外電路流向正極 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com