


分析 向鎂鋁合金中加入足量氫氧化鈉溶液,發生反應:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,鎂不反應,固體A為Mg,采用過濾的方法進行分離,向濾液中通入二氧化碳,發生反應:NaAlO2+CO2+2H2O═Al(OH)3
↓+NaHCO3,再通過過量進行分離,固體B為氫氧化鋁,氫氧化鋁與硫酸反應得到硫酸鋁溶液,再經過蒸發濃縮、冷卻結晶、洗滌、干燥得到硫酸鋁晶體;
(1)Al和氫氧化鈉溶液生成可溶性的偏鋁酸鈉,鎂不反應;
(2)從溶液中獲得晶體,需要經過蒸發濃縮、冷卻結晶、過濾、洗滌、干燥等操作;
(3)用乙醇洗滌,可以減少晶體的溶解,有利于晶體的干燥;
(4)Al的質量為9g-4.95g=4.05g,設硫酸鋁晶體化學式為:Al2(SO4)3.nH2O,根據Al元素守恒計算硫酸鋁晶體的物質的量,再計算硫酸鋁晶體的相對分子質量,進而計算n的值,確定化學式;
(5)根據(4)中計算可知,晶體中結晶水的質量分數,低溫加熱,首先失去結晶水,高溫下,最終硫酸鋁分解,根據失重%計算判斷各階段分解產物,再書寫化學方程式.
解答 解:向鎂鋁合金中加入足量氫氧化鈉溶液,發生反應:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,鎂不反應,固體A為Mg,采用過濾的方法進行分離,向濾液中通入二氧化碳,發生反應:NaAlO2+CO2+2H2O═Al(OH)3
↓+NaHCO3,再通過過量進行分離,固體B為氫氧化鋁,氫氧化鋁與硫酸反應得到硫酸鋁溶液,再經過蒸發濃縮、冷卻結晶、洗滌、干燥得到硫酸鋁晶體;
(1)Al和氫氧化鈉溶液生成可溶性的偏鋁酸鈉與氫氣,鎂不反應,反應方程式為:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,由上述分析可知,固體B為Al(OH)3,
故答案為:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;Al(OH)3;
(2)從溶液中獲得晶體,需要經過蒸發濃縮、冷卻結晶、過濾、洗滌、干燥等操作,
故答案為:冷卻結晶、過濾;
(3)用乙醇洗滌,可以減少晶體的溶解,有利于晶體的干燥,
故答案為:可以減少晶體的溶解,有利于晶體的干燥;
(4)Al的質量為9g-4.95g=4.05g,其物質的量為$\frac{4.05g}{27g/mol}$=0.15mol,設硫酸鋁晶體化學式為:Al2(SO4)3.nH2O,根據Al元素守恒,硫酸鋁晶體的物質的量為$\frac{0.15mol}{2}$=0.075mol,故硫酸鋁晶體的相對分子質量為$\frac{49.95}{0.075}$=666,則54+96×3+18n=666,解得n=18,故該硫酸鋁晶體的化學式為:Al2(SO4)3.18H2O,
故答案為:Al2(SO4)3.18H2O;
(5)晶體中結晶水的含量為$\frac{18×18}{666}$=48.65%,故第二階段完全失去結晶水,得到物質為Al2(SO4)3,第一階段失去部分結晶水,失去結晶水數目為$\frac{666×40.54%}{18}$=15,故第一階段得到的物質為Al2(SO4)3.3H2O,
第三階段剩余物質的相對分子質量為666×(1-84.68%)=102,應是Al2O3,故硫酸鋁反應生成氧化鋁與三氧化硫,反應方程式為:Al2(SO4)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3SO3↑,
故答案為:Al2(SO4)3.3H2O;Al2(SO4)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3SO3↑.
點評 本題考查實驗制備方案、物質分離提純、方案分析評價、物質組成測定等,是對學生綜合能力的考查,注意(5)中充分利用硫酸鋁晶體相對分子質量進行計算解答,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | Y元素為Na元素 | B. | X只能位于第3周期 | ||
| C. | a+n-b+m=10或16 | D. | Y不可能位于第2周期 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | M與X形成的化合物對應的水化物一定是強酸 | |
| B. | Y2X和Y2X2中化學鍵類型完全相同 | |
| C. | X、Y的簡單離子半徑:r(X2-)>r(Y+) | |
| D. | M的氣態氫化物比N的氣態氫化物穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 是離子化合物,含有離子鍵和共價鍵 | |
| B. | 電子式是 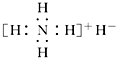 | |
| C. | 與水反應時,它既是還原劑又是氧化劑 | |
| D. | 固體投入少量的水中,有兩種氣體產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 實驗現象 | 反應方程式 |
| 1.將少量氯水加入盛有NaBr溶液的試管中,用力振蕩后加入少量四氯化碳,振蕩、靜置 | 上層為淺黃色(或無色) 下層為橙色 | 離子方程式: Cl2+2Br-=Br2+2 Cl- |
| 1.將少量溴水加入盛有NaI溶液的試管中,用力振蕩后加入少量四氯化碳,振蕩、靜置 | 上層為淺黃色(或無色) 下層為紫紅色 | 化學方程式: Br2+2NaI=I2+2NaBr |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 逸出ClO2使生成物濃度降低 | B. | 酸使HClO2的分解加速 | ||
| C. | 溶液中的H+起催化作用 | D. | 溶液中的Cl-起催化作用 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
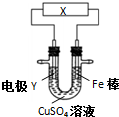
| A. | 若X為直流電源,Y為銅棒接正極,則Fe棒上鍍銅 | |
| B. | 若X為直流電源,Y為碳棒接負極,則Fe棒被保護 | |
| C. | 若X為電流計,Y為鋅棒,則SO42- 移向Fe棒 | |
| D. | 若X為導線,Y為銅棒,則Fe棒發生還原反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com