
A.此過程為混亂程度小的向混亂程度大的方向的變化過程,即熵增大的過程?
B.此過程為自發過程,而且沒有熱量的吸收或放出?
C.此過程從有序到無序,混亂度增大?
D.此過程是自發可逆的?
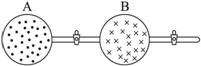
圖1?
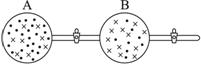
圖2 理想氣體的自發混合
科目:高中化學 來源: 題型:
| 3 | 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 (2009?丹東模擬)甲醇可以與水蒸氣反應生成氫氣,反應方程式如下:
(2009?丹東模擬)甲醇可以與水蒸氣反應生成氫氣,反應方程式如下:查看答案和解析>>
科目:高中化學 來源: 題型:
| [CH3OH] |
| [CO][H2]2 |
| [CH3OH] |
| [CO][H2]2 |

| b-a-4c |
| 2 |
| b-a-4c |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
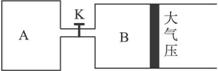
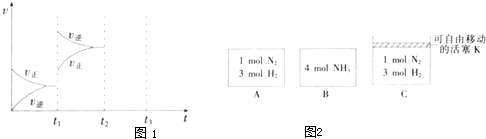
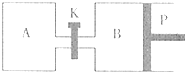
(1)設A、B兩容器中化學平衡常數分別為K1和K2,則它們的大小關系是K1_________K2(填“大于”“等于”或“小于”)。
(2)B中X的轉化率α(X)B為____________。
(3)A中Z和B中的W物質的量的比較:n(Z)A________n(W)B(填“大于”“等于”或“小于”)。
(4)打開K,過一段時間重新達平衡(Ⅱ)時,B的體積為__________ L(用含a的代數式表示,連通管中氣體體積不計);在溫度不變的情況下,要使B容器恢復原來反應前的體積,可采取的措施是_________________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com