
 液480mL.
液480mL.分析 (1)根據儀器的結構特點判斷;
(2)分離四氯化碳和酒精的混合物需用蒸餾,必須用酒精燈加熱;
(3)①根據n=cv計算溶質Na2CO3的物質的量,利用Na2CO3•10H2O的物質的量等于Na2CO3的物質的量,根據m=nM計算Na2CO3•10H2O的質量;
②根據配制一定物質的量濃度的溶液的步驟是稱量、溶解、冷卻、移液、洗滌、定容、搖勻和裝瓶來分析所需的儀器;
③根據c=$\frac{n}{V}$分析操作對溶質的物質的量或對溶液的體積的影響判斷;
④容量瓶只有一條刻度線,只能用容量瓶配制出與其規格相對應的體積的溶液;移液時必須要用玻璃棒引流.
解答 解:(1)①為蒸餾燒瓶,②為錐形瓶,故答案為:蒸餾燒瓶;錐形瓶;
(2)分離四氯化碳和酒精的混合物用蒸餾的方法分離,必須用溫度計測量揮發出的蒸汽的溫度,從而得知蒸汽的成分,此套裝置為蒸餾裝置,
故答案為:溫度計;蒸餾;
(3)①配制溶液所需的Na2CO3的物質的量n=CV=0.2mol/L×0.5L=0.1mol,利用Na2CO3•10H2O的物質的量等于Na2CO3的物質的量,故所需的Na2CO3•10H2O的質量m=nM=0.1mol×286g/mol=28.6g,故答案為:28.6g;
②根據配制一定物質的量濃度的溶液的步驟是稱量、溶解、冷卻、移液、洗滌、定容、搖勻和裝瓶可知所需的儀器有托盤天平、藥匙、量筒、燒杯、玻璃棒、500mL容量瓶和膠頭滴管,故除托盤天平、燒杯、玻璃棒、藥匙、量筒外,還需要500 mL容量瓶和膠頭滴管,故答案為:500 mL容量瓶、膠頭滴管;
③A.Na2CO3•10H2O晶體失去了部分結晶水,則晶體中Na2CO3的質量偏大,則配制出的溶液的濃度偏高,故A正確;
B.用“左碼右物”的稱量方法稱量晶體(使用游碼),則稱量出的固體的質量偏小,濃度偏低,故B錯誤;
C.稱量碳酸鈉晶體時所用砝碼生銹,則砝碼的質量偏大,稱量出的固體的質量偏大,濃度偏高,故C正確;
D.容量瓶未經干燥使用,對溶液濃度無影響,故D錯誤,
故選AC;
④容量瓶只有一條刻度線,只能用容量瓶配制出與其規格相對應的體積的溶液,故配制500mL的溶液應選擇500mL容量瓶;移液時必須要用玻璃棒引流,
故答案為:未采用500 mL容量瓶,未用玻璃棒引流.
點評 本題考查一定物質的量濃度溶液的配制,易錯點是計算溶質的質量,很多同學將溶液的體積認為是480mL而導致出錯.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
 實施以減少能源浪費和降低廢氣排放為基本內容的節能減排政策,是應對全球氣候問題、建設資源節約型、環境友好型社會的必然選擇.化工行業的發展必須符合國家節能減排的總體要求.試運用所學知識,解決下列問題:
實施以減少能源浪費和降低廢氣排放為基本內容的節能減排政策,是應對全球氣候問題、建設資源節約型、環境友好型社會的必然選擇.化工行業的發展必須符合國家節能減排的總體要求.試運用所學知識,解決下列問題: CO(g)+H2(g)△H=+132kJ/mol
CO(g)+H2(g)△H=+132kJ/mol| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某學生按下列操作做一個實驗:在一塊下襯白紙的玻璃片的不同位置分別滴加濃度為0.1mol•L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每種液滴彼此分開,圍成半徑小于表面皿的圓形(如下圖所示),在圓心處放置2粒芝麻粒大小的KMnO4晶體,向KMnO4晶體滴加一滴濃鹽酸,再立即將表面皿蓋好.(已知2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O)
某學生按下列操作做一個實驗:在一塊下襯白紙的玻璃片的不同位置分別滴加濃度為0.1mol•L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每種液滴彼此分開,圍成半徑小于表面皿的圓形(如下圖所示),在圓心處放置2粒芝麻粒大小的KMnO4晶體,向KMnO4晶體滴加一滴濃鹽酸,再立即將表面皿蓋好.(已知2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O)查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3:2:2 | B. | 1:2:3 | C. | 1:3:3 | D. | 3:1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用瓷坩堝熔融氫氧化鈉或碳酸鈉 | |
| B. | 用玻璃棒蘸取溶液,點在濕潤的pH試紙上測定溶液的pH | |
| C. | 讀取量筒內液體的體積,俯視讀數導致讀數偏大 | |
| D. | 用NaOH溶液洗滌并灼燒鉑絲后,再進行焰色反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
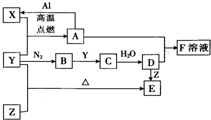 已知X、Y、Z為單質,其它為化合物.其中Y為氣體,F溶液呈黃色,E是常見的溫室氣體,它們之間存在如下的轉化關系(部分產物已經略去).請回答下列問題:
已知X、Y、Z為單質,其它為化合物.其中Y為氣體,F溶液呈黃色,E是常見的溫室氣體,它們之間存在如下的轉化關系(部分產物已經略去).請回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com