
【題目】近年來,隨著聚酯工業的快速發展,氯氣的需求量和氯化氫的產出量也隨之迅速增長。因此,將氯化氫轉化為氯氣的技術成為科學研究的熱點。回答問題:
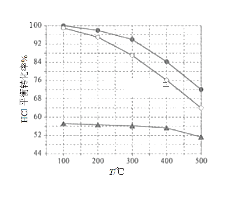
(1)Deacon發明的直接氧化法為:4HCl(g) + O2(g) ![]() 2Cl2(g) +2H2O(g)。如圖為剛性容器中,進料濃度比c(HCl):c(O2)分別等于1:1、4:1、7:1時HCl平衡轉化率隨溫度變化的關系:可知反應平衡常數K(300℃)_________K(400℃)(填“大于”或“小于”)。設HCl初始濃度為c0,根據進料濃度比的數據計算c(HCl):c(O2) = 1:1的數據計算K(400℃)=________________(列出計算式即可)。按化學計量比進料可以保持反應物高轉化率,同時降低產物分離的能耗。進料濃度比c(HCl):c(O2) 過低、過高的不利影響分別___________________________、____________________________。
2Cl2(g) +2H2O(g)。如圖為剛性容器中,進料濃度比c(HCl):c(O2)分別等于1:1、4:1、7:1時HCl平衡轉化率隨溫度變化的關系:可知反應平衡常數K(300℃)_________K(400℃)(填“大于”或“小于”)。設HCl初始濃度為c0,根據進料濃度比的數據計算c(HCl):c(O2) = 1:1的數據計算K(400℃)=________________(列出計算式即可)。按化學計量比進料可以保持反應物高轉化率,同時降低產物分離的能耗。進料濃度比c(HCl):c(O2) 過低、過高的不利影響分別___________________________、____________________________。
(2)在一定溫度的條件下,進一步提高HCl的轉化率的方法是__________________________、___________________________________。(寫出2種)
【答案】大于 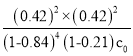 c(HCl):c(O2)過低,說明氧氣過量,則生成的氯氣中會混入氧氣,而不易分離 c(HCl):c(O2)過高,說明氯化氫過量,則氯化氫的轉化率減小 增加反應體系壓強 及時除去產物
c(HCl):c(O2)過低,說明氧氣過量,則生成的氯氣中會混入氧氣,而不易分離 c(HCl):c(O2)過高,說明氯化氫過量,則氯化氫的轉化率減小 增加反應體系壓強 及時除去產物
【解析】
(1)由圖像可知,溫度升高,HCl的平衡轉化率減小,即該反應逆向移動,說明高溫下,K減小,;
(2)4HCl(g) + O2(g) ![]() 2Cl2(g) +2H2O(g)是氣體體積減小的反應,故增加反應體系壓強、及時除去產物可以提高HCl的轉化率。
2Cl2(g) +2H2O(g)是氣體體積減小的反應,故增加反應體系壓強、及時除去產物可以提高HCl的轉化率。
(1)由圖像可知,溫度升高,HCl的平衡轉化率減小,即該反應逆向移動,說明高溫下,K減小,故K(300℃)大于K(400℃);c(O2)相等時,c(HCl)越小,HCl的轉化率越大,400℃時,當c(HCl):c(O2) = 1:1時,HCl的平衡轉化率為84%
4HCl(g) + O2(g) ![]() 2Cl2(g) +2H2O(g)
2Cl2(g) +2H2O(g)
起始 c0 c0 0 0
轉化 0.84 c0 0.21 c0 0.42 c0 0.42 c0
平衡(1-0.84)c0 (1-0.21)c0 0.42 c0 0.42 c0
K(400℃)=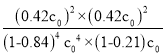 =
=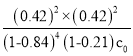 ;c(HCl):c(O2)過低,說明氧氣過量,則生成的氯氣中會混入氧氣,而不易分離;c(HCl):c(O2)過高,說明氯化氫過量,則氯化氫的轉化率減小;
;c(HCl):c(O2)過低,說明氧氣過量,則生成的氯氣中會混入氧氣,而不易分離;c(HCl):c(O2)過高,說明氯化氫過量,則氯化氫的轉化率減小;
(2)4HCl(g) + O2(g) ![]() 2Cl2(g) +2H2O(g)是氣體體積減小的反應,故增加反應體系壓強、及時除去產物可以提高HCl的轉化率。
2Cl2(g) +2H2O(g)是氣體體積減小的反應,故增加反應體系壓強、及時除去產物可以提高HCl的轉化率。


科目:高中化學 來源: 題型:
【題目】氮化鋁( AlN)是一種新型無機非金屬材料,常溫下AlN +NaOH+H2O=NaAlO2+NH3↑。某課題小組利用甲圖所示裝置測定樣品中AlN的含量(雜質不反應)。下列說法中正確的是

A. 量氣管中的液體應為水
B. 用長頸漏斗代替分液漏斗,有利于控制反應速率
C. 反應結束時,a、b兩管液面的差值即為產生氣體的體積
D. 若其它操作均正確,實驗結束時按乙圖讀數,測得AlN含量偏高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式氯化鋁[ Al2(OH)nCl6-n ] 是利用工業鋁灰和活性鋁礬土為原料(主要含Al、Al2O3、SiO2及鐵的氧化物)經過精制加工而成,此產品活性較高,對工業污水具有較好的凈化效果。其制備流程如下:
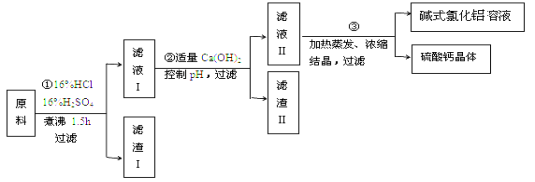
(1)原料需要粉碎,其目的是 ;濾渣I的主要成分是 ;
(2)步驟①在煮沸過程中,溶液逐漸變為淺綠色,檢驗溶液中呈淺綠色的陽離子常采用加入_________溶液進行檢驗(填試劑化學式)。
(3)步驟②中加入適量的Ca(OH)2并控制pH,其目的:一是生成堿式氯化鋁;二是 ;已知堿式氯化鋁的分散質粒子大小在1~100 nm之間,則區別濾液I與堿式氯化鋁兩種液體的物理方法是 ;若Ca(OH)2溶液過量,則步驟③得到的堿式氯化鋁產率偏低,用離子方程式解釋其原因為 ;
(4)某溫度下若0.1 mol AlCl3溶于蒸餾水,當有2.5%水解生成Al(OH)3膠體時,吸收熱量Q kJ ,該水解過程的熱化學反應方程為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列不能用勒夏特列原理解釋的是( )
A.工業合成氨:500℃比室溫更有利
B.SO2催化氧化成SO3的反應,往往加入過量的空氣
C.對于反應2NO2(g) ![]() N2O4(g),增大壓強,體系顏色變淺
N2O4(g),增大壓強,體系顏色變淺
D.實驗室中常用排飽和食鹽水的方法收集氯氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將H2S轉化為可再利用的資源是能源研究領域的重要課題。某轉化工作原理如圖。該裝置工作時,下列敘述錯誤的是( )
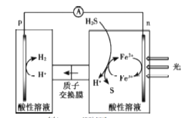
A.p電極的電極反應:2H++2e-=H2
B.該方法能實現由H2S高效產生S和H2
C.光照后,n電極的電極反應:H2S-2e-=2H++S
D.除了Fe3+/Fe2+外,I3-/I-也能實現如圖所示循環
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下兩種金屬硫化物MS、QS的沉淀溶解平衡曲線分別為圖中的I、II (X2+代表 M2+或Q2+),下列有關說法中正確的是
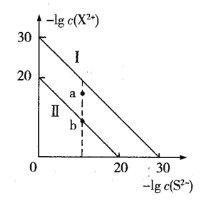
A.MS易與可溶性Q(N03)2的溶液作用轉化為QS
B.與a點對應的由MS形成的分散系很穩定
C.向c(M2+)>c(Q2+)的混合溶液中滴加Na2S溶液,首先析出MS沉淀
D.蒸發a點的QS溶液可得到b點狀態的QS溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金剛石,⑦(NH4)2SO4,⑧乙醇中,由極性鍵形成的非極性分子有_______(填序號,以下同),含有金屬離子的物質是__,分子間可形成氫鍵的物質是________,屬于離子晶體的是__,屬于原子晶體的是__,①~⑤五種物質的熔點由高到低的順序是__。
(2)A,B,C,D為四種晶體,性質如下:
A.固態時能導電,能溶于鹽酸
B.能溶于CS2,不溶于水
C.固態時不導電,液態時能導電,可溶于水
D.固態、液態時均不導電,熔點為3500 ℃
試推斷它們的晶體類型:A.__;B.__;C.__;D.__。
(3)下圖中A~D是中學化學教科書上常見的幾種晶體結構模型,請填寫相應物質的名稱:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 乳酸薄荷醇酯(![]() )僅能發生水解、氧化、消去反應
)僅能發生水解、氧化、消去反應
B. 乙醛和丙烯醛(![]() )不是同系物,它們與氫氣充分反應后的產物也不是同系物
)不是同系物,它們與氫氣充分反應后的產物也不是同系物
C. 淀粉和纖維素在酸催化下完全水解后的產物都是葡萄糖
D. CH3COOCH2CH3與CH3CH2COOCH3互為同分異構體,1H-NMR譜顯示兩者均有三種不同的氫原子且三種氫原子的比例相同,故不能用1H-NMR來鑒別
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是
A.標準狀況下,2.24L四氯化碳中含有共價鍵總數為0.4NA
B.46g NO2和N2O4的混合氣體中,含有的氮原子數為1NA
C.1L1.0mol/L的鹽酸中含有HCl分子數為NA
D.一定條件下,將2molSO2與1molO2充分反應,得到SO3的分子數為2NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com