
諾氟沙星別名氟哌酸,是治療腸炎痢疾的常用藥。其結構簡式如右圖,下列說法正確的是
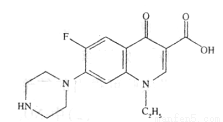
A. 該化合物屬于苯的同系物
B. 分子式為Cl6 H16 FN3O3
C. 1mol該化合物中含有6NA個雙鍵
D. 該化合物能與酸性高錳酸鉀、溴水、碳酸氫鈉溶液反應
科目:高中化學 來源:2016-2017學年山西省大同市高一3月月考化學試卷(解析版) 題型:選擇題
下列說法中不正確的是( )
①質子數相同的粒子一定屬于同種元素;
②同位素的性質幾乎完全相同;
③質子數相同,電子數也相同的兩種粒子,不可能是一種分子和一種離子;
④電子數相同的粒子不一定是同一種元素;
⑤一種元素只能有一種質量數;
⑥某種元素的相對原子質量取整數,就是其質量數
⑦元素周期表中從ⅢB族到ⅡB族10個縱行的元素都是金屬元素
⑧核外電子排布相同的微粒化學性質不一定相同
⑨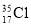 與
與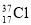 得電子能力相同
得電子能力相同
A. ①②④⑤ B. ③④⑤⑥ C. ②③⑤⑥ D. ①②⑤⑥
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省太原市高一3月階段性測試化學試卷(解析版) 題型:選擇題
化學試劑不變質和實驗方法科學是化學實驗成功的保障。下列試劑保存方法或實驗方法中,不正確的是( )
A. 實驗室中金屬鈉通常保存在煤油里
B. 液溴易揮發,在存放液溴的試劑瓶中應加水封
C. 保存FeCl3溶液時,通常在溶液中加少量的單質鐵
D. 濃硝酸通常保存在棕色試劑瓶中,置于陰涼處
查看答案和解析>>
科目:高中化學 來源:2017屆新疆烏魯木齊地區高三第二次診斷性測驗化學試卷(解析版) 題型:簡答題
氫氣是一種清潔能源,氫氣的制取與儲存是氫能源利用領域的熱點。
(1) NaBH4是一神重要的儲氫載體,能與水反應生成NaBO2,且反應前后B的化合價不變,該反應的化學方程式為_________,反應消耗1molNaBH4時轉移的電子數目為___________。
(2) H2S熱分解可制氫氣。反應方程式:2H2S(g)=2H2(g)+S2(g) △H;在恒容密閉容器中,測得H2S分解的轉化率(H2S起始濃度均為c mol/L)如圖1所示。圖l中曲線a表示H2S的平衡轉化率與溫度的關系,曲線b表示不同溫度下反應經過相同時間且未達到化學平衡時H2S的轉化率。
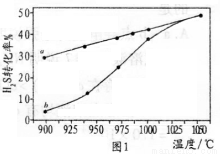
①△H ______0(填“>”“<”或“=”);
②若985℃時,反應經t min達到平衡,此時H2S的轉化率為40%,則t min內反應速率v(H2)=_____(用含c、t的代數式表示);
③請說明隨溫度升高,曲線b向曲線a接近的原因____________。
(3) 使用石油裂解的副產物CH4可制取H2,某溫度下,向體積為2L的密閉容器中充入0.40mol CH4(g)和0.60molH2O(g)的濃度隨時間的變化如下表所示:

①寫出此反應的化學方程式_________,此溫度下該反應的平衡常數是_________。
②3 min時改變的反應條件是_________(只填一種條件的改變)。
③一定條件下CH4的平衡轉化率與溫度、壓強的關系如圖2所示。則P1_________P2填“>”、“<”或“=“)。
查看答案和解析>>
科目:高中化學 來源:2017屆新疆烏魯木齊地區高三第二次診斷性測驗化學試卷(解析版) 題型:選擇題
常溫下,下列各組離子在指定溶液中一定能大量共存的是( )
A. Na2S溶液中:SO42-、K+、Cl-、Cu2+
B.  的溶液:K+、AlO2-、CO32-、Na+
的溶液:K+、AlO2-、CO32-、Na+
C. 飽和氯水中:Cl-、NO3-、Na+、SO32-
D. 碳酸氫鈉溶液:K+、SO42-、Cl-、H+
查看答案和解析>>
科目:高中化學 來源:南開中學2016-2017高三第四次月考理綜化學試卷 題型:填空題
平板電視顯示屏生產過程中產生大量的廢玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物質)。某課題以此粉末為原料,設計如下工藝流程對資源進行回收,得到Ce(OH)4和硫酸鐵銨:
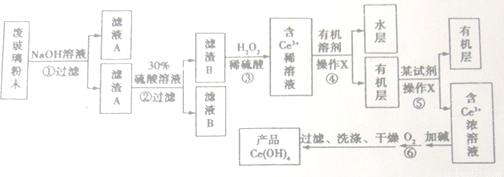
己知:
I.酸性條件下,鈰在水溶液中有Ce3+、Ce4+兩種主要存在形式;
II. CeO2不溶于稀硫酸;利用有機溶劑可分離稀土元素如Ce等化合物。
請按要求回答下列問題:
(1) Ce的原子序數為58,它位于元素周期表中第______周期。
(2)步驟①、⑥反應的化學方程式分別為_________________、______________。
(3)檢驗濾渣B洗滌干凈的方法是____________________。
(4)步驟③的離子方程式為____________________。
(5)操作X名稱為_________________。
(6)在濾液B中加過量鐵粉于50 °C水浴中加熱充分反應后趁熱過濾,濾液移至試管中,用橡膠塞塞緊試管口,靜置、冷卻一段時間后收集得產品綠礬。
步驟②中的硫酸溶液過稀會導致____________;靜置冷卻一段時間后,在試管中觀察到的現象是______________________。
(7)取2.08 g產品Ce(OH)4加過量稀硫酸溶解后,用0.1000 mol/L FeSO4溶液滴定至終點共消耗90.00mL,則產品中Ce(OH)4的質量分數為______________。
查看答案和解析>>
科目:高中化學 來源:南開中學2016-2017高三第四次月考理綜化學試卷 題型:選擇題
下列離子方程式書寫正確的是
A.向CaCl2溶液中通入少量CO2氣體:Ca2++CO2+H2O=CaCO3↓+2H+
B.碳酸鈉溶液與硫酸氫鈉溶液反應:CO32-+H+=CO2↑+H2O
C.Ba(OH)2溶液中滴加NH4HSO4溶液至剛好沉淀完全:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.向FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
查看答案和解析>>
科目:高中化學 來源:2016-2017學年廣西省桂林市高一下學期開學考試化學試卷(解析版) 題型:選擇題
下列溶液中通入CO2沒有沉淀產生的是
A. NaAlO2溶液 B. Na2SiO3溶液 C. BaCl2溶液 D. 飽和Na2CO3溶液
查看答案和解析>>
科目:高中化學 來源:2017屆河北省石家莊市高三下學期模擬聯考理科綜合化學試卷(解析版) 題型:選擇題
堿性硼化釩(VB2)—空氣電池工作時反應為:4VB2+11O2=4B2O3+2V2O5,用該電池電解100mL 硫酸銅溶液,實驗裝置如圖所示(b、c均為惰性電極),當外電路中通過0.02mol電子時,B裝置兩極共收集到0.224L氣體(標準狀況)。下列說法正確的是( )
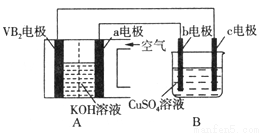
A. 電解過程中,b電極表面先有紅色物質析出,然后有氣泡產生
B. VB2為負極,電極反應為:2VB2+11H2O-22e-=V2O5+2B2O3+22H+
C. 電池內部OH-移向a電極,溶液pH保持增大
D. 忽略溶液體積變化,電解后B裝置中溶液的pH為1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com