
I.已知:反應




請回答:
 反應生成氣態水的熱化學方程式__________________________
反應生成氣態水的熱化學方程式__________________________
II.實施以減少能源浪費和降低廢氣排放為基本內容的節能減排政策,是應對全球氣候問題、建設資源節約型、環境友好型社會的必然選擇。化工業的發展必須符合國家節能減排的總體要求。試運用所學知識,解決下列問題:
(1)已知某反應的平衡表達式為:
它所對應的化學方程式為:_________________________________________________
(2)已知在400℃時,反應

 =0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應
=0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應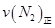 ____________
____________ (填:>、<、=、不能確定);
(填:>、<、=、不能確定);
欲使得該反應的化學反應速率加快,同時使平衡時NH3的體積分數增加,
可采取的正確措施是____________(填序號)
A.加催化劑 B.升高溫度 C.縮小體積增大壓強 D.使氨氣液化移走
(3)在一定體積的密閉容器中,進行如下化學反應:

 ,其化學平衡常數K與溫度T的關系如下表:
,其化學平衡常數K與溫度T的關系如下表:

請完成下列問題:
①判斷該反應的 ___________0(填“>”或“<”)
___________0(填“>”或“<”)
②在一定條件下,能判斷該反應一定達化學平衡狀態的是___________(填序號)。
A. B.容器內壓強保持不變
B.容器內壓強保持不變
C.A和B的轉化率相等 D.混合氣體的密度保持不變
I 2H2(g)+ O2 (g)= 2H2O(g) △H= -483.6 kJ/mol
II(1)C(s)+H2O(g) H2(g)+
CO(g)(2)=;C(3)①
> ② BD
H2(g)+
CO(g)(2)=;C(3)①
> ② BD
【解析】
試題分析:I 根據題意△H=△1H +△2H,故2H2(g)+
O2 (g)= 2H2O(g) △H= -483.6 kJ/mol;(2)一段時間后,當N2、H2、NH3的物質的量分別為2mol/L、1mol/L、2mol/L時,Qc=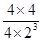 =0.5,所以該狀態是平衡狀態,正逆反應速率相等,故答案為
= 。A、使用催化劑,平衡不移動,NH3的體積分數不變,故A錯誤;B、升高溫度,平衡向吸熱的方向移動,即逆反應方向移動,NH3的體積分數減少,故B錯誤;C、增大壓強,平衡向氣體體積減少的方向移動,即正向移動,NH3的體積分數增大,故C正確;D、及時分離出NH3,平衡正向移動,NH3的體積分數降低,故D錯誤;(3)①由表中數據可知,溫度越高化學平衡常數越大,升高溫度平衡向正反應移動,正反應是吸熱反應,△H>0;②A、速率之比等于系數之比,3v正(B)=2v逆(C)不符合速率之比等于系數之比,故A不符合;B、容器內壓強保持不變,反應前后氣體體積減小,壓強不變,說明平衡不變,故B符合;C、A和B的轉化率的比等于系數比是平衡不變,故C錯誤;D、在一定體積的密閉容器中,當達到平衡狀態時,反應的壓強不變,則混合氣體的密度保持不變,故D正確。
=0.5,所以該狀態是平衡狀態,正逆反應速率相等,故答案為
= 。A、使用催化劑,平衡不移動,NH3的體積分數不變,故A錯誤;B、升高溫度,平衡向吸熱的方向移動,即逆反應方向移動,NH3的體積分數減少,故B錯誤;C、增大壓強,平衡向氣體體積減少的方向移動,即正向移動,NH3的體積分數增大,故C正確;D、及時分離出NH3,平衡正向移動,NH3的體積分數降低,故D錯誤;(3)①由表中數據可知,溫度越高化學平衡常數越大,升高溫度平衡向正反應移動,正反應是吸熱反應,△H>0;②A、速率之比等于系數之比,3v正(B)=2v逆(C)不符合速率之比等于系數之比,故A不符合;B、容器內壓強保持不變,反應前后氣體體積減小,壓強不變,說明平衡不變,故B符合;C、A和B的轉化率的比等于系數比是平衡不變,故C錯誤;D、在一定體積的密閉容器中,當達到平衡狀態時,反應的壓強不變,則混合氣體的密度保持不變,故D正確。
考點:蓋斯定理的計算;工業合成氨,化學平衡的調控作用;化學平衡狀態的判斷


科目:高中化學 來源: 題型:閱讀理解
| C(H2)?C(CO) |
| C(H2O) |
| 高溫 |
| 高溫 |
| 高溫 |
查看答案和解析>>
科目:高中化學 來源:2013-2014學年湖北省高三上學期12月月考化學試卷(解析版) 題型:填空題
I.已知:反應①H2(g) + Cl2(g) = 2HCl(g) ΔH= —184 kJ/mol
②4HCl(g)+O2(g)
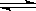 2Cl2(g)+2H2O(g)
ΔH= —115.6 kJ/mol
2Cl2(g)+2H2O(g)
ΔH= —115.6 kJ/mol


請回答:
(1)H2與O2反應生成氣態水的熱化學方程式
(2)斷開1 mol H—O 鍵所需能量約為 kJ。
II.實施以減少能源浪費和降低廢氣排放為基本內容的節能減排政策,是應對全球氣候問題、建設資源節約型、環境友好型社會的必然選擇。化工行業的發展必須符合國家節能減排的總體要求。試運用所學知識,解決下列問題:
(1)已知某反應的平衡表達式為:  ,它所對應的化學方程式為:
。
,它所對應的化學方程式為:
。
(2)已知在400℃時,N2 (g)+ 3H2(g) 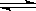 2NH3(g)
△H<0 的K=0.5, 則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應V(N2)正 V(N2)逆(填:>、<、=、不能確定)。欲使得該反應的化學反應速率加快,同時使平衡時NH3的體積百分數增加,可采取的正確措施是 (填序號)
2NH3(g)
△H<0 的K=0.5, 則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應V(N2)正 V(N2)逆(填:>、<、=、不能確定)。欲使得該反應的化學反應速率加快,同時使平衡時NH3的體積百分數增加,可采取的正確措施是 (填序號)
A.縮小體積增大壓強 B.升高溫度 C.加催化劑 D.使氨氣液化移走
(3)在一定體積的密閉容器中,進行如下化學反應:A(g) + 3B(g) 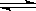 2C(g) + D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:
2C(g) + D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:
|
t/K |
300 |
400 |
500 |
… |
|
K/(mol·L-1)2 |
4×106 |
8×107 |
K1 |
… |
請完成下列問題:
①判斷該反應的ΔH 0(填“>”或“<”)
②在一定條件下,能判斷該反應一定達化學平衡狀態的是 (填序號)。
A.3v(B)(正)=2v(C)(逆) B.A和B的轉化率相等
C.容器內壓強保持不變 D.混合氣體的密度保持不變
查看答案和解析>>
科目:高中化學 來源:2013-2014學年江西省高三12月月考理綜考化學試卷(解析版) 題型:填空題
I.已知:反應H2(g) + Cl2(g) = 2HCl(g) ΔH= —184 kJ/mol
4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)
ΔH= —115.6 kJ/mol
2Cl2(g)+2H2O(g)
ΔH= —115.6 kJ/mol


請回答:
(1)H2與O2反應生成氣態水的熱化學方程式
(2)斷開1 mol H—O 鍵所需能量約為 kJ
II.試運用所學知識,解決下列問題:
(1)已知某反應的平衡表達式為: ,它所對應的化學方程式為:
,它所對應的化學方程式為:
(2)已知在400℃時,N2 (g)+ 3H2(g)
 2NH3(g)
△H<0 的K=0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應v(N2)正 v(N2)逆(填:>、<、=、不能確定)(1分)
2NH3(g)
△H<0 的K=0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應v(N2)正 v(N2)逆(填:>、<、=、不能確定)(1分)
欲使得該反應的化學反應速率加快,同時使平衡時NH3的體積百分數增加,可采取的正確措施是 (填序號)(1分)
A.縮小體積增大壓強 B.升高溫度 C.加催化劑 D.使氨氣液化移走
(3)在一定體積的密閉容器中,進行如下化學反應:A(g) + 3B(g)  2C(g)
+ D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:
2C(g)
+ D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:
|
t/K |
300 |
400 |
500 |
… |
|
K/(mol·L—1)2 |
4×106 |
8×107 |
K1 |
… |
請完成下列問題:
①判斷該反應的ΔH 0(填“>”或“<”) (1分)
②在一定條件下,能判斷該反應一定達化學平衡狀態的是 (填序號)
A.3v(B)(正)=2v(C)(逆) B.A和B的轉化率相等
C.容器內壓強保持不變 D.混合氣體的密度保持不變
(4)以天然氣(假設雜質不參與反應)為原料的燃料電池示意圖如圖所示。

①放電時,負極的電極反應式為
②假設裝置中盛裝100.0 mL 3.0 mol·L—1 KOH溶液,放電時參與反應的氧氣在標準狀況下體積為8 960 mL。放電完畢后,電解質溶液中各離子濃度的大小關系為
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
I.已知:反應 H2(g) + Cl2(g) = 2HCl(g) ΔH= —184 kJ/mol
4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g) ΔH= —115.6 kJ/mol
2Cl2(g)+2H2O(g) ΔH= —115.6 kJ/mol
![]()

請回答:
(1)H2與O2反應生成氣態水的熱化學方程式
(2)斷開1 mol H—O 鍵所需能量約為 kJ。
II.實施以減少能源浪費和降低廢氣排放為基本內容的節能減排政策,是應對全球氣候問題、建設資源節約型、環境友好型社會的必然選擇。化工行業的發展必須符合國家節能減排的總體要求。試運用所學知識,解決下列問題:
(1)已知某反應的平衡表達式為: ![]() ,
,
它所對應的化學方程式為: .
(2)已知在400℃時,N2 (g)+ 3H2(g) ![]() 2NH3(g) △H<0 的K=0.5, 則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應V(N2)正 V(N2)逆(填:>、<、=、不能確定)。
2NH3(g) △H<0 的K=0.5, 則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應V(N2)正 V(N2)逆(填:>、<、=、不能確定)。
欲使得該反應的化學反應速率加快,同時使平衡時NH3的體積百分數增加,可采取的正確措施是 (填序號)
A.縮小體積增大壓強 B.升高溫度 C.加催化劑 D.使氨氣液化移走
(3)在一定體積的密閉容器中,進行如下化學反應:A(g) + 3B(g) ![]() 2C(g) + D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:
2C(g) + D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:
| t/K | 300 | 400 | 500 | … |
| K/(mol·L-1)2 | 4×106 | 8×107 | K1 | … |
請完成下列問題:
①判斷該反應的ΔH 0(填“>”或“<”)
②在一定條件下,能判斷該反應一定達化學平衡狀態的是 (填序號)。
A.3v(B)(正)=2v(C)(逆) B.A和B的轉化率相等
C.容器內壓強保持不變 D.混合氣體的密度保持不變
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com