
【題目】三氯硅烷(SiHCl3)在空氣中極易燃燒,易與水反應生成兩種酸,主要用于生產多晶硅、硅油等,熔點為134 ℃、沸點為31.8 ℃。已知氯化氫氣體在加熱條件下可與單質硅反應得到三氯硅烷,某同學利用如圖裝置制備一定量的三氯硅烷(加熱裝置均省略)。

(1)制備HCl氣體的方法之一是將濃硫酸與濃鹽酸混合,下列性質與制備原理無關的是______(填字母),B裝置的作用是___________________,冰鹽水的作用是________________________。
A.濃硫酸具有脫水性 B.濃硫酸具有吸水性
C.鹽酸具有揮發性 D.氣體的溶解度隨溫度升高而降低
(2)實驗開始后,首先要通入一段時間的HCl氣體后才能對C處試劑加熱,目的是:①排出裝置中空氣,防止硅與氧氣反應,②_____________________。該套實驗裝置有兩處明顯的錯誤:①E中會產生倒吸,②____________________。E裝置的用途是_______________________。
(3)加熱條件下,C中發生的是置換反應,相應的化學方程式為________________________。
(4)制得的SiHCl3中含有少量SiCl4(沸點為57.6 ℃),提純SiHCl3采用的適宜方法為__________,收集SiHCl3時溫度應控制在_____________。
(5)設計一個實驗證明C中產生的氣體是H2:_______________________________。
【答案】(1)A 除去HCl氣體中的水蒸氣 冷卻生成的SiHCl3,使其液化,以便收集
(2)防止生成的SiHCl3與氧氣反應 D、E之間缺少一個盛有濃硫酸的干燥裝置 吸收HCl氣體,防止其污染空氣
(3)Si+3HCl![]() SiHCl3+H2
SiHCl3+H2
(4)蒸餾 31.8 ℃
(5)點燃E裝置出口處的氣體,氣體能燃燒產生淡藍色火焰,將冷而干燥的燒杯罩在火焰上方,燒杯壁上有水珠
【解析】(1)濃硫酸與濃鹽酸混合制取HCl氣體,利用了濃硫酸的吸水性、鹽酸的揮發性以及氣體的溶解度隨溫度升高(濃硫酸吸水放熱)而降低的性質,與濃硫酸的脫水性無關,故選A。B裝置裝有干燥劑,用于除去HCl氣體中的水蒸氣。冰鹽水的作用是冷卻生成的SiHCl3,使其液化,以便收集起來。
(2)由題給信息知SiHCl3在空氣中極易燃燒,還易與水反應,先通入一段時間HCl氣體,排出空氣的目的之二是防止生成的SiHCl3與氧氣反應;整套裝置缺陷之二是D、E之間缺少一個干燥裝置,否則E中水蒸氣逆流進入試管中與SiHCl3反應;HCl氣體在C裝置中無法反應完,故E是用于吸收HCl氣體,防止其污染空氣。
(3)置換反應生成的單質是H2。
(4)SiHCl3和SiCl4沸點差異較大,故適宜的分離方法是蒸餾,收集31.8 ℃時的餾分即得到SiHCl3。
(5)可在E裝置出口處點燃氣體,氣體燃燒時產生淡藍色火焰,將冷而干燥的燒杯罩在火焰上方,燒杯壁上有水珠,說明有氫氣生成。


科目:高中化學 來源: 題型:
【題目】下列有關元素周期表中“周期”的說法錯誤的是
A. 元素周期表中有四個長周期、三個短周期
B. 同一周期主族元素原子的核外電子層數相同
C. 同一周期主族元素原子的價電子數目不同
D. 元素周期表中每個周期均從金屬元素開始,以非金屬元素結束
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯氣是一種重要的工業原料。
Ⅰ.實驗室可用二氧化錳和濃鹽酸反應制取氯氣,反應的化學方程式是________。
Ⅱ.某研究性學習小組查閱資料得知,漂白粉與硫酸反應可制取氯氣,化學方程式為:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O他們利用該反應設計如下制取氯氣并驗證其性質的實驗。
2CaSO4+2Cl2↑+2H2O他們利用該反應設計如下制取氯氣并驗證其性質的實驗。

回答下列問題:(1)該實驗中A部分的裝置是_______(填標號)。
(2)請你幫助他們設計一個實驗,證明洗氣瓶C中的Na2SO3已被氧化(簡述實驗步驟):_____________________________。
(3)寫出D裝置中發生反應的離子方程式_________________
(4)該實驗存在明顯的缺陷,請你提出改進的方法__________________________________________寫出反應離子方程式_____________________________________。
(5)該小組又進行了如下實驗:稱取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取出25 mL加入到錐形瓶中,再加入過量的KI溶液和過量的H2SO4溶液,靜置。待完全反應后,用0.1 mol.L1的Na2S2O3溶液作標準液滴定反應生成的碘,已知反應方程式為:2Na2S2O3+I2===Na2S4O6+2NaI,共用去Na2S2O3溶液20.0 mL。則該漂白粉中Ca(ClO)2的質量分數為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在任何條件下,純水顯中性,這是因為 ( )
A、PH=7 B、c(H+)=c(OH-)
C、c(H+)=c(OH-)=10-7mol/L D、c(H+)×c(OH-)=10-14
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】蔗糖與濃硫酸的炭化實驗會產生大量的有刺激性氣味的氣體,對環境產生污染。為此,某化學興趣小組設計了如下裝置進行實驗。玻璃管中①②③分別為CO檢測試紙(浸有氯化鈀溶液的濾紙,遇CO變黑色)、滴有品紅溶液的濾紙、滴有酸性KMnO4溶液的濾紙,a和b分別為兩個小氣球。
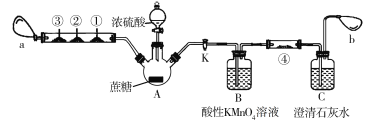
實驗步驟如下:按圖示連接好儀器,然后檢查裝置的氣密性;裝好試劑,夾緊止水夾K,向A瓶中的蔗糖上小心滴加濃硫酸,片刻后可觀察到A瓶內蔗糖變黑,體積膨脹,有白霧產生,氣球a鼓起,玻璃管中①號濾紙由白色變黑色,②號和③號濾紙均褪色。請回答以下問題:
(1)上圖中盛裝濃硫酸的儀器名稱為________。待上述反應結束后,點燃酒精燈并在②號和③號濾紙的玻璃管附近均勻加熱,觀察到的現象是____________________。
(2)B瓶中酸性KMnO4溶液的作用是___________________________,發生反應的離子方程式為________________________________。
(3)打開止水夾K,使氣球a內氣體緩慢通過B瓶和C瓶,一段時間之后,發現澄清石灰水變渾濁,但此現象并不能證明該反應生成了CO2。為了證明有CO2生成并簡化實驗裝置,可在④號位置放上滴有__________的濾紙(從以下試劑中選擇)。
A.品紅溶液 B.酸性高錳酸鉀溶液 C.溴水 D.澄清石灰水
(4)若反應生成的兩種碳的氧化物在相同條件下的體積比為2∶1,則蔗糖炭化后體積膨脹發生反應的化學方程式可能為_______________________________。(若是氧化還原反應,請用單線橋法在化學方程式上標明電子轉移的方向和數目。)
(5)若在尾端沒有氣球b,會有什么不良結果?______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[2017新課標Ⅱ]水中的溶解氧是水生生物生存不可缺少的條件。某課外小組采用碘量法測定學校周邊河水中的溶解氧。實驗步驟及測定原理如下:
Ⅰ.取樣、氧的固定
用溶解氧瓶采集水樣。記錄大氣壓及水體溫度。將水樣與Mn(OH)2堿性懸濁液(含有KI)混合,反應生成MnO(OH)2,實現氧的固定。
Ⅱ.酸化、滴定
將固氧后的水樣酸化,MnO(OH)2被I還原為Mn2+,在暗處靜置5 min,然后用標準Na2S2O3溶液滴定生成的I2(2![]() +I2=2I+
+I2=2I+![]() )。
)。
回答下列問題:
(1)取水樣時應盡量避免擾動水體表面,這樣操作的主要目的是_____________。
(2)“氧的固定”中發生反應的化學方程式為_______________。
(3)Na2S2O3溶液不穩定,使用前需標定。配制該溶液時需要的玻璃儀器有燒杯、玻璃棒、試劑瓶和____________;蒸餾水必須經過煮沸、冷卻后才能使用,其目的是殺菌、除____及二氧化碳。
(4)取100.00 mL水樣經固氧、酸化后,用a mol·L1Na2S2O3溶液滴定,以淀粉溶液作指示劑,終點現象為________________;若消耗Na2S2O3溶液的體積為b mL,則水樣中溶解氧的含量為_________mg·L1。
(5)上述滴定完成時,若滴定管尖嘴處留有氣泡會導致測量結果偏___________。(填“高”或“低”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,質量為95 g的氯化鎂溶解在0.2 L水中(水的密度近似為1 g/mL)恰好得到氯化鎂的飽和溶液,所得溶液的密度為ρ g/mL,物質的量濃度為c mol/L,溶解度為s,NA表示阿伏加德羅常數的值,則下列敘述中正確的是( )
A. 所得溶液中含有NA個氯化鎂分子
B. 所得溶液的物質的量濃度為5 mol/L
C. 所得溶液的溶解度可表示為9500 c/(1000ρ-95c)
D. 所得溶液的質量分數可表示為95 ρ/(1000c)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【衡水中學2017屆第二次模擬】航天員呼吸產生的CO2用下列反應處理,可實現空間站中O2的循環利用。
sabatior反應:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
水電解反應:2H2O(l)![]() 2H2(g) + O2(g)
2H2(g) + O2(g)
(1)將原料氣按nCO2∶nH2=1:4置于密閉容器中發生Sabatier反應,測得H2O(g)的物質的量分數與溫度的關系如圖所示(虛線表示平衡曲線)。
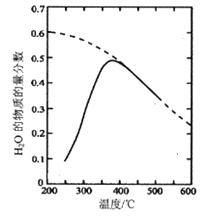
①己知H2(g)、CH4(g)的燃燒熱分別為A kJ/mol、BkJ/mol, H2O(l)=H2O(g) △H =C kJ/mol。計算Sabatier反應的△H=___kJ/mol。
②溫度過高或過低均不利于該反應的進行,原因是________。
③200℃達到平衡時體系的總壓強為p,該反應平衡常數Kp的計算式為________。(不必化簡。用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)
(2)Sabatier反應在空間站運行時,下列措施能提高CO2轉化效率的是______(填標號)。
A.適當減壓 B.增大催化劑的比表面積
C.反應器前段加熱,后段冷卻 D.提高原料氣中CO2所占比例
E.合理控制反應器中氣體的流速
(3) 一種新的循環利用方案是用Bosch反應CO2(g)+2H2(g)![]() C(s)+2H2O(g)代替Sabatier反應。
C(s)+2H2O(g)代替Sabatier反應。
在250℃,向體積為2L且帶氣壓計的恒容密閉容器中通入0.08molH2和0.04molCO2發生Bosch 反應CO2(g)+2H2(g)![]() C(s)+2H2O(g) △ H
C(s)+2H2O(g) △ H
①若反應起始和平衡時溫度相同(均為250℃),測得反應過程中壓強(P)隨時間(t)的變化如圖I 曲線a所示,則△H___ 0(填“>”“<”或“不確定”) ;若其它條件相同,僅改變某一條件時,測得其壓強(P)隨時間(t)的變化如圖I 曲線b所示,則改變的條件是______________。
②圖II是甲、乙兩同學描繪上述反應平衡常數的對數值(lgK)與溫度的變化關系,其中正確的曲線是____________(填“甲”或“乙”):m值為____________。

③Bosch反應必須在高溫下才能啟動,原因是__________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com