

 Ba+CO2↑,各元素化合價未發生變化,屬于分解反應;反應⑥為2BaO+O2
Ba+CO2↑,各元素化合價未發生變化,屬于分解反應;反應⑥為2BaO+O2 2BaO2,氧元素化合價發生變化,屬于氧化還原反應;反應⑦BaO2+H2SO4=BaSO4↓+H2O2,各元素化合價未發生變化,屬于復分解反應.所以7個反應中①②⑥屬于氧化還原反應.
2BaO2,氧元素化合價發生變化,屬于氧化還原反應;反應⑦BaO2+H2SO4=BaSO4↓+H2O2,各元素化合價未發生變化,屬于復分解反應.所以7個反應中①②⑥屬于氧化還原反應. .
.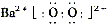 .
. BaS+4CO↑.反應③:BaS+ZnSO4=ZnS↓+BaSO4↓.
BaS+4CO↑.反應③:BaS+ZnSO4=ZnS↓+BaSO4↓. BaS+4CO↑.反應③:BaS+ZnSO4=ZnS↓+BaSO4↓.
BaS+4CO↑.反應③:BaS+ZnSO4=ZnS↓+BaSO4↓.

 小學奪冠AB卷系列答案
小學奪冠AB卷系列答案科目:高中化學 來源: 題型:
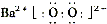
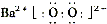
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
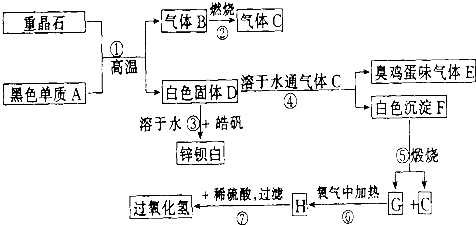
例硫酸鋇是惟一無毒的鋇鹽,工業上以BaSO4等為原料通入圖所示流程反應可以制備鋅鋇白和過氧化氫:
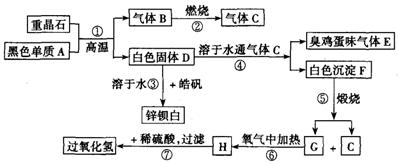
(1)上述流程中共有7個化學反應,其中有__________個屬于氧化還原反應。
(2)寫出過氧化氫的電子式:__________;寫出物質H的電子式:__________。
(3)寫出下列化學反應方程式:
反應①:____________________;
反應③:____________________;
反應④:____________________;
反應⑦:____________________。
查看答案和解析>>
科目:高中化學 來源:天津一模 題型:問答題
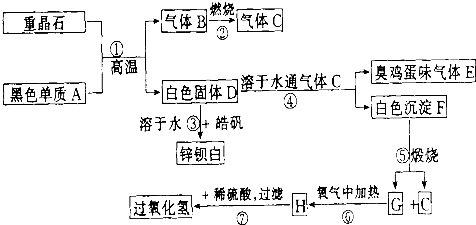
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com