
| m |
| n |
| 44g/mol×2mol |
| 1mol |


 新思維假期作業寒假吉林大學出版社系列答案
新思維假期作業寒假吉林大學出版社系列答案科目:高中化學 來源: 題型:
| 化學鍵 | C≡O (CO) | C=O | H-O | H-H |
| 鍵能(kJ?mol-1) | 1070 | 801 | 463 | 436 |
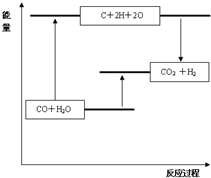 B.
B.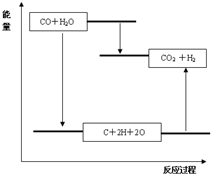
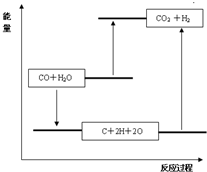 D.
D.
| 1 |
| 6 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
A、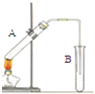 A中為乙醇、醋酸,B中為飽和碳酸鈉溶液,制取乙酸乙酯 |
B、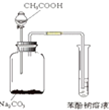 驗證醋酸、碳酸、苯酚的酸性強弱 |
C、 用濃硫酸、乙醇共熱到約170℃制乙烯 |
D、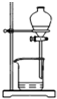 用NaOH溶液除去苯中混有的少量苯酚 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 放電 |
| 通電 |
| A、充電時,外接電源的正極與電池上標注“-”的電極連接 |
| B、電池工作時,H+由正極流向負極 |
| C、電池放電時,負極的電極反應為VO2++H2O=VO2++2H++e- |
| D、電池充電時,陰極的電極反應為V3++e-=V2+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com