
分析 (1)制取硝酸過程中主要發生反應有:①氨氣的催化氧化,反應方程式為:4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O; ②一氧化氮與氧氣、水生成硝酸,反應方程式為:4NO+3O2+2H2O=4HNO3;
(2)計算氨氣的濃度變化,進而計算生成氨氣的質量,再根據n=$\frac{m}{M}$計算得到氨氣的物質的量;
(3)由氮元素守恒可得關系式NH3~HNO3,據此計算.
解答 解:(1)制取硝酸過程中主要發生反應有:①氨氣的催化氧化,反應方程式為:4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O,故答案為:4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O;
(2)氨氣的濃度變化為168mg/L-15mg/L=153mg/L=0.153g/L,
m(NH3)=0.1536g/L×800m3×103L/m3=122400g,
n(NH3)=$\frac{122400g}{17g/mol}$=7200mol,
故答案為:7200mol;
(3)令生成硝酸的質量為x t,則:
NH3~~~~~HNO3,
17 63
1.224t×90% x t
所以,$\frac{17}{63}=\frac{1.224t×90%}{xt}$,解得x=0.41,
答:該廠每天可生產硝酸0.41t.
點評 本題考查溶液濃度計算、根據方程式計算的計算,難度中等,(3)注意利用關系式計算,簡化計算過程.


科目:高中化學 來源: 題型:選擇題
| A. | 在Na2SO4溶液中,c(Na+):c(SO42-) | |
| B. | 相同溫度下,0.2 mol/L CH3COOH溶液中c(H+)與0.1 mol/LCH3COOH溶液中c(H+) | |
| C. | 在密閉容器中,反應N2(g)+3H2(g)?2NH3 (g)已達平衡時的c(NH3)與c(N2) | |
| D. | 液面均在“0”刻度時,50mL堿式滴定管和25mL堿式滴定管所盛溶液體積 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
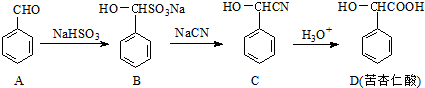
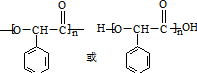
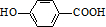 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ⑤④①③② | B. | ⑤③④②① | C. | ②④③①⑤ | D. | ③②④⑤① |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.5mol?L-1K2SO4含有的K+數目為NA | |
| B. | 56g鐵與足量的鹽酸反應時失去電子的數目為3NA | |
| C. | 在標準狀況下,22.4LCCl4中含有的分子數目為NA | |
| D. | 在常溫常壓下,16gO2和O3的混合氣體所含原子數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 元素Y的最高正化合價為+6 | |
| B. | 簡單離子半徑的大小順序為W>Q>Z>X>Y | |
| C. | 氣態氫化物的穩定性:Q>W | |
| D. | 元素W的最高價氧化物對應的水化物酸性比Q的強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
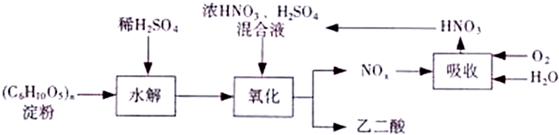
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 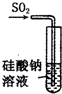 裝置:可證明H2SiO3酸性與H2SO3酸性強 | |
| B. |  裝置:橡膠管的作用是能使水順利流下 | |
| C. | 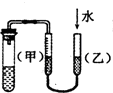 裝置:用圖示的方法能檢查此裝置的氣密性 | |
| D. | 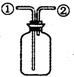 裝置:可在瓶中先裝入某種液體收集NO氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 物質 | 除雜試劑 | 分離方法 |
| A | NaCl溶液(CuCl2) | 鈉 | 結晶 |
| B | S02(SO3) | NaOH溶液 | 萃取 |
| C | Cu(NO3)2溶液(AgNO3) | 銅粉 | 分液 |
| D | 乙醇(水) | … | 蒸餾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com