
【題目】A、B、C、D 均為短周期元素組成的物質,它們之間符合如下轉化關系:
![]()
(1)若A 為可使濕潤的紅色石蕊試紙變藍的氣態氫化物,X 為水,D 為重要的化工原料。
① A 的電子式為_________________,A→B 的化學方程式為______________________。
②A 和 D 發生化合反應得到的化合物 E 的化學式是___________,用離子方程式表示檢驗E中陽離子的方法________________。
③寫出D的稀溶液與Cu反應的離子方程式____________________________。
(2)若A為非金屬單質,X為水,該轉化關系為工業生產D的一系列反應。
①將B通入溴水中顏色褪去,體現了B的___________________性,寫出該變化的化學方程式________________________。
②A和H2發生化合反應得到的E,在B與E的反應中,氧化產物和還原產物的質量比為_______________________________。
③寫出D的濃溶液與Cu反應的化學方程式_________________________________________________________。
(3)若A為烴的含氧衍生物,醫療上常用75%(體積分數)A的水溶液作消毒劑,X為甲醇(CH3OH)。
①A→B的化學方程式為____________________________;C→D的化學方程式為_____________________________________。
②下列說法正確的是___________________________________(選填序號字母)
a. A 可通過葡萄糖分解反應得到 b. B 的官能團的結構簡式為-COH
c. C 可與 NaHCO3 反應產生 CO2 d. A 與X 互為同系物
③已知:CH≡CH 在一定條件下可與C反應得到E(結構簡式為 CH2=CHOOCCH3),則上述反應的反應類型為_______________________,E中的官能團名稱為_____________,E發生加聚反應的化學方程式為_____________________________。
【答案】![]() 4NH3+5O2
4NH3+5O2![]() 4NO+6H2O NH3+HNO3=NH4NO3 NH4++OH-
4NO+6H2O NH3+HNO3=NH4NO3 NH4++OH-![]() NH3↑+H2O 3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O 還原 SO2+Br2+2H2O=2HBr+H2SO4 2:1 Cu+2H2SO4(濃)
NH3↑+H2O 3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O 還原 SO2+Br2+2H2O=2HBr+H2SO4 2:1 Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O 2CH3CH2OH+O2
CuSO4+SO2↑+2H2O 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3OH+CH3COOH
2CH3CHO+2H2O CH3OH+CH3COOH![]() CH3COOCH3+H2O acd 加成反應 酯基和碳碳雙鍵 nCH2=CHOOCCH3
CH3COOCH3+H2O acd 加成反應 酯基和碳碳雙鍵 nCH2=CHOOCCH3![]()
![]()
【解析】
(1)若A 為可使濕潤的紅色石蕊試紙變藍的氣態氫化物,則A為NH3,X 為水,B為NO,C為NO2,D為HNO3,據此分析解答;
(2)若A為非金屬單質,X為水,將B通入溴水中顏色褪去,則A為S,B為SO2,C為SO3,D為H2SO4,據此分析解答;
(3)若A為烴的含氧衍生物,醫療上常用75%(體積分數)A的水溶液作消毒劑,則A為乙醇(CH3CH2OH),X為甲醇(CH3OH),則B為乙醛,C為乙酸,D為乙酸甲酯,據此分析解答。
(1)若A 為可使濕潤的紅色石蕊試紙變藍的氣態氫化物,則A為NH3,X 為水,B為NO,C為NO2,D為HNO3,
①A 的電子式為![]() ,A→B 氨氣的催化氧化,化學方程式為4NH3+5O2
,A→B 氨氣的催化氧化,化學方程式為4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
②NH3和HNO3發生化合反應得到的化合物硝酸銨,化學式是NH3+HNO3=NH4NO3,檢驗銨根離子的方法取少量待測液體于試管中,滴加氫氧化鈉溶液并加熱,用濕潤的紅色石蕊試紙于試管口,試紙變藍,證明有氨氣生成,進而證明有銨根離子存在,發生的離子反應為:NH4++OH-![]() NH3↑+H2O;
NH3↑+H2O;
③稀硝酸與Cu反應生成硝酸銅、一氧化氮和水,離子方程為3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O;
(2) 若A為非金屬單質,X為水,將B通入溴水中顏色褪去,則A為S,B為SO2,C為SO3,D為H2SO4;
①將SO2通入溴水中發生氧化還原反應生成硫酸和溴化氫,溴水顏色褪去,體現了SO2的還原性,該變化的化學方程式SO2+Br2
②S和H2發生化合反應得到的H2S,在H2S與SO2的反應中生成S和水,反應方程式為:2H2S+SO2=3S+2H2O,H2S中的S化合價升高,被氧化,SO2中的S元素化合價降低,被還原,氧化產物和還原產物的質量比為2:1;
③濃硫酸與Cu在加熱條件下反應生成硫酸銅、二氧化硫和水,化學方程式Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(3) 若A為烴的含氧衍生物,醫療上常用75%(體積分數)A的水溶液作消毒劑,,則A為乙醇(CH3CH2OH),X為甲醇(CH3OH),則B為乙醛,C為乙酸,D為乙酸甲酯;
①乙醇在催化劑加熱條件下與氧氣發生催化氧化反應,化學方程式為2CH3CH2OH+O2![]() 2CH3CHO+2H2O;C為乙酸,X為甲醇(CH3OH),乙酸和甲醇在濃硫酸加熱條件下發生酯化反應,化學方程式為CH3OH+CH3COOH
2CH3CHO+2H2O;C為乙酸,X為甲醇(CH3OH),乙酸和甲醇在濃硫酸加熱條件下發生酯化反應,化學方程式為CH3OH+CH3COOH![]() CH3COOCH3+H2O;
CH3COOCH3+H2O;
②a.A 為乙醇,無氧或缺氧的條件下,通過酶的催化作用,把葡萄糖等有機物不徹百底的氧化分解成酒精或乳酸等,反應為C6H12O6![]() 2C2H5OH+ 2CO2,故a正確;
2C2H5OH+ 2CO2,故a正確;
b.B為乙醛,則B的官能團的結構簡式為-CHO,故b錯誤;
c.C為乙酸,乙酸的酸性強于碳酸,則C可與NaHCO3反應產生CO2,故c正確;
d.結構相似,類別相同,分子組成上相差一個或多個-CH2-的有機物互為同系物,A為乙醇(CH3CH2OH),X為甲醇(CH3OH),互為同系物,故d正確;
答案選acd;
③已知:CH≡CH 在一定條件下可與C反應得到E(結構簡式為CH2=CHOOCCH3),三鍵變雙鍵,反應類型為加成反應,E中的官能團名稱為酯基和碳碳雙鍵,E發生加聚反應的化學方程式為nCH2=CHOOCCH3![]()
![]() 。
。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】短周期元素R、T、Q、W在周期表中的相對位置如圖所示,其中Q原子的質子數是其最外層電子數的三倍。下列說法正確的是

A. 原子半徑:R>T
B. 氧化物對應水化物的酸性:W>Q
C. 最簡單氣態氫化物的熱穩定性:R>Q
D. Q與W形成的化合物中,各原子的最外層都滿足8電子穩定結構
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為分析某鹽的成分, 做了如下實驗:
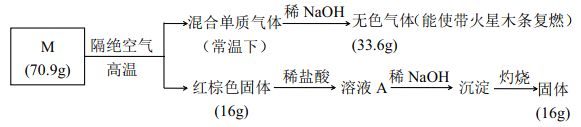
請回答:
(1)鹽 M 的化學式是_________;
(2)被 NaOH 吸收的氣體的電子式____________;
(3)向溶液 A 中通入H2S 氣體, 有淡黃色沉淀產生, 寫出反應的離子方程式________ (不考慮空氣的影響)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A.濃硫酸和濃硝酸都具有強氧化性,都能把 HCl 氣體氧化
B.非金屬氧化物不一定是酸性氧化物,金屬氧化物多數是堿性氧化物
C.同溫同壓下,兩份相同質量的鋅粉,分別與足量的稀硫酸和濃硫酸反應,產生氣體的體積相同
D.將 CO2 氣體通入BaCl2 溶液中至飽和未見沉淀生成,繼續通入 NH3 則有沉淀生成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表中是A、B、C、D、E五種短周期元素的某些性質,下列判斷正確的是

A. C、D、E 的氫化物的穩定性:C>D>E
B. 元素 A 的原子最外層軌道中無自旋狀態相同的電子
C. 元素 C、D 之間不可能形成化合物
D. 與元素 B 同周期且第一電離能最小的元素的單質能與 H2O 發生置換反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知298.15K時,可逆反應:Pb2+(aq)+Sn(s)![]() Pb(s)+Sn2+(aq)的平衡常數K=2.2,若溶液中Pb2+和Sn2+的濃度均為0.010mol·L-1,則反應進行的方向是
Pb(s)+Sn2+(aq)的平衡常數K=2.2,若溶液中Pb2+和Sn2+的濃度均為0.010mol·L-1,則反應進行的方向是
A. 向右進行 B. 向左進行 C. 處于平衡狀態 D. 無法判斷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 是一種高效安全消毒劑,常溫下
是一種高效安全消毒劑,常溫下![]() 為紅黃色有刺激性氣味氣體,其熔點為-59.5℃,沸點為11.0℃,能溶于水但不與水反應,遇熱水緩慢水解。某研究性學習小組欲制備
為紅黃色有刺激性氣味氣體,其熔點為-59.5℃,沸點為11.0℃,能溶于水但不與水反應,遇熱水緩慢水解。某研究性學習小組欲制備![]() 水溶液并檢驗其性質。
水溶液并檢驗其性質。
Ⅰ.二氧化氯水溶液制備。

在圓底燒瓶中先放入![]() 固體和
固體和![]() ,然后再加入5mL稀硫酸,用磁力攪拌棒攪拌(如圖),將燒瓶放在熱水浴中,保持60℃~80℃,至B中廣口瓶內呈深紅黃色時停止加熱。回答下列問題:
,然后再加入5mL稀硫酸,用磁力攪拌棒攪拌(如圖),將燒瓶放在熱水浴中,保持60℃~80℃,至B中廣口瓶內呈深紅黃色時停止加熱。回答下列問題:
(1)裝置A用水浴加熱的優點是_________;裝置A中水浴溫度不低于60℃,其原因是_______________。
(2)裝置A中反應生成![]() 及
及![]() 等產物的化學方程式為_____________________;
等產物的化學方程式為_____________________;
(3)裝置B的水中需放入冰塊的目的是__________________;已知![]() 緩慢水解生成的含氯化合物只有
緩慢水解生成的含氯化合物只有![]() 和
和![]() ,且物質的量之比為2:1,則該反應的化學方程式為____________;裝置C中的
,且物質的量之比為2:1,則該反應的化學方程式為____________;裝置C中的![]() 溶液吸收尾氣中的
溶液吸收尾氣中的![]() ,生成物質的量之比為的1:1的兩種鹽,一種為
,生成物質的量之比為的1:1的兩種鹽,一種為![]() ,另一種為_________________。
,另一種為_________________。
Ⅱ.![]() 的含量測定
的含量測定
步驟1:量取![]() 溶液
溶液![]() ,稀釋成
,稀釋成![]() 試樣;量取
試樣;量取![]() 試樣加入到錐形瓶中;
試樣加入到錐形瓶中;
步驟2:調節試樣的![]() ,加入足量的
,加入足量的![]() 晶體,振蕩后,靜置片刻;
晶體,振蕩后,靜置片刻;
步驟3:加入指示劑,用![]() 溶液滴定至終點,消耗
溶液滴定至終點,消耗![]() 溶液
溶液![]() 。
。
(4)已知:![]() ,
,![]() ,原
,原![]() 溶液的濃度為_____
溶液的濃度為_____![]() (用含字母的代數式表示),如果滴定速度過慢,會使計算出的數值______(填“偏大”、“偏小”或“不變”)。
(用含字母的代數式表示),如果滴定速度過慢,會使計算出的數值______(填“偏大”、“偏小”或“不變”)。
Ⅲ.設計實驗驗證![]() 的氧化性
的氧化性
(5)取適量![]() 水溶液加入
水溶液加入![]() 溶液中,振蕩,得無色溶液。欲檢驗
溶液中,振蕩,得無色溶液。欲檢驗![]() 的氧化產物,還需要用到的試劑是____________。
的氧化產物,還需要用到的試劑是____________。
(6)證明![]() 的氧化性比
的氧化性比![]() 強的方案是__________________________________。
強的方案是__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.已知:R-CH=CH-O-R′![]() R-CH2CHO + R′OH
R-CH2CHO + R′OH
(烴基烯基醚)
烴基烯基醚A的相對分子質量(Mr)為176,分子中碳氫原子數目比為3∶4 。與A相關的反應如下:
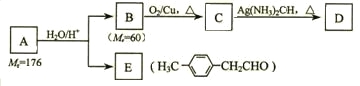
請回答下列問題:
⑴ A的分子式為_________________。
⑵ B的名稱是__________;A的結構簡式為_______________。
⑶寫出C → D反應的化學方程式:_____________________________。
⑷寫出兩種同時符合下列條件的E的同分異構體的結構簡式:
①屬于芳香醛; ②苯環上有兩種不同環境的氫原子。
_________________________、________________________。
Ⅱ.由E轉化為對甲基苯乙炔(![]() )的一條路線如下:
)的一條路線如下:

⑸寫出G的結構簡式:___________________________。
⑹寫出①-④步反應所加試劑、反應條件和①-③步反應類型:____________
序號 | 所加試劑及反應條件 | 反應類型 |
① | ||
② | ||
③ | ||
④ | —— |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)家用液化氣的主要成分之一是丁烷,當10kg丁烷完全燃燒并生成二氧化碳和液態水時,放出熱量為5×105kJ,試寫出表示丁烷燃燒熱的熱化學方程式:_____________________________________________________
(2)已知:C(s)+O2(g)===CO2(g);ΔH=-393.5 kJ/mol;2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ/mol,現有0.2 mol的炭粉和氫氣組成的懸浮氣,因混合物在氧氣中完全燃燒,共放出63.53 kJ熱量,則混合物中C與H2的物質的量之比為________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com