
CuSO4·5H2O![]() CuSO4·3H2O
CuSO4·3H2O![]() CuSO4·H2O
CuSO4·H2O![]() CuSO4
CuSO4
某課外活動小組準備用濃硫酸和銅片為主要原料制取少量膽礬,其主要步驟有:①取少量銅片放在干燥的蒸發皿內,用酒精燈灼燒到其表面變黑為止;②向蒸發皿內加入一定量濃硫酸并加熱,反應結束后發現有少量黑色固體及白色固體存在;③將上述冷卻后的反應混合物用水稀釋得藍色溶液,白色固體消失,但仍有黑色固體存在;④向稀釋后的所得溶液中加入過量堿式碳酸銅[Cu2(OH)2CO3],充分攪拌;⑤過濾,棄去不溶物;⑥將濾液轉回洗凈的蒸發皿內,用沸水浴緩緩加熱蒸發,濃縮至表面有晶膜析出時為止,取下蒸發皿使溶液冷卻,析出藍色晶體。
(1)步驟⑤中要用到的玻璃儀器有_________________________________________________。
(2)步驟④中發生反應的離子方程式是____________________________________________。
(3)簡述步驟③的具體操作方法:________________________________________________。
(4)下列敘述錯誤的是_____________
A.將銅片灼燒,可以減少濃硫酸的消耗量
B.用濃硫酸溶解灼燒后的銅片時,應在通風櫥中進行
C.步驟②中得到的黑色固體是CuO
D.步驟②中得到的白色固體是CuSO4
E.步驟⑥中為加快蒸發速度,也可用酒精燈直接給蒸發皿加熱
科目:高中化學 來源: 題型:閱讀理解
 (2009?廣東)銅單質及其化合物在很多領域有重要的用途,如金屬銅用來制造電線電纜,五水硫酸銅可用作殺菌劑.
(2009?廣東)銅單質及其化合物在很多領域有重要的用途,如金屬銅用來制造電線電纜,五水硫酸銅可用作殺菌劑.
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
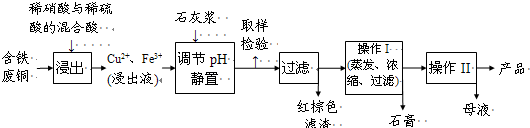
| 溫度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 膽礬 | 32 | 44.6 | 61.8 | 83.8 | 114 |
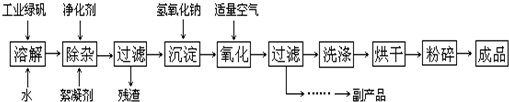
查看答案和解析>>
科目:高中化學 來源: 題型:
 (2010?陜西模擬)由CO與H2催化合成甲醇是生物質能利用的方法之一.
(2010?陜西模擬)由CO與H2催化合成甲醇是生物質能利用的方法之一.查看答案和解析>>
科目:高中化學 來源: 題型:
4、甲、乙、丙三位同學分別以銅屑為原料制取膽礬。
(1)甲同學稱取6.400g銅屑,置于燒杯中,加入98%濃H2SO4,加熱到銅屑完全溶解為止,然后轉移到另一儀器中,濃縮、結晶。
在上述實驗過程中,用到儀器有___________(填寫字母編號,多選扣分)。
a.托盤天平 b.電子天平 c.坩堝 d.蒸發皿
(2)乙同學認為甲實驗方案不符合“綠色化學”的理念,主要理由是此________________________。
乙同學設計如下實驗方案:稱取同質量銅屑放在敞口坩堝中灼燒,冷卻后,加100ml某濃度稀H2SO4,使之充分反應,接下的實驗操作與甲相同。若恰好反應,稀H2SO4的濃度(理論值)為_________mol/L
(3)丙同學設計如下實驗方案:稱取同質量銅屑,放入燒杯中,加入與上述(2)相同濃度相同體積稀H2SO4,加熱,并不斷通入空氣,使之充分反應,接下的實驗操作與甲相同。
寫出上述反應的化學方程式:___________________________________________。
丙同學的實驗方案優點在于_____________(填寫字母編號,多選扣分)。
a.制得的膽礬純度高 b.耗酸少,無污染 c.銅的轉化率高
(4)已知膽礬在不同加熱溫度下有不同產物生成:
![]()
丙同學將制得的25.00g膽礬加熱,結果得到灰白色的固體10.00g。經推斷可知,該固體組成成份和它們的物質的量__________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com