
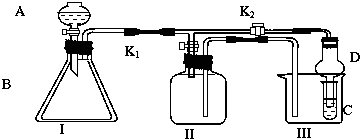
分析 (1)Ⅱ裝置中進氣管短,出氣管長,為向下排空氣法;NO與氧氣反應;
(2)用排水法可以收集O2和NO等氣體,二氧化氮與水反應,且易溶于水;
(3)比較H2SO4、H2CO3和H2SiO3的酸性強弱,可在Ⅰ中用碳酸鈉和稀硫酸反應生成二氧化碳,Ⅲ為硅酸鈉,與二氧化碳反應可生成硅酸沉淀;
(4)比較Ca(ClO)2>Cl2>Br2氧化性強弱,在Ⅰ中Ca(ClO)2與濃鹽酸反應生成氯氣,氯氣與Ⅲ中NaBr溶液反應生成溴,溶液顏色由無色變為橙色或橙紅色,注意防止氯氣污染環境.
解答 解:(1)Ⅱ裝置中進氣管短,出氣管長,為向下排空氣法,O2、NO2的密度大于空氣的密度,則O2、NO2應采用向上排空氣法收集;一氧化氮和氧氣能發生反應生成二氧化氮,一氧化氮應采用排水法收集,所以該裝置不能收集氧氣和一氧化氮,
故答案為:O2、NO2密度比空氣大,NO與空氣密度相差不大且與空氣中的氧氣反應;
(2)O2 和NO不能與水發生反應,而且難溶于水,所以能采用排水法收集,故答案為:將Ⅱ裝置加滿水;
(3)比較H2SO4、H2CO3和H2SiO3的酸性強弱,可在Ⅰ中用碳酸鈉和稀硫酸反應生成二氧化碳,Ⅲ為硅酸鈉,與二氧化碳反應可生成硅酸沉淀,
故答案為:Na2CO3;Na2SiO3溶液;裝置Ⅰ中產生氣泡、裝置C中產生白色沉淀;
(4)比較Ca(ClO)2>Cl2>Br2氧化性強弱,在Ⅰ中Ca(ClO)2與濃鹽酸反應生成氯氣,氯氣與Ⅲ中NaBr溶液反應生成溴,溶液顏色由無色變為橙色或橙紅色,注意防止氯氣污染環境,可用氫氧化鈉溶液吸收氯氣,
故答案為:濃鹽酸;NaBr溶液;溶液由無色變為橙色或黃色或橙紅色;氯氣易逸出污染環境.
點評 本題考查了實驗方案設計,題目難度中等,注意根據氣體的性質及密度選擇相應的收集方法以及實驗設計的方案的設計,側重于考查學生對實驗原理的把握和對儀器的使用.


科目:高中化學 來源: 題型:選擇題
| A. | pH=1的溶液中:Na+、Fe2+、NO3-、Cl- | |
| B. | pH=7的溶液中:Fe3+、Mg2+、Cl-、SO42- | |
| C. | 使酚酞變紅的溶液中:Ba2+、Cl-、Na+、NO3- | |
| D. | 加入鋁粉產生氫氣的溶液:Na+、Cu2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 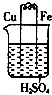 鐵上有氣泡 鐵上有氣泡 | |
| B. |  銅上有氣泡 銅上有氣泡 | |
| C. |  鐵片上析出紅色的銅 鐵片上析出紅色的銅 | |
| D. |  AB為導體,反應一段時間后,鐵球向下傾斜 AB為導體,反應一段時間后,鐵球向下傾斜 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
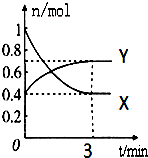 在一定溫度下,體積為2L的密閉容器中,NO2和N2O4之間發生反應:2NO2 (g) (紅棕色)?N2O4g)(無色),如圖所示.
在一定溫度下,體積為2L的密閉容器中,NO2和N2O4之間發生反應:2NO2 (g) (紅棕色)?N2O4g)(無色),如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 手機上用的鋰離子電池屬于二次電池 | |
| B. | 原電池中,陽離子一定向負極移動 | |
| C. | 甲醇燃料電池可把化學能轉化為電能 | |
| D. | 鋅錳干電池中,鋅電極是負極 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
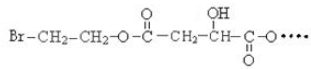
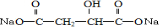 BHOCH2CH2OHC
BHOCH2CH2OHC D
D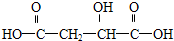
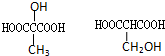
 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 41.8g固體物質為Na2CO3 | |
| B. | 41.8g固體物質為0.1mol Na2CO3和0.4mol Na2O2的混合物 | |
| C. | 41.8g固體物質為31.2g NaHCO3和10.6g Na2CO3的混合物 | |
| D. | 一定量的Na2O2為78g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com