
分析 ①取此溶液少許,滴在石蕊試紙上,試紙顯紅色,說明溶液呈酸性,則存在H+,肯定不能大量存在OH-、CO32-,則由溶液的電中性可知含有SO42-,不能存在Ba2+、Ag+;
②然后加入足量鹽酸,觀察不到明顯現象,說明不含Ag+;
③另取少許此溶液,加入足量氫氧化鈉溶液,有白色沉淀生成,說明含有Mg2+,以此解答該題.
解答 解:①取此溶液少許,滴在石蕊試紙上,試紙顯紅色,說明溶液呈酸性,則存在H+,肯定不能大量存在OH-、CO32-,則由溶液的電中性可知含有SO42-,不能存在Ba2+、Ag+;
②然后加入足量鹽酸,觀察不到明顯現象,說明不含Ag+;
③另取少許此溶液,加入足量氫氧化鈉溶液,有白色沉淀生成,說明含有Mg2+,
(1)根據以上分析可知,該溶液中一定存在的離子有:H+、Mg2+、SO42-;一定不存在的離子為:Ba2+、Ag+ OH-、CO32-,
故答案為:H+、Mg2+、SO42-; Ba2+、Ag+、OH-、CO32-;
(2)以上信息中存在的反應有:鎂離子與氫氧根離子生成氫氧化鎂沉淀,離子方程式為:Mg2++2 OH-=Mg(OH)2↓,故答案為:Mg2++2OH-=Mg(OH)2↓.
點評 本題考查了離子反應、常見的離子檢驗方法,為高頻考點,題目難度中等,注意熟練掌握常見離子之間發生的反應現象及離子檢驗的方法,明確某些離子的特征反應,如鋁離子、亞鐵離子的特征反應.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
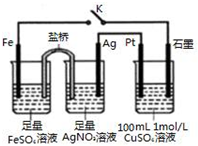
| A. | 鹽橋中的電解質不可以用KCl | |
| B. | 導線中通過0.5 mol e-后,向CuSO4溶液中加入12.4g CuCO3,該溶液可恢復原組成 | |
| C. | 閉合K,Pt電極上發生的反應為:4OH--4e-=O2↑+2H2O | |
| D. | 閉合K,整個電路中電流的流向為:Ag電極→Pt電極→石墨電極→Fe電極→Ag電極 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 丙烯與等物質的量氯化氫加成只生成一種產物 | |
| B. | 1mol丙烯完全燃燒的耗氧量為4.5mol | |
| C. | 聚丙烯的鏈節是-CH2-CH2-CH2- | |
| D. | 1mol丙烯和1mol聚丙烯完全燃燒放出CO2的量相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑 P>S>Cl | |
| B. | 最高價氧化物對應水化物的酸性 H3PO4<H2SO4<HClO4 | |
| C. | 氫化物的穩定性 PH3<H2S<HCl | |
| D. | 元素的非金屬性 P>S>Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上常采用電解法冶煉Y 單質 | |
| B. | 氣態氫化物的穩定性:H2W強于H2Z | |
| C. | 離子半徑由大到小:Z2->X+>Y3+>W2- | |
| D. | W、X 形成的化合物中陰、陽離子個數比一定是1:2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com