
已知:2R—Cl+2Na→R—R+2NaCl(R代表烴基),下列有機物通過上述反應可制得對二甲基環己烷的是
A.2,3—二氯丁烷
B.1,3—二氯丁烷
C.2—氯丁烷
D.2,5—二氯己烷和1,2—二氯乙烷
科目:高中化學 來源:2015-2016學年遼寧東北育才學校高一下第二段考化學試卷(解析版) 題型:選擇題
烷烴分子可以看作由以下基團組合而成: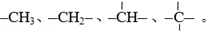 如某烷烴分子中同時存在這四種基團,則該烷烴最少含有的碳原子數應是( )
如某烷烴分子中同時存在這四種基團,則該烷烴最少含有的碳原子數應是( )
A.6 B.7 C.8 D.10
查看答案和解析>>
科目:高中化學 來源:2016屆黑龍江哈爾濱六中高三下三模理綜化學試卷(解析版) 題型:填空題
鎳電池廣泛應用于混合動力汽車系統,電極材料由NiO2、Fe和碳粉涂在鋁箔上制成。
放電過程中產生Ni(OH)2和Fe(OH)2,Fe(OH)2最終氧化、脫水生成氧化鐵。由于電池使用后電極材料對環境有危害,某學習小組對該電池電極材料進行回收研究。
已知 :①NiO2有強氧化性,可與濃鹽酸反應;
②NiCl2易溶于水,Fe3+不能氧化Ni2+。
③某溫度下一些金屬氫氧化物的Ksp及開始沉淀和完全沉淀時的理論pH如表所示:
M(OH)n | Ksp | pH | |
開始沉淀 | 沉淀完全 | ||
Al(OH)3 | 2.0×10-32 | 4.1 | - |
Fe(OH)3 | 3.5×10-38 | 2.2 | 3.5 |
Fe(OH)2 | 1.0×10-15 | 7.5 | 9.5 |
Ni(OH)2 | 6.5×10-18 | 6.4 | 8.4 |
回答下列問題:
(1)該電池的正極反應式為; ;
(2)維持電流強度為1.0A,消耗0.28gFe,理論電池工作 s。(已知F=96500C/mol)
(3)對該電池電極材料進行回收方案設計:
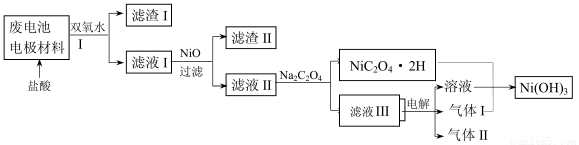
①方案中加入適量雙氧水的目的是 ;在濾液I中慢慢加入NiO固體,則依次析出沉淀
和沉淀 (填化學式)。若兩種沉淀都析出,pH應控制在不超過
(離子濃度小于1×10-5mol/L為完全沉淀,lg2=0.3、lg3=0.4);設計將析出的沉淀混合物中的兩種物質分離開來的實驗方案 。
②濾液III中溶質的主要成分是 (填化學式);氣體I為 ,判斷依據是 。
查看答案和解析>>
科目:高中化學 來源:2016屆海南中學高三考前高考模擬十化學試卷(解析版) 題型:選擇題
溶液的pH、體積相同的鹽酸和醋酸兩種溶液,下列敘述錯誤的是
A.它們與NaOH完全中和時,醋酸溶液所消耗的NaOH少
B.它們分別與足量CaCO3反應時,放出的CO2一樣多
C.兩種溶液的n(Cl-)= n(CH3COO-)相同
D.分別用水稀釋相同倍數時,n(Cl-)<n(CH3COO-)
查看答案和解析>>
科目:高中化學 來源:2016屆海南中學高三考前高考模擬十化學試卷(解析版) 題型:選擇題
同位素示蹤法可用于反應機理的研究,下列反應或轉化中同位素示蹤表示正確的是
A.2Na218O2 +2H2O====4Nal8OH+O2↑
B.NH4Cl+ 2H2O====NH3·2H2O+HCl
C.2KMnO4 +5H218O2 +3H2SO4====K2SO4+2MnSO4 +518O2↑+8H2O
D.K37ClO3+6HCl===K37Cl+3Cl2↑+3H2O
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三臨考模擬化學試卷(解析版) 題型:推斷題
U、V、W、X、Y、Z是原子序數依次增大的六種常見元素。Y的單質在W2中燃燒的產物可使品紅溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的單質在W2中燃燒可生成UW和UW2兩種氣體。X的單質是一種金屬,該金屬單質在UW2中劇烈燃燒生成黑、白兩種固體。
請回答下列問題:
(1)X在周期表中的位置:____________,UW2的電子式為____________;
(2)寫出下列反應的化學方程式,Z在高溫下與水反應_______________________________________;
(3)U、V、W形成的10電子氫化物中,氫化物的穩定性從強到弱的順序是____________(寫化學式),V元素的氫化物極易溶于水的主要原因是__________________________,該氫化物與空氣可以構成一種環保燃料電池,電解質溶液是KOH,其負極的電極反應式為____________。
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三臨考模擬化學試卷(解析版) 題型:選擇題
下列關于熱化學反應的描述中正確的是
A.HCl和NaOH反應的中和熱△H=-57.3kJ/mol,則H2SO4和NaOH完全反應的中和熱為-114.6kJ/mol
B.CO(g)的燃燒熱是283.0kJ/mol,則表示CO燃燒熱的熱化學方程式為2CO(g)+O2(g)=2CO2(g);△H=-283.0kJ/mol
C.一個化學反應的熱效應,只與反應的始態與終態有關,與反應的過程無關。
D.需要加熱才能發生的反應一定是吸熱反應
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三考前預測化學試卷(解析版) 題型:填空題
常溫下,將0.01molNH4Cl和0.002molNaOH溶于水,形成1L混合溶液:
(1)該溶液中存在三個平衡體系,用電離方程式或離子方程式表示:
①____________
②____________
③____________。
(2)溶液中含有的微粒是__________________。
(3)在上述溶液中,電荷守恒是:____________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省高二5月月考化學試卷(解析版) 題型:實驗題
環己酮是重要的化工原料,也是重要的工業溶劑。實驗室制備環己酮的原理、有關數據及裝置示意圖如下:
反應原理: 
反應放熱,溫度過高或者重鉻酸鈉過量會進一步氧化。
主要物料及產物的物理參數:

實驗裝置:
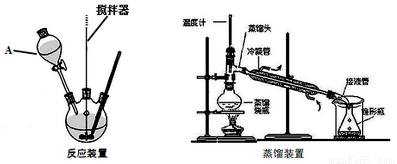
實驗步驟:
1.投料:在100mL三頸燒瓶中加入20mL水,慢慢加入5mL濃硫酸搖動,振蕩下緩慢加入5mL(4.8g,0.048mol)環己醇,并將混合液溫度降至30℃以下。將5g(0.019mol)重鉻酸鈉溶于水得橙紅色溶液備用。
2.反應:將約1/5的重鉻酸鈉溶液加入三頸燒瓶中,充分攪拌使之混合均勻。冷水浴冷卻,控制反應溫度在55~60℃。待橙紅色消失后,再將剩余的重鉻酸鈉溶液分四次加入到三頸燒瓶中。當溫度自動下降時,加入4mL甲醇使反應液完全變成墨綠色(三價鉻);
3.蒸餾:在反應瓶中加入30mL水,并改為蒸餾裝置,收集90~99℃之間的餾分(環己酮與水的共沸物)至無油珠為止;
4.萃取、干燥:將餾出液用食鹽飽和后轉入分液漏斗中,分出有機層。水層用8mL乙醚提取一次,將乙醚提取液和有機層合并,用無水硫酸鎂干燥; 5.蒸餾,收集環己酮產品2.6g。 請回答下列問題:
(1)裝置A的名稱是___________。
(2)完成并配平反應方程式:

(3)反應過程中加入甲醇后有無色氣體生成。加入甲醇的作用是___________,請用離子方程式表示反應原理___________。
(4)步驟4向餾出液加入食鹽的目的是___________,將乙醚提取液和有機層合并的原因是___________。
(5)計算所得產品的產率___________。(保留三位有效數字)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com