
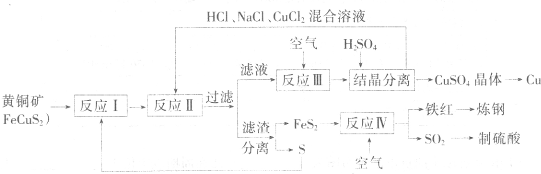
一種以黃銅礦和硫磺為原料制取銅和其他產物的新工藝,原料的綜合利用率較高。其主要流程如下:
注:反應Ⅱ的離子方程式為Cu2++CuS+4Cl—=2CuCl2-+S
請回答下列問題:
⑴反應Ⅰ的產物為(填化學式) ▲ 。
⑵反應Ⅲ的離子方程式為 ▲ 。
⑶一定溫度下,在反應Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸銅晶體,其原因是
▲ 。
⑷煉鋼時,可將鐵紅投入熔融的生鐵中,該過程中主要反應的化學方程式是 ▲ 。
⑸某硫酸廠為測定反應Ⅳ所得氣體中SO2的體積分數,取280mL(已折算成標準狀況)氣體樣品與足量Fe2(SO4)3溶液完全反應后,用濃度為0.02000 mol/L的K2Cr2O7標準溶液滴定至終點,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr 3++
3++  Fe3++ H2O(未配平)
Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,發生反應的離子方程式為 ▲ 。
②反應Ⅳ所得氣體中SO2的體積分數為 ▲ 。
科目:高中化學 來源: 題型:閱讀理解
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| O | 2- 7 |
查看答案和解析>>
科目:高中化學 來源: 題型:
一種以黃銅礦和硫磺為原料制取銅和其他產物的新工藝,原料的綜合利用率較高。其主要流程如下:

注:反應Ⅱ的離子方程式為Cu2++CuS+4Cl—=2CuCl2-+S
請回答下列問題:
⑴反應Ⅰ的產物為(填化學式) ▲ 。
⑵反應Ⅲ的離子方程式為 ▲ 。
⑶一定溫度下,在反應Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸銅晶體,其原因是
▲ 。
⑷煉鋼時,可將鐵紅投入熔融的生鐵中,該過程中主要反應的化學方程式是 ▲ 。
⑸某硫酸廠為測定反應Ⅳ所得氣體中SO2的體積分數,取280mL(已折算成標準狀況)氣體樣品與足量Fe2(SO4)3溶液完全反應后,用濃度為0.02000 mol/L的K2Cr2O7標準溶液滴定至終點,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,發生反應的離子方程式為 ▲ 。
②反應Ⅳ所得氣體中SO2的體積分數為 ▲ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
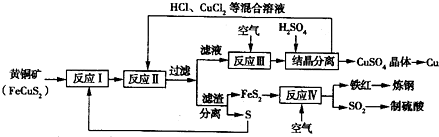
一種以黃銅礦和硫磺為原料制取銅和其他產物的新工藝,原料的綜合利用率較高。其主要流程如下:
注:反應Ⅱ的離子方程式為Cu2++CuS+4Cl—=2CuCl2-+S
請回答下列問題:
⑴反應Ⅰ的產物為(填化學式) ▲ 。
⑵反應Ⅲ的離子方程式為 ▲ 。
⑶一定溫度下,在反應Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸銅晶體,其原因是
▲ 。
⑷煉鋼時,可將鐵紅投入熔融的生鐵中,該過程中主要反應的化學方程式是 ▲ 。
⑸某硫酸廠為測定反應Ⅳ所得氣體中SO2的體積分數,取280mL(已折算成標準狀況)氣體樣品與足量Fe2(SO4)3溶液完全反應后,用濃度為0.02000 mol/L的K2Cr2O7標準溶液滴定至終點,消耗K2Cr2O7溶液25.00mL 。
已知:Cr2O72-+ Fe2++ H+→Cr3++ Fe3++H2O(未配平)
①SO2通入Fe2(SO4)3溶液,發生反應的離子方程式為 ▲ 。
②反應Ⅳ所得氣體中SO2的體積分數為 ▲ 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com