
隨著人們生活質量的不斷提高,廢電池進行集中處理的問題被提到議事日程,其首要原因是( )。
| A.利用電池外殼的金屬材料 |
| B.防止電池中汞、鎘和鉛等金屬離子對土壤和水源的污染 |
| C.不使電池中滲泄的電解液腐蝕其他的物品 |
| D.回收其中的石墨電極 |
科目:高中化學 來源: 題型:單選題
鉛蓄電池的反應原理為:2PbSO4+2H2O Pb+PbO2+2H2SO4,下列敘述中,正確的是
Pb+PbO2+2H2SO4,下列敘述中,正確的是
| A.PbSO4的氧化性比PbO2的強、還原性比Pb的強 |
| B.放電時,PbO2為氧化劑、做負極,Pb為還原劑、做正極 |
| C.放電時,當有2 mol H2SO4反應時,會有1.204×1024個電子從鉛電極流出 |
| D.充電時,PbSO4既被氧化又被還原,Pb是陽極產物之一 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
以葡萄糖為燃料的微生物燃料電池結構示意圖如圖所示。關于該電池的敘述正確的是( )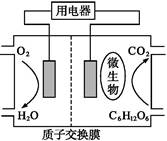
| A.該電池能夠在高溫下工作 |
B.電池的負極反應為:C6H12O6+6H2O-24e- 6CO2↑+24H+ 6CO2↑+24H+ |
| C.放電過程中,H+從正極區向負極區遷移 |
| D.在電池反應中,每消耗1 mol氧氣,理論上能生成標準狀況下CO2氣體L |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
結合下圖判斷,下列敘述正確的是( )
| A.Ⅰ和Ⅱ中正極均保護 |
| B.Ⅰ和Ⅱ中負極反應均是Fe-2e-=Fe2+ |
| C.Ⅰ和Ⅱ中正極反應均是O2+2H2O+4e-=4OH- |
| D.Ⅰ和Ⅱ中分別加入少量K3[Fe(CN)6]溶液,均有藍色沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
化合物Bilirubin在一定波長的光照射下發生分解反應,反應物濃度隨反應時間變化如下圖所示,計算反應4~8 min 間的平均反應速率和推測反應16 min 時反應物的濃度,結果應是( )。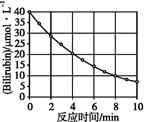
| A.2.5 μmol·L-1·min-1和2.0 μmol·L-1 |
| B.2.5 μmol·L-1·min-1和2.5 μmol·L-1 |
| C.3.0 μmol·L-1·min-1和3.0 μmol·L-1 |
| D.5.0 μmol·L-1·min-1和3.0 μmol·L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
關于原電池的敘述中正確的是( )。
| A.任何化學反應,均可以設計成原電池 |
| B.原電池是把化學能直接轉化成電能的裝置 |
| C.原電池的兩極必須都是金屬 |
| D.原電池都可以提供持續穩定的電流,應用十分廣泛 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
如圖是工業電解飽和食鹽水的裝置示意圖,下列有關說法中不正確的是( )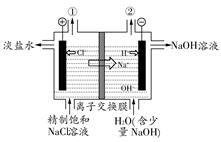
| A.裝置中出口①處的物質是氯氣,出口②處的物質是氫氣 |
| B.該離子交換膜只能讓陽離子通過,不能讓陰離子通過 |
C.裝置中發生反應的離子方程式為:2Cl-+2H+ Cl2↑+H2↑ Cl2↑+H2↑ |
| D.該裝置是將電能轉化為化學能 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用石墨作電極電解200 mL CuSO4溶液,電解過程中電子轉移的物質的量n(e-)與產生氣體的體積V(g)(標準狀況)的關系如圖所示,下列說法正確的是 ( )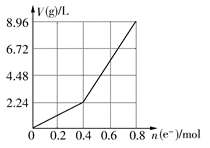
| A.電解前CuSO4溶液的物質的量濃度為2 mol/L |
| B.電解后所得溶液中c(H+)=2 mol/L |
| C.當n(e-)=0.6 mol時,V(H2):V(O2)=2:3 |
| D.向電解后的溶液中加入16 g CuO,則溶液可恢復為電解前的濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
如圖,纏上金屬條的鐵釘插在含有酚酞的NaCl溶液中,可以看到在金屬條表面的溶液出現粉紅色。該金屬條可能是 ( )。
| A.銅 | B.鎂 | C.鋁 | D.鋅 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com