
A鎳(Ni)可形成多種配合物,且各種配合物有廣泛的用途。
(1)配合物Ni(CO)4常溫下為液態,易溶于CCl4、苯等有機溶劑。固態Ni(CO)4屬于 ____________晶體;基態Ni原子的電子排布式為 _______________;
寫出兩種與配體CO互為等電子體微粒的化學式_____________、________________ 。
(2)某鎳配合物結構如圖所示,分子內含有的作用力有____________(填序號)。
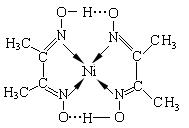
A.氫鍵 B.離子鍵 C.共價鍵 D.金屬鍵 E.配位鍵
(3)很多不飽和有機物在Ni催化下可與H2發生加成反應,
如①CH2=CH2、②HC ≡ CH、③ ![]() ④HCHO等,其中碳原子采取sp2雜化的分子有_________(填序號);HCHO分子的空間構型為:__________。
④HCHO等,其中碳原子采取sp2雜化的分子有_________(填序號);HCHO分子的空間構型為:__________。
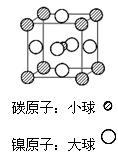
(4)據報道,某種含有鎂、鎳和碳三種元素的晶體具有超導性,其結構如圖所示。則該晶體的化學式為__________ 。晶體中每個鎂原子周圍距離最近的鎳原子有 _________個。
科目:高中化學 來源: 題型:閱讀理解
 能源問題日益成為制約國際社會經濟發展的瓶頸,越來越多的國家開始實行“陽光計劃”,開發太陽能資源,尋求經濟發展的新動力.
能源問題日益成為制約國際社會經濟發展的瓶頸,越來越多的國家開始實行“陽光計劃”,開發太陽能資源,尋求經濟發展的新動力.| A-B | A=B | A≡B | ||
| CO | 鍵能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 鍵能差值(kJ?mol-1) | 441.2 273 | |||
| N2 | 鍵能(kJ?mol-1) | 154.8 | 418.3 | 941.7 |
| 鍵能差值(kJ?mol-1) | 263.6 523.3 | |||
查看答案和解析>>
科目:高中化學 來源: 題型:
碳元素是形成單質及其化合物種類最多的元素。回答下列有關問題。
(1)碳元素可形成多種不同形式的單質,下列是幾種單質的結構圖
a b
c
觀察上述結構,判斷a中碳原子的雜化方式為 ,b對應的物質是 ,
c是C60的分子結構模型,在每個C60分子中形成的σ鍵數目為 。
(2)在C60單質中,微粒之間的作用力為 ,C60能與金屬鉀化合生成具有超導性的K3C60,在K3C60中陰陽離子個數比為1∶3,則K3C60屬于 晶體。
(3)CO是碳元素的常見氧化物,分子中C原子上有一對孤對電子,與N2互為等電子體,則CO的結構式為 ;寫出另一與CO互為等電子體的化學式 。
(4)CO可以和很多過渡金屬形成配合物。金屬鎳粉在CO氣流中輕微地加熱,可生成液態的Ni(CO)4,用配位鍵表示Ni(CO)4 的結構為 ;寫出基態Ni原子的電子排布式 。
(5)科學發現,C和Ni、Mg元素的原子形成的晶體也具有超導性,其晶胞的結構特點如右圖,則該化合物的化學式為 ; C、Ni、Mg三種元素中,電負性最大的是 。
(6)碳的氫化物甲烷在自然界中廣泛存在,其中可燃冰是有待人類開發的新能源。可燃冰是一種籠狀結構,CH4分子存在于H2O分子形成的籠子中(如右圖所示)。兩種分子中,共價鍵的鍵能 ;CH4分子與H2O分子的分子量相差不大,但兩種物質的熔沸點相差很大,其主要原因是 。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年江蘇省海門市高二下學期期末教學質量調研化學試題 題型:填空題
碳元素是形成單質及其化合物種類最多的元素。回答下列有關問題。
(1)碳元素可形成多種不同形式的單質,下列是幾種單質的結構圖
a  b
b  c
c 
觀察上述結構,判斷a中碳原子的雜化方式為 ,b對應的物質是 ,
c是C60的分子結構模型,在每個C60分子中形成的σ鍵數目為 。
(2)在C60單質中,微粒之間的作用力為 ,C60能與金屬鉀化合生成具有超導性的K3C60,在K3C60中陰陽離子個數比為1∶3,則K3C60屬于 晶體。
(3)CO是碳元素的常見氧化物,分子中C原子上有一對孤對電子,與N2互為等電子體,則CO的結構式為 ;寫出另一與CO互為等電子體的化學式 。
(4)CO可以和很多過渡金屬形成配合物。金屬鎳粉在CO氣流中輕微地加熱,可生成液態的Ni(CO)4,用配位鍵表示Ni(CO)4的結構為 ;寫出基態Ni原子的電子排布式 。
(5)科學發現,C和Ni、Mg元素的原子形成的晶體也具有超導性,其晶胞的結構特 點如右圖,則該化合物的化學式為 ; C、Ni、Mg三種元素中,電負性最大的是 。
點如右圖,則該化合物的化學式為 ; C、Ni、Mg三種元素中,電負性最大的是 。
(6)碳的氫化物甲烷在自然界中廣泛存在,其中可燃冰是有待人類開發的新能源。可燃冰是一種籠狀結構,CH4分子存在于H2O分子形成的籠子中(如右圖所示)。兩種分子中,共價鍵的鍵能 ;CH4分子與H2O分子的分子量相差不大,但兩種物質的熔沸點相差很大,其主要原因是 。
查看答案和解析>>
科目:高中化學 來源:2012屆江蘇省海門市高二下學期期末教學質量調研化學試題 題型:填空題
碳元素是形成單質及其化合物種類最多的元素。回答下列有關問題。
(1)碳元素可形成多種不同形式的單質,下列是幾種單質的結構圖
a  b
b  c
c 
觀察上述結構,判斷a中碳原子的雜化方式為 ,b對應的物質是 ,
c是C60的分子結構模型,在每個C60分子中形成的σ鍵數目為 。
(2)在C60單質中,微粒之間的作用力為 ,C60能與金屬鉀化合生成具有超導性的K3C60,在K3C60中陰陽離子個數比為1∶3,則K3C60屬于 晶體。
(3)CO是碳元素的常見氧化物,分子中C原子上有一對孤對電子,與N2互為等電子體,則CO的結構式為 ;寫出另一與CO互為等電子體的化學式 。
(4)CO可以和很多過渡金屬形成配合物。金屬鎳粉在CO氣流中輕微地加熱,可生成液態的Ni(CO)4,用配位鍵表示Ni(CO)4 的結構為 ;寫出基態Ni原子的電子排布式 。
(5)科學發現,C和Ni、Mg元素的原子形成的晶體也具有超導性,其晶胞的結構特點如右圖,則該化合物的化學式為 ; C、Ni、Mg三種元素中,電負性最大的是 。

(6)碳的氫化物甲烷在自然界中廣泛存在,其中可燃冰是有待人類開發的新能源。可燃冰是一種籠狀結構,CH4分子存在于H2O分子形成的籠子中(如右圖所示)。兩種分子中,共價鍵的鍵能 ;CH4分子與H2O分子的分子量相差不大,但兩種物質的熔沸點相差很大,其主要原因是 。

查看答案和解析>>
科目:高中化學 來源: 題型:
(09鹽城第三次調研)在Ni、NiO、Ni3C、γ-Al2O3組成的催化劑表面,可實現H2O、CO2及CH4合成乙醇。
 (1)下列說法正確的是 (選填序號)。
(1)下列說法正確的是 (選填序號)。
A.第一電離能:碳原子大于氧原子
B.CO2分子中含有2個σ鍵和2個π鍵
C.CH4分子中碳原子采用sp3雜化
D.二甲醚的沸點比乙醇高
(2)鎳原子基態時的核外電子排布式 。
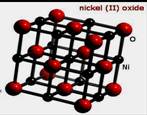
(3)NiO晶胞如右上圖所示,每個晶胞中與每個Ni2+距離相等且最近的Ni2+有 個,某種有缺陷的氧化鎳晶體
由Ni2+、Ni3+、O2-及空隙組成,可表示為Ni0.98O,則n(Ni2+)/n(Ni3+)= 。
(4)對苯二甲酸( ![]() )、4,4’-聯吡啶[
)、4,4’-聯吡啶[![]() (可簡化為
(可簡化為 ![]() )]等與Ni2+能形成多核配合物。配合物[Ni2(TPHA)(bpy)4](ClO4)2絡離子的結構如下圖:
)]等與Ni2+能形成多核配合物。配合物[Ni2(TPHA)(bpy)4](ClO4)2絡離子的結構如下圖:

該絡合物中配位原子是: ;依據價層互斥理論,ClO4-空間結構為 型。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com