
【題目】某同學設計下列方案對A 鹽的水溶液進行鑒定:

由此得出的結論中一定不正確的是( )
A.D溶液中存在Fe(SCN)3B.A 一定為無氧酸鹽FeBr2
C.B可為AgBrD.濾液中有Fe3+
【答案】B
【解析】
由圖中轉化可知,B為A與硝酸銀反應生成的淺黃色沉淀,根據元素守恒知則為AgBr,所以A中含有Br-,C中加KSCN溶液變為血紅色溶液,所以D為Fe(SCN)3溶液,則C中含有Fe3+,A中含有鐵元素,硝酸具有強氧化性,能氧化亞鐵離子生成鐵離子,所以A為可能含有Fe3+或Fe2+,以此來解答。
A. 通過以上分析知,D中含有Fe(SCN)3,A項正確;
B. 硝酸具有強氧化性,能將亞鐵離子氧化生成鐵離子,所以A中可能是FeBr2,也可能是FeBr3,也可能是二者的混合物,B項錯誤;
C. 能和銀離子反應生成淡黃色沉淀的離子是溴離子,所以B是AgBr,C項正確;
D. C能和硫氰化鉀溶液反應生成血紅色溶液,說明C中含有Fe3+,D項正確;
答案選B。


科目:高中化學 來源: 題型:
【題目】LED系列產品是被看好的一類節能新產品,下圖是一種氫氧燃料電池驅動LED發光的裝置。下列有關敘述正確的是
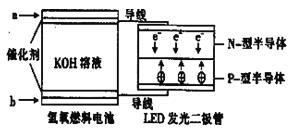
A.a處通入氫氣,發生了還原反應:H2-2e-+2OH-=2H2O
B.b處通入氧氣,為電池的正極
C.該裝置中只涉及兩種形式的能量轉化,電池中的KOH溶液也可用稀硫酸溶液代替
D.P-型半導體連接的是電池負極.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】雌二醇的結構簡式如圖,下列說法不正確的是
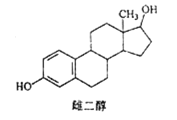
A. 能與 Na、NaOH溶液、Na2CO3溶液反應
B. 能發生加成反應、取代反應、消去反應
C. 該分子中所有碳原子不可能在同一個平面內
D. 可與 FeC13溶液發生顯色反應,但不能發生氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是課外活動小組的同學設計的4個噴泉實驗方案。下列有關操作不可能引發噴泉現象的是( )
A.擠壓裝置①的膠頭滴管使CCl4全部進入燒瓶,片刻后打開止水夾
B.擠壓裝置②的膠頭滴管使NaOH溶液全部進入燒瓶,片刻后打開止水夾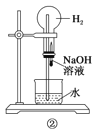
C.用鼓氣裝置從裝置③的a處不斷鼓入空氣并打開止水夾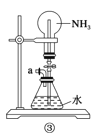
D.向裝置④的水槽中慢慢加入足量濃硫酸并打開止水夾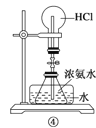
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列粒子中,中心原子雜化軌道類型相同,粒子的空間構型也相同的是( )
A. PCl3、BCl3B. H3O+、SO3
C. BeCl2、CS2D. NH3、CH4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】類推思維是化學解題中常用的一種思維方法,下列有關離子方程式的類推正確的是)
選項 | 已知 | 類推 |
A | 將Fe加入CuSO4溶液中:Fe+Cu2+=== Cu+Fe2+ | 將Na加入到CuSO4溶液中:2Na+Cu2+=== Cu+2Na+ |
B | 向Ca(ClO)2溶液中通入少量CO2:CO2+H2O+Ca2++2ClO-=== CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:SO2+H2O+Ca2++2ClO-=== CaSO3↓+2HClO |
C | 惰性電極電解氯化鈉溶液:2Cl-+2H2O | 惰性電極電解MgBr2溶液:2Br-+2H2O |
D | 稀鹽酸與NaOH溶液反應至中性:H++OH-===H2O | 稀硝酸與Ba(OH)2溶液反應至中性:H++OH-===H2O |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關有機化合物的性質和用途的說法正確的是 ( )
A.乙烯分子與苯分子中的碳碳鍵相同,二者都能發生加成反應
B.乙烷、乙烯、苯乙烯(![]() )分子結構中都含有不飽和碳原子
)分子結構中都含有不飽和碳原子
C.乙醇既可作燃料,也可在日常生活中使用,如一定濃度的乙醇可用于殺菌、消毒
D.淀粉、油脂、蛋白質都屬于高分子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧化鐵紅(Fe2O3)用途廣泛,用廢鐵皮制取鐵紅的部分流程示意圖如下:
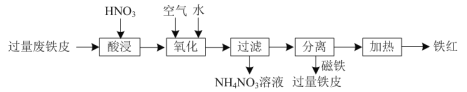
⑴“酸浸”時發生反應的離子方程式是______。
⑵“氧化”時有紅褐色沉淀生成,該反應的離子方程式為______。
⑶將鐵紅與FeS2混合焙燒可以生成磁性氧化鐵和SO2,該反應的化學方程式為______。
⑷“淬火”是將紅熱的鐵器浸入水中急速冷卻以增加鐵器的硬度以及減緩腐蝕,反應歷程如圖,寫出該歷程中第Ⅰ步反應的方程式______。
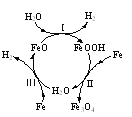
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.在一密閉容器中充入1molH2和1molI2,壓強為p(Pa),并在一定溫度下使其發生反應:H2(g)+I2(g)![]() 2HI(g)。
2HI(g)。
(1)保持容器容積不變,向其中充入1molHe,反應速率________(填“加快”“減慢”或“不變”,下同)。
(2)保持容器內氣體壓強不變,向其中充入1molHe,反應速率________。
II.航天飛機常采用新型燃料電池作為電能來源,燃料電池一般指采用H2、CH4、CO、C2H5OH等可燃物質與O2一起構成的電池裝置。它可直接將化學能轉化為電能,氫氧燃料電池以KOH溶液為電解質,其總反應的化學方程式為2H2+O2=2H2O。
(3)負極上的電極反應為______________________________。
(4)工作過程中時,溶液的c(OH-)_______(填“增大”、“減小”或“不變”)。
Ⅲ..A、B、C、D、E、W、T六種短周期主族元素,它們的核電荷數依次增大。A可與D、E形成10電子分子。B原子的最外層電子數等于次外層電子數,C原子最外層電子數是次外層電子數的2倍,W的L層電子數為K層和M層電子數之和,D和W同主族。回答下列問題:
(5)元素B在周期表中的位置是_______________________。
(6)元素C的原子結構示意圖為_______________________。
(7)元素C與W可形成CW2,C與T可形成CT4,這兩種化合物均可做溶劑,其電子式分別為____________________________________。
(8)元素A與D、E形成10電子分子的結構式分別為_______________________________。
(9)元素D、W的簡單氫化物的沸點高的為____________(用化學式表示)。
(10)1molCA4與D2完全反應生成兩種氣體時放出熱量802kJ,則該反應的熱化學方程式為__________________________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com