
一定溫度下,反應X2(g)+H2(g) 2HX(g)的平衡常數為100。若將1.0mol的HX(g)通入體積為1.0L的密閉容器中,在該溫度時HX(g)的最大分解率接近于( )
2HX(g)的平衡常數為100。若將1.0mol的HX(g)通入體積為1.0L的密閉容器中,在該溫度時HX(g)的最大分解率接近于( )
 A. 5% B. 17% C. 25% D.33%
A. 5% B. 17% C. 25% D.33%
 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源:2015-2016學年浙江省高二下期末化學試卷(解析版) 題型:選擇題
氧化銅礦用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO2— 4、Mg2+、A13+、Fe2+) 經下列流程可制得高純度硫酸銅晶體:
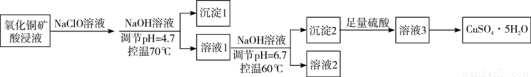
已知:該實驗條件下,各金屬離子沉淀的pH如圖所示。下列判斷正確的是
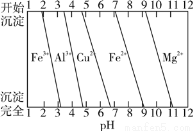
A.沉淀1的主要成分為Al(OH)3和Fe(OH)3
B.溶液2中所含金屬陽離子只有Mg2+
C.將溶液3蒸干即得CuSO4·5H2O晶體
D.若不加入NaClO溶液,對制得硫酸銅晶體的純度將無影響
查看答案和解析>>
科目:高中化學 來源:2015-2016學年寧夏高二下期末化學試卷(解析版) 題型:選擇題
城市居民所用的液化石油氣成分為丁烷,在使用過程中常有一些雜質以液態形式沉積于鋼瓶底部,這些雜質可能是 ( )
A.丙烷 B.乙烷和丙烷 C.乙烷和甲烷 D.戊烷和己烷
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省高一下期末化學試卷(解析版) 題型:選擇題
符合如圖所示的轉化關系,且當X、Y、Z的物質的量相等時,存在焓變ΔH=ΔH1+ΔH2。滿足上述條件的X、Y可能是( )
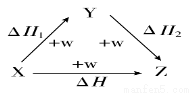
①C、CO ②S、SO2 ③Na、Na2O ④AlCl3、Al(OH)3⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3
A.①④⑤ B.①②③
C.①③④ D.①③④⑤⑥
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一下期末化學試卷(解析版) 題型:填空題
用氮化硅(Si3N4)陶瓷代替金屬制造發動機的耐熱部件,能大幅度提高發動機的熱效率。工業上用化學氣相沉積法制備氮化硅,其反應如下:
3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH <0
Si3N4(s)+12HCl(g) ΔH <0
完成下列填空:
(1)試寫出SiCl4的電子式_____________________________。
(2)在一定溫度下進行上述反應,若反應容器的容積為2 L,3 min后達到平衡,測得固體的物質的量增加了0.02mol,則H2的平均反應速率為____________________。
(3)上述反應達到平衡后,下列說法正確的是__________。
a.其他條件不變,壓強增大,平衡常數K減小
b.其他條件不變,溫度升高,平衡常數K減小
c.其他條件不變,增大Si3N4的物質的量平衡向左移動
d.其他條件不變,增大HCl的濃度平衡向左移動
(4)一定條件下,在恒容密閉的容器中,能表示上述反應達到化學平衡狀態的是_____。
a.3v逆(N2)= v正(H2)
b.v正(HCl)=4v正(SiCl4)
c.混合氣體密度保持不變
d.c(N2):c(H2):c(HCl)=1:3:6
e.單位時間內有n molN2消耗的同時有6 molHCl生成
(5)若平衡時H2和HCl的物質的量之比為m:n,保持其它條件不變,降低溫度后達到新的平衡時,H2和HCl的物質的量之比_______m:n(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一下期末化學試卷(解析版) 題型:選擇題
下面的烷烴是烯烴R和氫氣發生加成反應后的產物,則R可能的結構簡式有( )
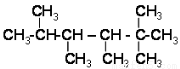
A.4種 B.5種 C.6種 D.7種
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一下期末化學試卷(解析版) 題型:選擇題
下列實驗方案不合理的是( )
A.鑒定蔗糖水解產物中有葡萄糖:在水解液中直接加入新制Cu(OH)2懸濁液
B.鑒別織物成分是真絲還是人造絲:灼燒
C.鑒定苯中有無碳碳雙鍵:加入高錳酸鉀酸性溶液
D.鑒別乙烯和乙烷:分別通入高錳酸鉀酸性溶液
查看答案和解析>>
科目:高中化學 來源:2015-2016學年福建省高二下學期期末化學試卷(解析版) 題型:選擇題
下列各組有機物,無論以何種比例混和,只要物質的量一定,完全燃燒時消耗氧氣的量為一恒量的是( )
A.C3H6和C3H8O B.C3H4和C2H6 C.C3H6O2和C3H8O D.C4H6和C3H6O
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高二下學期期末化學試卷(解析版) 題型:填空題
鐵及其化合物在生產、生活中有廣泛應用.請回答下列問題:
(一)高爐煉鐵過程中發生的主要反應為:
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知該反應在不同溫度下的平衡常數如下:
溫度/℃ 1000 1115 1300
平衡常數 4.0 3.7 3.5
(1)該反應的平衡常數表達式K= ;△H 0(填“>”、“<”或“=”).
(2)欲提高上述反應中CO的平衡轉化率,可采取的措施是 .
A.提高反應溫度
B.移出部分CO2
C.加入合適的催化劑
D.減小容器的容積
(3)在一個容積為10L的密閉容器中,1000℃時加入Fe、Fe2O3、CO、CO2各1.0mol,此時υ正 υ逆(填“>”、“<”或“=”).經過10min,在1000℃達到平衡,則該時間范圍內反應的平均反應速率υ(CO2)= .
(二)高鐵酸鉀(K2FeO4)是一種集氧化、吸附、絮凝于一體的新型多功能水處理劑.
(4)一定條件下Fe(OH)3與KClO在KOH溶液中反應可制得K2FeO4,其中反應的氧化劑是 ;生成0.5mol K2FeO4轉移電子的物質的量是 mol.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com