
分析 根據M=$\frac{m}{n}$可計算出混合氣體的平均摩爾質量;設出一氧化碳和二氧化碳的物質的量,然后根據總質量、總體積列式計算出二氧化碳的物質的量即可.
解答 解:標準狀況下17.92L混合氣體的物質的量為:$\frac{17.92L}{22.4L/mol}$=0.8mol,該混合氣體的平均摩爾質量為:$\frac{25.6g}{0.8mol}$=32g/mol,則此混合氣體的平均分子質量為32;
設該混合氣體中含有CO和CO2的物質的量分別為x、y,
則:28x+44y=25.6、x+y=0.8,
解得:x=0.6mol、y=0.2mol,
故答案為:32;0.2 mol.
點評 本題考查了物質的量的計算,題目難度不大,明確平均分子質量與平均摩爾質量的關系為解答關鍵,注意掌握物質的量與摩爾質量、氣體摩爾體積之間的關系,試題培養了學生的化學計算能力.


 考前必練系列答案
考前必練系列答案科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
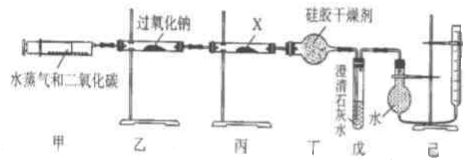
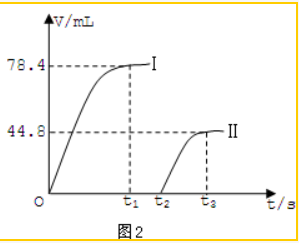
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2CO3、NaCl、AgNO3 | B. | Na2SO4、NaOH、HCl | ||
| C. | Na2SO4、NaNO3、NaOH | D. | Na2SO4、BaCl2、CuSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH 3CH 2CH2 CHO醛類 | B. | 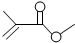 飽和酯類 飽和酯類 | ||
| C. | 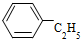 芳香烴 芳香烴 | D. | CH 3CH 2 COOH 羧酸類 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 人體內的鐵是以Fe2+ 和Fe3+的形式存在.正二價鐵離子易被吸收,給貧血者補充鐵時,應給予含Fe2+的亞鐵鹽,如硫酸亞鐵.服用維生素C,可使食物中的Fe3+還原成Fe2+,有利于人體吸收.
人體內的鐵是以Fe2+ 和Fe3+的形式存在.正二價鐵離子易被吸收,給貧血者補充鐵時,應給予含Fe2+的亞鐵鹽,如硫酸亞鐵.服用維生素C,可使食物中的Fe3+還原成Fe2+,有利于人體吸收.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 能說明NH3結合H+能力比H2O強:NH3+H3O+=NH4++H2O | |
| B. | 能說明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| C. | 能說明鹽酸是強酸:HCl+AgNO3=AgCl↓+HNO3 | |
| D. | 能說明CH3COOH是弱電解質:CH3COO-+H2O?CH3COOH+OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實驗 序號 | 碳酸鈣 狀態 | c(HCl) /mol•L-1 | 溶液溫度/℃ | 碳酸鈣消失 時間/s | |
| 反應前 | 反應后 | ||||
| 1 | 粒狀 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 粒狀 | 0.6 | 20 | 41 | 280 |
| 4 | 粒狀 | 0.8 | 20 | 40 | 200 |
| 5 | 粉末 | 0.8 | 20 | 40 | 30 |
| 6 | 粒狀 | 1.0 | 20 | 40 | 120 |
| 7 | 粒狀 | 1.0 | 30 | 50 | 40 |
| 8 | 粒狀 | 1.2 | 20 | 40 | 90 |
| 9 | 粒狀 | 1.2 | 25 | 45 | 40 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com