
| A. | 鎂與鹽酸反應放出氫氣 | B. | 高錳酸鉀分解 | ||
| C. | 氫氧化鈉與鹽酸的反應 | D. | Ba(OH)2•8H2O與NH4Cl反應 |
科目:高中化學 來源: 題型:選擇題
| A. | 2-甲基丁醛 CH3CH2 (CH3)CHCOH | B. | 硬酯酸甘油脂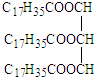 | ||
| C. | TNT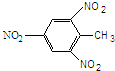 | D. | α-氨基丙酸 CH3CH(NH2)COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
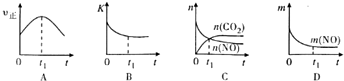
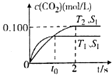 汽車尾氣凈化的主要原理為2NO(g)+2CO(g)$\stackrel{催化劑}{→}$2CO2+N2(g).在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示.據此判斷:
汽車尾氣凈化的主要原理為2NO(g)+2CO(g)$\stackrel{催化劑}{→}$2CO2+N2(g).在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示.據此判斷:| 容器編號 | 起始物質的量 | 平衡時物質的量 |
| Ⅰ | 2.0mol NO,2.0mol CO | 1.0mol CO2 |
| Ⅱ | 4.0mol NO,4.0mol CO |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
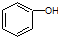 和
和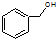
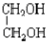 與
與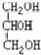
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2個 | B. | 3個 | C. | 4個 | D. | 5個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金不溶于任何溶液 | |
| B. | 銅、鋅在空氣中均能被氧化成對應的氧化物 | |
| C. | 銅鋅合金的熔點低于銅或鋅的熔點 | |
| D. | ${\;}_{29}^{63}$Cu的質子數和中子數之差為34 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氮氣的電子式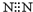 | B. | 乙烯的結構式:C2H4 | ||
| C. | 用電子式表示HCl的形成過程: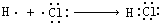 | D. | 乙醇的分子式:C2H5OH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com