
| 成分 | 成分的質量(g) | 摩爾質量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸鉀 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高錳酸鉀 | 0.316 | 158 |
| 硝酸銀 | 0.02 | 170 |
分析 (1)K+來自高錳酸鉀、硫酸鉀的電離,由n=$\frac{m}{M}$計算高錳酸鉀、硫酸鉀的物質的量及所含鉀離子的物質的量,依據C=$\frac{n}{V}$計算;
(2)根據配制溶液的實驗操作過程進行實驗步驟排序;
(3)分析操作對溶質的物質的量或對溶液的體積的影響,根據c=$\frac{n}{V}$分析判斷;
(4)①依據C=$\frac{1000ρω}{M}$計算濃硫酸的物質的量濃度,溶液稀釋過程中溶質的物質的量不變,據此計算需要濃硫酸體積;
②依據濃硫酸體積選擇合適規格量筒;
③依據濃硫酸稀釋的正確操作解答;
解答 解:(1)高錳酸鉀的物質的量為n(KMnO4)=$\frac{0.316g}{158g/mol}$=0.002mol;
硫酸鉀的物質的量為n(K2SO4)=$\frac{0.87g}{174g/mol}$=0.005mol,
n(K+)=n(KMnO4)+2n(K2SO4)=0.002mol+2×0.005mol=0.012mol,所以c(K+)=$\frac{0.012mol}{0.5L}$=0.024mol/L;
故答案為:0.024mol/L;
(2)操作步驟有計算、稱量、溶解、移液、洗滌移液、定容、搖勻等操作,一般用托盤天平稱量,用藥匙取用藥品,在燒杯中溶解(可用量筒量取水加入燒杯),并用玻璃棒攪拌,加速溶解.冷卻后轉移到500mL容量瓶中,并用玻璃棒引流,洗滌燒杯、玻璃棒2-3次,并將洗滌液移入容量瓶中,加水至液面距離刻度線1~2cm時,改用膠頭滴管滴加,最后定容顛倒搖勻,
所以需儀器有:托盤天平、燒杯、玻璃棒、藥匙外、500mL容量瓶、膠頭滴管、量筒(可用可不用)等,
故答案為:500mL容量瓶;膠頭滴管;
(3)A.定容時,俯視容量瓶刻度線,導致溶液體積偏小,溶液濃度偏高,故A不選;
B.容量瓶在使用前未干燥,里面有少量蒸餾水,對溶質的物質的量和溶液體積都不產生影響,溶液濃度不變,故B選;
C.容量瓶在使用前剛剛配制完一定物質的量濃度的NaCl溶液而未洗凈,氯化鈉能夠與硝酸銀反應,導致溶質的物質的量偏小,產生誤差,故C不選;
D.定容搖勻后發現液面低于容量瓶的刻度線,但未做任何處理,屬于正確操作,溶液濃度準確,故D選;
故選:BD;
(4)①質量分數為98%、密度為1.84g.cm-3的濃硫酸,物質的量濃度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,配制0.5mol/L 500mL的硫酸溶液設需要濃硫酸體積為V,則依據溶液稀釋過程中溶質的物質的量不變得:V×18.4mol/L=0.5mol/L×500mL,解得V=13.6mL;
故答案為:13.6;
②量取13.6mL溶液,應選擇15mL量筒;
故答案為:15;
③濃硫酸稀釋的正確操作為:將濃硫酸沿燒杯壁注入水中并用玻 璃棒不斷攪拌;
故答案為:將濃硫酸沿燒杯壁注入水中并用玻 璃棒不斷攪拌.
點評 本題考查了一定物質的量濃度溶液的配制,明確配制原理及操作步驟是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 當溫度一定時,不同的起始條件下可逆反應建立平衡狀態時,平衡常數和轉化率一定是定值 | |
| B. | 依據焓判據:NH4HCO3受熱分解可自發進行 | |
| C. | 大多數化學反應在一定條件下都有一定的限度 | |
| D. | FeCl3與KSCN反應達到平衡時,向其中滴加少量KCl溶液,則溶液顏色變深 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發操作時,應使混合物中的水分完全蒸干后,才能停止加熱 | |
| B. | 蒸餾操作時,應使溫度計水銀球靠近蒸餾燒瓶的支管口處 | |
| C. | 分液操作時,分液漏斗中下層液體從下口放出,上層液體從上口倒出 | |
| D. | 萃取操作時,應選擇有機萃取劑,萃取劑的密度不一定比水大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 200mL 2 mol/LMgCl2溶液 | B. | 1000mL 2.5 mol/L NaCl溶液 | ||
| C. | 300mL 5 mol/L KCl溶液 | D. | 250mL 1 mol/L FeCl3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 組別 | c(一元酸) | c(NaOH)/mol•L-1 | 混合溶液的pH |
| 甲 | c(HX)=0.1mol•L-1 | 0.1 | pH=x |
| 乙 | c(HY)=0.1mol•L-1 | 0.1 | pH=7 |
| 丙 | c(HZ)=0.1mol•L-1 | 0.1 | pH=9 |

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
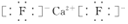 ;Y2與NaOH溶液反應的產物之一是OY2,該反應的離子方程式為2F2+2OH-=OF2↑+2F-+H2O.
;Y2與NaOH溶液反應的產物之一是OY2,該反應的離子方程式為2F2+2OH-=OF2↑+2F-+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
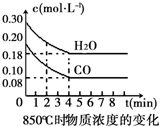 在一體積為10L的容器中,通入一定量的CO和H2O(g),在850℃時發生如下反應:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)濃度變化如圖
在一體積為10L的容器中,通入一定量的CO和H2O(g),在850℃時發生如下反應:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)濃度變化如圖| 時間(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0J062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com