
【題目】某化工廠以軟錳礦、閃鋅礦(除主要成分為MnO2、ZnS外還含有少量的FeS、CuS、Al2O3等物質)為原料制取Zn和MnO2.
(1)在一定條件下,將這兩種礦粉在硫酸溶液中相互作用,配平如下的化學方程式:MnO2+FeS+H2SO4=MnSO4+Fe2(SO4)3+S+H2O_____
(2)將所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按如圖甲的工業流程進行操作處理得溶液(IV),電解溶液(IV)即得MnO2和Zn.
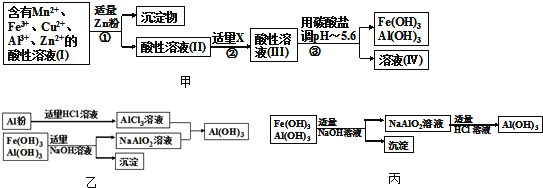
a、操作①中加Zn粉后發生反應的離子方程式為 ______ .
b、操作②中加入適量X的作用是什么 ______ ;X的首選物的化學式是: ______ .
c、操作③中所加碳酸鹽的化學式是 ______ .
(3)為了從上述流程中產生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工廠設計了如圖乙的有關流程圖.
a、AlCl3溶液和NaAlO2溶液反應生成Al(OH)3的離子方程式為 ______ .若總共得到nmol Al(OH)3,則消耗的NaOH和HCl的理論量(mol)分別為 ______ 、 ______ .
b、若使用如圖丙流程回收處理,請比較兩個流程消耗酸堿的用量? ______ .
【答案】3MnO2+ 2FeS +6 H2SO4 = 3MnSO4 + Fe2(SO4)3+2S+6H2O Zn+2Fe3+=Zn2++2Fe2+,Zn + Cu2+ =Zn2+ + Cu 將Fe2+氧化成Fe3+ MnO2 MnCO3或ZnCO3 Al3++3AlO2-+6H2O=4 Al(OH)3↓ ![]()
![]() 按丙流程,則得到同樣nmolAl(OH)3,消耗的NaOH、HCl的理論量均為nmol,大于乙流程的消耗量,相對而言,乙流程更符合節約的原則。
按丙流程,則得到同樣nmolAl(OH)3,消耗的NaOH、HCl的理論量均為nmol,大于乙流程的消耗量,相對而言,乙流程更符合節約的原則。
【解析】
⑴根據氧化還原反應配平方程式。
⑵加入鋅,先是鐵離子反應,再是銅離子反應,為了除掉鐵元素,用氧化劑氧化亞鐵離子變為鐵離子,再通過調節溶液的pH值來除掉鐵離子,一般用碳酸錳等。
⑶得到nmol氫氧化鋁,根據化學方程式求出需要的鋁離子和偏鋁酸根離子的物質的量,再根據方程式計算需要消耗得鹽酸和氫氧化鈉的物質的量,分析乙、丙兩種流程得到的相同的氫氧化鋁消耗的鹽酸和氫氧化鈉的量來得出哪種方式更優。
⑴在一定條件下,將這兩種礦粉在硫酸溶液中相互作用,配平如下的化學方程式:MnO2中Mn的化合價降低2價,1molMnO2得到2mol電子,FeS中鐵和硫的化合價都升高,1molFeS失去3mol電子,因此轉移電子數為6,在FeS前面配系數2,MnO2配系數為3,再根據質量守恒配平其他物質的系數:3MnO2+ 2FeS +6H2SO4 = 3MnSO4 + Fe2(SO4)3+2S+6H2O,故答案為:3MnO2+ 2FeS +6H2SO4 = 3MnSO4 + Fe2(SO4)3+2S+6H2O。
⑵a、操作①中加Zn粉后發生反應的離子方程式為Zn+2Fe3+=Zn2++2Fe2+,Zn + Cu2+ =Zn2+ + Cu,故答案為:Zn+2Fe3+=Zn2++2Fe2+,Zn + Cu2+ =Zn2+ + Cu。
b、后面要將鐵元素除掉,因此要先將亞鐵離子氧化,操作②中加入適量X的作用是將Fe2+氧化成Fe3+,為了不引入新的雜質,因此X的首選物的化學式是:MnO2,故答案為:將Fe2+氧化成Fe3+,MnO2。
c、不引入新的雜質且要調節溶液的pH值,則操作③中所加碳酸鹽的化學式是MnCO3或ZnCO3或MnCO3,故答案為:MnCO3或ZnCO33。
⑶a、流程乙中發生反應的離子方程式為:2Al+6H+=2Al3++3H2↑,Al(OH)3+OH-=AlO2-+2H2O,Al3++3AlO2-+6H2O=4 Al(OH)3↓,若總共得到n mol Al(OH)3,根據方程式,需要AlO2-的物質的量為![]() mol,則需要NaOH的物質的量為
mol,則需要NaOH的物質的量為![]() mol,Al3+的物質的量為
mol,Al3+的物質的量為![]() mol,消耗鹽酸的物質的量為
mol,消耗鹽酸的物質的量為![]() mol,因此消耗的NaOH和HCl的理論量(mol)分別為
mol,因此消耗的NaOH和HCl的理論量(mol)分別為![]() mol、
mol、![]() mol,故答案為:Al3++3AlO2-+6H2O=4 Al(OH)3↓;
mol,故答案為:Al3++3AlO2-+6H2O=4 Al(OH)3↓;![]() ;
;![]() 。
。
b、若使用如圖丙流程回收處理,發生反應的離子方程式為:Al(OH)3+OH-=AlO2-+2H2O,AlO2-+H++H2O=Al(OH)3↓,生成n mol Al(OH)3,需要n mol鹽酸和n mol偏鋁酸根,生成n mol偏鋁酸根需要n mol氫氧化鋁和n mol氫氧化鈉,因此按丙流程,則得到同樣nmolAl(OH)3,消耗的NaOH、HCl的理論量分別為nmol,大于乙流程的消耗量,相對而言,乙流程更符合節約的原則,故答案為:按丙流程,則得到同樣nmolAl(OH)3,消耗的NaOH、HCl的理論量分別為nmol,大于乙流程的消耗量,相對而言,乙流程更符合節約的原則。


科目:高中化學 來源: 題型:
【題目】鐵有δ、γ、α三種同素異形體,三種晶體在不同溫度下能發生轉化。
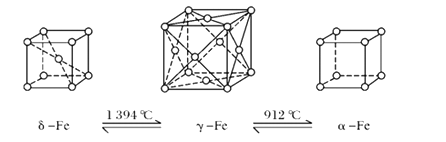
(1)δ、γ、α三種晶體晶胞中鐵原子的配位數之比為_________。
(2)若δ-Fe晶胞邊長為acm,α-Fe晶胞邊長為bcm,則兩種晶胞空間利用率之比為________(用a、b表示)
(3)若Fe原子半徑為r pm,NA表示阿伏加德羅常數的值,則γ-Fe單質的密度為_______g/cm3(用含r的表達式表示、列出算式即可)
(4)三氯化鐵在常溫下為固體,熔點為282℃,沸點為315℃,在300℃以上升華,易溶于水,也易溶于乙醚、丙酮等有機溶劑。據此判斷三氯化鐵的晶體類型為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國學者在水煤氣變換[CO(g)+H2O(g)=CO2(g)+H2(g) ΔH]中突破了低溫下高轉化率與高反應速率不能兼得的難題,該過程是基于雙功能催化劑(能吸附不同粒子)催化實現的。反應過程示意圖如下:
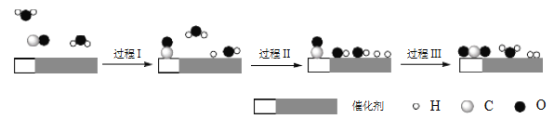
下列說法正確的是
A. 過程Ⅰ、過程Ⅲ均為放熱過程
B. 過程Ⅲ生成了具有極性共價鍵的H2、CO2
C. 使用催化劑降低了水煤氣變換反應的ΔH
D. 圖示過程中的H2O均參與了反應過程
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.在實驗室利用下列裝置,可制備某些氣體并驗證其化學性質。

完成下列表格:
序號 | 氣體 | 裝置連接順序(填字母) | 制備反應的化學方程式 |
(1) | 乙烯 | B→D→E | ___ |
(2) | 乙炔 | ___ | ___ |
(3)D裝置中氫氧化鈉溶液的作用___。
Ⅱ.工業上用乙烯和氯氣為原料,經下列各步合成聚氯乙烯(PVC):
乙烯![]() 甲
甲![]() 乙
乙![]() PVC
PVC
(4)甲的結構簡式是___;
(5)反應③的化學方程式是__。
(6)下列說法正確的是___。
A.乙烯可以作為植物生長調節劑
B.PVC不能使酸性高錳酸鉀溶液褪色
C.PVC中的官能團是碳碳雙鍵和氯原子
查看答案和解析>>
科目:高中化學 來源: 題型:
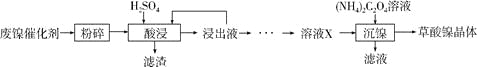
【題目】草酸鎳晶體(NiC2O4·2H2O)可用于制鎳催化劑,硫酸鎳晶體(NiSO4·7H2O)主要用于電鍍工業。某小組用廢鎳催化劑(成分為Al2O3、Ni、Fe、SiO2、CaO等)制備草酸鎳晶體的部分實驗流程如下:
已知:①相關金屬離子生成氫氧化物沉淀的pH如下表(開始沉淀的pH按金屬離子濃度為1.0mol·L-1計算)。
金屬離子 | 開始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Al3+ | 3.0 | 5.0 |
Ni2+ | 6.7 | 9.5 |
②Ksp(CaF2)=1.46×10-10,Ksp(CaC2O4)=2.34×10-9。
(1)“粉碎”的目的是____________。
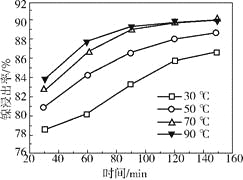
(2)保持其他條件相同,在不同溫度下對廢鎳催化劑進行“酸浸”,鎳浸出率隨時間變化如右圖。“酸浸”的適宜溫度與時間分別為_________(填字母)。
a.30℃、30min
b.90℃、150min
c.70℃、120min
d.90℃、120min
(3)證明“沉鎳”工序中Ni2+已經沉淀完全的實驗步驟及現象是___________。
(4)將“沉鎳”工序得到的混合物過濾,所得固體用乙醇洗滌、110 ℃下烘干,得草酸鎳晶體。
①用乙醇洗滌的目的是_________________。
②烘干溫度不超過110℃的原因是_________________。
(5)由流程中的“浸出液”制備硫酸鎳晶體的相關實驗步驟如下:
第1步:取“浸出液”,___,充分反應后過濾,以除去鐵、鋁元素;
第2步:向所得濾液中加入適量NH4F溶液,充分反應后過濾,得“溶液X”;
第3步:___,充分反應后過濾;
第4步:濾渣用稍過量硫酸充分溶解后,蒸發濃縮、冷卻結晶、過濾、洗滌、干燥,得硫酸鎳晶體。
①請補充完整相關實驗步驟(可選試劑:H2SO4溶液、NaOH溶液、HNO3溶液、H2O2溶液)。
②第2步中加入適量NH4F溶液的作用是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以廢舊鉛酸電池中的含鉛廢料(Pb、PbO、PbO2、PbSO4及炭黑等)為原料,制備粗鉛,實現鉛的再生利用。其工作流程如下圖所示:
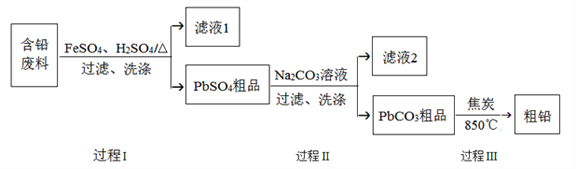
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
(1)過程Ⅰ中,在Fe2+催化下,Pb和PbO2反應生成PbSO4的化學方程式是__________。
(2)過程Ⅰ中,Fe2+催化過程可表示為:
i:2Fe2++ PbO2+4H++SO42-![]() 2Fe3++PbSO4+2H2O
2Fe3++PbSO4+2H2O
ii: ……
①寫出ii的離子方程式:________________。
②下列實驗方案可證實上述催化過程。將實驗方案補充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液幾乎無色,再加入少量PbO2,溶液變紅。
b.___________。
(3)過程Ⅱ的目的是脫硫。若濾液2中c(SO42-)=1.6mol/L,c(CO32-)=0.1mol/L,則PbCO3中____(填“是”或“否”)混有PbSO4。
(4)鈉離子交換膜固相電解法是從含鉛廢料中提取鉛的一種新工藝,其裝置如圖所示。將含鉛廢料投入陰極室,含鉛廢料中的PbSO4與NaOH溶液發 生反應:PbSO4+3OH-=HPbO2-+SO42-+H2O。
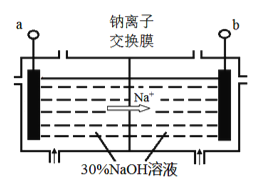
①a與外接電源的________極相連。
②電解過程中,PbO2、PbO、HPbO2-在陰極放電,其中PbO2放電的電極反應式為___________。
③與傳統無膜固相電解法相比,使用鈉離子交換膜可以 提高Pb元素的利用率,原因是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
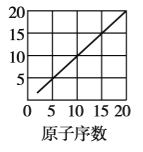
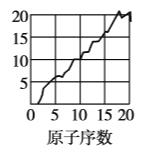
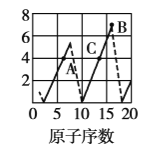
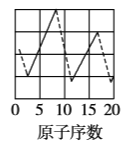
【題目】下圖是依據各種元素(原子)的性質與原子序數(1~20)的關系而繪制出來的,各圖的縱軸可能代表下列某一性質:核電荷數,中子數、最高正化合價、原子半徑、得電子能力,A、B、C分別代表三種元素.(注意:圖3中原子序數為8、9的元素和圖4中原子序數為2、10、18的元素在縱軸上沒有對應的數值.)
請回答下列問題:
(1)圖2的縱軸代表的性質是______,圖4的縱軸代表的性質是______.
(2)A元素的最低負化合價為______.
(3)B、C兩種元素形成的化合物中,C顯最高正化合價而B顯最低負化合價,該化合物的化學式為______.
(4)1~20號元素中,原子(稀有氣體元素原子除外)半徑最大的是__(填元素符號)
(5)寫出B的單質與NaOH溶液反應的離子方程式:____________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 、
、![]() 為核電荷數小于18的兩種元素,元素
為核電荷數小于18的兩種元素,元素![]() 的原子的最外層電子數是次外層電子數的一半,元素
的原子的最外層電子數是次外層電子數的一半,元素![]() 的原子的最外層電子數與最內層電子數之和等于次外層電子數。下列有關敘述正確的是
的原子的最外層電子數與最內層電子數之和等于次外層電子數。下列有關敘述正確的是
A.![]() 、
、![]() 一定是非金屬元素B.
一定是非金屬元素B.![]() 的最外層電子數比
的最外層電子數比![]() 的少
的少
C.![]() 的單質在化學反應中只能作還原劑D.
的單質在化學反應中只能作還原劑D.![]() 與
與![]() 的最外層電子數相等
的最外層電子數相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在堿的作用下,兩分子酯縮合形成β-羰基酯,同時失去一分子醇,該反應稱克菜森(R·L·Claisen)酯縮合反應,其反應機理如下:
2RCH2COOC2H5 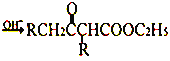 +C2H5OH 利用Claisen反應制備化合物I的一種合成路線如下:
+C2H5OH 利用Claisen反應制備化合物I的一種合成路線如下:
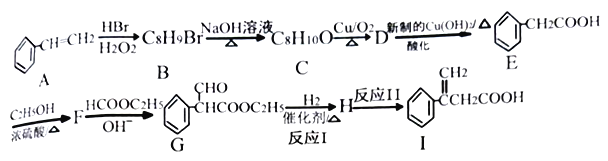
回答下列問題:
(1)E的名稱為_______,F的結構簡式為_______。
(2)I中官能團的名稱是_______,反應I的反應類型是_______。
(3)F→G反應的化學方程式為_______。
(4)滿足下列條件E的同分異構體有_____種。
①含有苯環,能發生水解反應 ②分子結構中含有一個甲基
其中分子結構中只有一個側鏈的有機物結構簡式為______、_______。
(5)乙酰乙酸乙酯(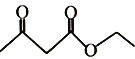 )是一種重要的有機合成原料,寫出由乙醇制備乙酰乙酸乙酯的合成路線________(無機試劑任選)。
)是一種重要的有機合成原料,寫出由乙醇制備乙酰乙酸乙酯的合成路線________(無機試劑任選)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com