
【題目】下列關于電子式的表述正確的是( )
A.HClO的電子式為
B.SCl2的電子式為
C.用電子式表示HCl的形成過程為
![]()
D.已知SCN-每個原子都達到8電子結構,則其電子式為
 南大教輔搶先起跑暑假銜接教程南京大學出版社系列答案
南大教輔搶先起跑暑假銜接教程南京大學出版社系列答案科目:高中化學 來源: 題型:
【題目】一種基于酸性燃料電池原理設計的酒精檢測儀,負極上的反應為CH3CH2OH-4e-+H2O![]() CH3COOH+4H+。下列有關說法正確的是 ( )
CH3COOH+4H+。下列有關說法正確的是 ( )
A. 電池反應的化學方程式為CH3CH2OH+O2![]() CH3COOH+H2O
CH3COOH+H2O
B. 若有0.4 mol電子轉移,則在標準狀況下消耗4.48 L氧氣
C. 檢測時,電解質溶液中的H+向負極移動
D. 正極上發生的反應為O2+4e-+2H2O![]() 4OH-
4OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組同學用 NaHCO3和KHCO3組成的某均勻混合物進行實驗,測得如下數據(鹽酸的物質的量濃度相等)
實驗序號 | I | II | III |
鹽酸體積(mL) | 100.0 | 100.0 | 100.0 |
樣品質量/g | 9.2 | 15.7 | 27.6 |
CO2體積/L (標準狀況) | 2.24 | 3.36 | 3.36 |
(1)該鹽酸的物質的量濃度為______mol·Lˉ1
(2)使鹽酸恰好完全反應,所需要的樣品質量為______g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素 Q、R、T、W 在元素周期表中的位置如圖所示,其中 T 所處的周期數與主族序數相等。
![]()
(1)W 在周期表中的位置是_______,Q、R、T 三種元素原子半徑由大到小的順序為_______________________(用元素符號表示),Q 的最高價氧化物的化學式為________________,
(2)元素的原子得電子 能力:Q________________W(填“強于”或“弱于”)。
(3)原子序數比 R 多 1 的元素有一種氫化物能分解為它的另一種氫化物,該反應的化學方程式為______________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期金屬元素甲~戊在元素周期表中的相對位置如右表所示,下面判斷正確的是
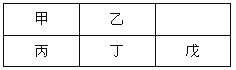
A. 原子半徑:丙<丁<戊B. 金屬性:甲>丙
C. 氫氧化物堿性:丙>丁>戊D. 最外層電子數:甲>乙
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、Q、R為原子序數依次增大的短周期主族元素,其原子半徑與最外層電子數的關系如下圖所示。R原子最外層電子數Q原子最外層電子數的4倍,Q的簡單離子核外電子排布與Z2-相同。下列相關敘述不正確的是

A. 化合物![]() 中含有離子鍵
中含有離子鍵
B. 五種元素中Q的金屬性最強
C. 氣態氫化物的穩定性:![]()
D. 最高價氧化物對應的水化物酸性:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】主要用于高分子膠囊和印刷油墨的粘合劑的甲基兩烯酸縮水油酯GMA(即:![]() )的合成路線如下(部分反應所需試劑和條件已略去):
)的合成路線如下(部分反應所需試劑和條件已略去):

已知:
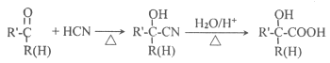
請按要求回答下列問題:
(1)GMA的分子式______________________;B中的官能團名稱:______________________;甘油的系統命名:______________________。
(2)驗證D中所含官能團各類的實驗設計中,所需試劑有______________________。
(3)寫出下列反應的化學方程式:反應⑤:____________________。反應⑧:______________________。
(4)M是H的同分異構體。M有多種同分異構體,寫出滿足下述所有條件的M的所有可能的結構:____________________________。
①能發生銀鏡反應 ②能使溴的四氯化碳溶液褪色 ③能在一定條件下水解
(5)已知: { 2 }![]()
![]()
![]() 。參照上述合成路線并結合此信息,以丙烯為原料,完善下列合成有機物C的路線流程圖:丙烯
。參照上述合成路線并結合此信息,以丙烯為原料,完善下列合成有機物C的路線流程圖:丙烯![]() Br
Br![]() ________________________。
________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,將![]() 溶液分別滴加到濃度均為
溶液分別滴加到濃度均為![]() 的
的![]() 溶液中,所得的沉淀溶解平衡曲線如圖所示(
溶液中,所得的沉淀溶解平衡曲線如圖所示(![]() 用
用![]() 表示,不考慮
表示,不考慮![]() 的水解)。下列敘述正確的是( )。
的水解)。下列敘述正確的是( )。

A. ![]() 的數量級為
的數量級為![]()
B. ![]() 點對應的
點對應的![]() 溶液為不飽和溶液
溶液為不飽和溶液
C. 所用![]() 溶液的濃度為
溶液的濃度為![]()
D. ![]() 平衡常數為
平衡常數為![]() ,反應趨于完全
,反應趨于完全
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】產自我國西北某鹽湖的“塊堿”是一種Na2CO3和NaCl的混合物。可通過以下方法對塊堿樣品的組成和含量進行分析測定。
Ⅰ.定性測定NaCl的存在:
(1)取樣品少許溶于水,加入足量稀硝酸充分反應后再滴加_________________溶液,能觀察到有_______________________產生,說明塊堿中含有NaCl。
Ⅱ.定量測定Na2CO3的含量:
準確稱量w g樣品置于如下裝置中,向其中加入足量稀硫酸,通過測定生成氣體的體積來求算Na2CO3的含量。請回答下列相關問題:

(2)測定裝置中,導管a的作用是___________________________________________。
(3)為提高測定的準確度,溶液b最宜選用___________________________________。
①飽和食鹽水 ②飽和NaHCO3溶液 ③澄清石灰水 ④酸性KMnO4溶液
(4)若根據所取樣品的質量估計反應時產生的氣體體積最多在30mL左右,則產生氣體前對量氣裝置讀數時,裝置內的裝液量和液面調節最為合理的是_______________________(填虛線框中對應這的字母編號)。
(5)用你以上所選出的最為合理的讀數為起點,若終點讀數為17.60mL,則反應所產生的氣體的測定體積為_____________mL。若實驗溫度下的氣體摩爾體積為VmL.mol-1,由此可得出樣品中Na2CO3的含量表達式為: __________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com