
【題目】從定性分析到定量研究是高中生化學學習的重要發展歷程。請你根據所學知識對以下化學問題進行定量分析。
(1)高錳酸鉀是一種典型的強氧化劑。在用KMnO4酸性溶液處理CuS的混合物時,發生的反應如下:MnO4-+ CuS + H+=Cu2+ + SO2↑ + Mn2++ H2O,請配平離子方程式并用單線橋法標出該反應中電子轉移的方向和數目:___。
(2)K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O氧化劑是__,氧化產物與還原產物的物質的量之比為___。
(3)Cl2是一種有毒氣體,如果泄漏會造成嚴重的環境污染,化工廠可用濃氨水來檢驗Cl2是否泄漏,有關反應的化學方程式為:3Cl2(氣)+8NH3(氣)=6NH4Cl(固)+N2(氣),若反應中消耗Cl2 1.5mol,則被氧化的NH3在標準狀況下的體積為__ L。
【答案】![]() K2Cr2O7 3:2 22.4
K2Cr2O7 3:2 22.4
【解析】
(1)依據氧化還原反應電子守恒、電荷守恒、原子守恒配平離子方程式;
(2)依據電子守恒計算;
(3)依據電子守恒計算。
(1)反應②中Mn元素化合價降低,從+7價降低為+2價,1mol MnO4-得到5mol電子,CuS中硫元素化合價從-2價升高到+4價,1mol CuS失去6mol電子,則二者物質的量之比為6:5,依據電荷守恒,原子守恒配平方程式是6MnO4-+5CuS +28 H+=5Cu2++5SO2↑+6Mn2++14H2O,轉移電子數目為5×6=30,可表示為 ,故答案為:
,故答案為:![]() ;
;
(2)鉻元素的化合價降低,故氧化劑是K2Cr2O7,設氧化產物的物質的量是x mol,還原產物的物質的量是y mol,依據電子守恒得x mol×2=y mol×3,解得:x:y=3:2;
(3)設被氧化的NH3在標準狀況下的體積為x L,依據電子守恒得:1.5mol×2×1=x÷22.4L/mol×3,解得:x=22.4,故答案為:22.4。


科目:高中化學 來源: 題型:
【題目】以甲醛和苯酚為主要原料,經下列轉化可合成酚醛樹脂和重要的有機合成中間體D(部分反應條件和產物已略去)
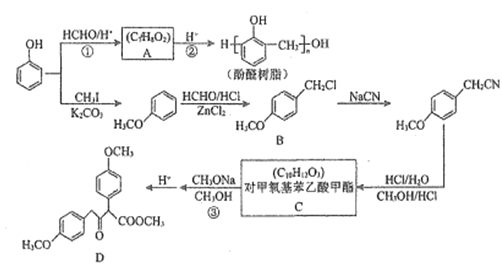
已知:R1CH2COOCH2+R2COOCH3![]() CH3OH+
CH3OH+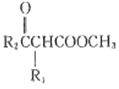
請回答下列問題:
(1)反應①的反應類型為___________;A的化學名稱為___________。
(2)C中所含官能團的名稱為___________;D的分子式為___________。
(3)反應②的化學方程式為______________________。
(4)A的下列性質中,能反映支鏈對苯環結構產生影響的是___________(填字母)。
a.能與氫氧化鈉溶液反應
b.能使酸性高錳酸鉀溶液褪色
c.向稀溶液中加入濃溴水后,產生沉淀
(5)芳香化合物E(C8H10O2)與B的水解產物互為同分異構體,1molE可與2 mol NaOH反應,其核磁共振氫譜中有3組峰且峰面積之比為3:1:1,則E有___________種可能的結構(不考慮立體異構)。
(6)以CH3OH和CH3ONa為原料(其他試劑任選),設計制備CH3COCH2 COOCH3的合成路線:CH3OH![]() ______。
______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某有機物結構如圖,下列說法中正確的是
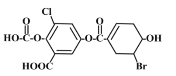
A. 該物質的化學式為C15H12O8BrCl
B. 該物質能與FeCl3溶液發生顯色反應
C. 1mol該物質最多能與3mol溴水發生加成反應
D. 一定條件下,1mol該物質最多能與7molNaOH反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將0.2mol MnO2和50mL 12mol·L-1鹽酸混合后緩慢加熱,反應完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀,物質的量為x mol(不考慮鹽酸的揮發),則x的取值范圍是
A.x=0.3B.x<0.3C.0.3<x<0.6D.以上結論都不對
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同學設計如圖所示的實驗裝置,通過測量反應產生的CO2和H2O的質量,來確定該混合物中各組分的質量分數。
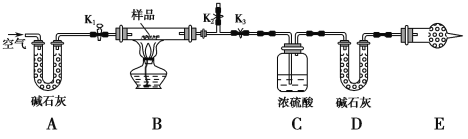
(1) 實驗步驟:
① 按圖(夾持儀器未畫出)組裝好實驗裝置后,首先進行的操作是____________________。
② 稱取樣品,并將其放入硬質玻璃管中;稱量裝濃硫酸的洗氣瓶C的質量和裝堿石灰的U形管D的質量。
③打開活塞K1、K2,關閉K3,緩緩鼓入空氣數分鐘,其目的是___________________。
④關閉活塞K1、K2,打開K3,點燃酒精燈加熱至不再產生氣體。裝置B中發生反應的化學方程式為___________________________、______________________________。
⑤ 打開活塞K1,緩緩鼓入空氣數分鐘,然后拆下裝置,再次稱量洗氣瓶C的質量和U形管D的質量。
(2) 關于該實驗方案,請回答下列問題。
① E處干燥管中盛放的藥品是________,其作用是______________________________________,如果實驗中沒有該裝置,則可能導致測量結果NaHCO3的質量分數________(填“偏大”“偏小”或“無影響”)。
② 若樣品質量為w g,反應后C、D裝置增加的質量分別為m1 g、m2 g,則混合物中Na2CO3·10H2O的質量分數為__________________(用含w、m1、m2的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化學中化合物的結構可用鍵線式表示,如CH2=CHCH2Br可表示為![]() 。環之間共用一個碳原子的化合物稱為螺環化合物,螺[2.2]戊烷(
。環之間共用一個碳原子的化合物稱為螺環化合物,螺[2.2]戊烷(![]() )是最簡單的一種。下列關于該化合物的說法錯誤的是( )
)是最簡單的一種。下列關于該化合物的說法錯誤的是( )
A. ![]() 與環戊烯互為同分異構體
與環戊烯互為同分異構體
B. ![]() 二氯代物超過兩種
二氯代物超過兩種
C. ![]() 所有碳原子均處同一平面
所有碳原子均處同一平面
D. ![]() 的一氯代物有1種,所有碳原子均處同一平面
的一氯代物有1種,所有碳原子均處同一平面
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于同分異構體(不考慮立體異構)的數目判斷正確的是( )
選項 | A | B | C | D |
分子式(或結構簡式) | C5H10O2 | C5H10 |
| C7H16 |
已知條件 | 能與碳酸氫鈉反應 | 能使溴 水褪色 | 一氯代物 | 分子中含 有3個甲基 |
同分異構體數目 | 4 | 3 | 4 | 5 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:
![]()
從A出發發生圖示中的一系列反應,其中B和C按1:2反應生成Z。F和E按1:2反應生成W,F的核磁共振氫譜只有兩種峰,W和Z互為同分異構體。
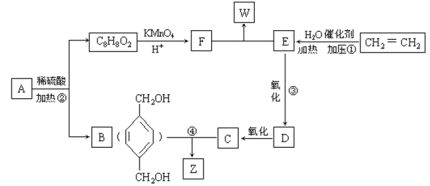
回答下列問題:
(1)寫出反應類型:①_____________________,②______________________________。
(2)寫出下列反應的化學方程式:
③_____________________________________________________;
④_____________________________________________________。
(3)與B互為同分異構體,屬于酚類且苯環上只有兩個取代基的化合物有___種(不包括對映異構體)。
(4)A的結構簡式可能為_________________________________。
(5)已知酯與醇有如下反應:
RCOOR′+R″OH![]() RCOOR″+R′OH(R、R′、R″代表烴基)
RCOOR″+R′OH(R、R′、R″代表烴基)
B與W在上述條件下可形成高分子化合物Q,請寫出B與W生成Q的化學方程式________。
(6)同一碳原子上連兩個羥基時結構不穩定,易脫水生成醛或酮:
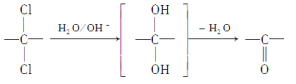
根據已有知識并結合相關信息,寫出以對二甲苯為原料(其他無機試劑任選)制備![]() 的合成路線。__________________
的合成路線。__________________
合成路線示意圖,如: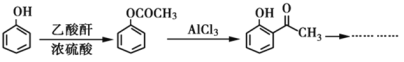
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列四種裝置中,溶液的體積均為250mL,開始時電解質溶液的濃度均為0.10mol/L,工作一段時間后,測得導線上均通過0.02mol電子,若不考慮溶液體積的變化,則下列敘述正確的是( )
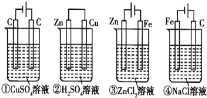
A. 工作一段時間后溶液的濃度:①=②=③=④
B. 工作一段時間后溶液的pH:④>③>①>②
C. 產生氣體的總體積:④>③>①>②
D. 電極上析出固體的質量:①>②>③>④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com