
(16分)(1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理上可以設計成原電池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液為電解質溶液,依據所選反應設計一個原電池,其負極反應的電極反應式為 。
(3)電解原理在化學工業中有著廣泛的應用。現將你設計的原電池通過導線與下圖中電解池相連,其中,a為電解液,X和Y是兩塊電極板,則:
① 若X和Y均為惰性電極,a為CuSO4溶液,則陽極的電極反應式為 ,電解時的化學反應方程式為 ,通過一段時間后,向所得溶液中加入0.2molCuO粉末,恰好恢復到電解前的濃度和pH,則電解過程中轉移的電子的物質的量為 。
②若X、Y依次為銅和鐵,a仍為CuSO4溶液,且反應過程中未生成Fe3+,,則Y極的電極反應式為
③若用此裝置電解精煉銅, 做陽極,電解液CuSO4的濃度 (填“增大”、“減小”或“不變”)。
④若用此裝置在鐵制品上鍍銅,鐵制品做 ,電鍍液的濃度 (填“增大”、“減小”或“不變”)。
⑴C ⑵H2+2OH--2e-=2H2O ⑶①4OH--4e-=2H2O+O2↑
通電
2CuSO4+2H2O====2Cu+O2↑+2H2SO4 0.4mol
Fe-2e-=Fe2+ ③粗銅 減小 ④陰極 不變
解析(1)原電池的組成條件包括:“兩級、一線、一液、一回路、一個自發的氧化還原反應”,再有原電池的反應通常是放熱反應的信息選C
(2)氫氧燃料電池,堿性電解質系統的負極反應為H2+2OH--2e-=2H2O
(3)電解池裝置圖可知Y是陽極,X是陰極。
① 若X和Y均為惰性電極,a為CuSO4溶液,則陽極的電極反應式為4OH--4e-=2H2O+O2↑
通電
2CuSO4+2H2O====2Cu+O2↑+2H2SO4 加入0.2molCuO粉末,恰好恢復到電解前的濃度和pH,說明電解中陰極銅離子得0.4mol電子。
②若X、Y依次為銅和鐵,a仍為CuSO4溶液,且反應過程中未生成Fe3+, 鐵做陽極,鐵失去電子Fe-2e-=Fe2+
③若用此裝置電解精煉銅,粗銅作陽極,精銅作陰極,硫酸銅溶液做電解質,電精煉過程陽極粗銅中金屬性比同強的金屬都失去電子,溶液中的銅離子在陰極得到電子,故電解質溶液的濃度減小。
④若用此裝置在鐵制品上鍍銅,鍍層金屬做陽極,鍍件做陰極,含有鍍層金屬的鹽溶液做電解質,電鍍過程電解質濃度不變。


科目:高中化學 來源: 題型:
 (1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理上可以設計成原電池的是
(1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理上可以設計成原電池的是
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
(10分)(1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在可以設計成原電池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液為電解質溶液,依據所選反應設計一個原電池,其負極反應的電極反應式為 。
(3)電解原理在化學工業中有著廣泛的應用。現將你設計的原電池通過導線與下圖中
電解池相連,其中,a為電解液,X和Y是兩塊電極板,則:
① 若X和Y均為惰性電極,a為CuSO4溶液,
則陽極的電極反應式為 ,電解時的化學反應方程式為 ,通過一段時間后,向所得溶液中加入0.2molCuO粉末,恰好恢復到電解前的濃度和pH,則電解過程中轉移的電子的物質的量為 。
②若X、Y分別為鐵和銅,a仍為CuSO4溶液,則Y極的電極反應式為
③若用此裝置電解精煉銅, 做陽極,電解液CuSO4的濃度 (填“增大”、“減小”或“不變”)。
④若用此裝置在鐵制品上鍍銅,鐵制品做 ,電鍍液的濃度 (填“增大”、“減小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
(20分)(1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理論上可以設計成原電池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液為電解質溶液,依據所選反應設計一個原電池,其負極反應的電極反應式為 。
(3)電解原理在化學工業中有著廣泛的應用。
現將你設計的原電池通過導線與下圖中電解池相連,其中,a為電解液,X和Y是兩塊電極板,則:

① 若X和Y均為惰性電極,a為CuSO4溶液
則陽極的電極反應式為 ,電解時的化學反應方程式為 ,通過一段時間后,向所得溶液中加入0.2molCuO粉末,恰好恢復到電解前的濃度和pH,則電解過程中轉移的電子的物質的量為 。
②若X、Y分別為鐵和銅,a仍為CuSO4溶液,則Y極的電極反應式為
③若用此裝置電解精煉銅, 做陽極,電解液CuSO4的濃度 (填“增大”、“減小”或“不變”)。
④若用此裝置在鐵制品上鍍銅,鐵制品做 ,電鍍液的濃度 (填“增大”、“減小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源:2013屆河南省宜陽一高高二3月月考化學試卷 題型:填空題
(10分)(1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在可以設計成原電池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液為電解質溶液,依據所選反應設計一個原電池,其負極反應的電極反應式為 。
(3)電解原理在化學工業中有著廣泛的應用。現將你設計的原電池通過導線與下圖中
電解池相連,其中,a為電解液,X和Y是兩塊電極板,則:
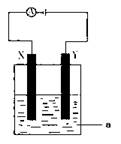
① 若X和Y均為惰性電極,a為CuSO4溶液,
則陽極的電極反應式為 ,電解時的化學反應方程式為 ,通過一段時間后,向所得溶液中加入0.2molCuO粉末,恰好恢復到電解前的濃度和pH,則電解過程中轉移的電子的物質的量為 。
②若X、Y分別為鐵和銅,a仍為CuSO4溶液,則Y極的電極反應式為
③若用此裝置電解精煉銅, 做陽極,電解液CuSO4的濃度 (填“增大”、“減小”或“不變”)。
④若用此裝置在鐵制品上鍍銅,鐵制品做 ,電鍍液的濃度 (填“增大”、“減小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源:2013屆山東省高二上學期模塊考試化學試卷 題型:填空題
(20分)(1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理論上可以設計成原電池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液為電解質溶液,依據所選反應設計一個原電池,其負極反應的電極反應式為 。
(3)電解原理在化學工業中有著廣泛的應用。
現將你設計的原電池通過導線與下圖中
電解池相連,其中,a為電解液,X和Y是兩塊電極板,則:
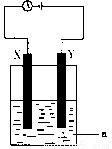
① 若X和Y均為惰性電極,a為CuSO4溶液
則陽極的電極反應式為 ,電解時的化學反應方程式為 ,通過一段時間后,向所得溶液中加入0.2molCuO粉末,恰好恢復到電解前的濃度和pH,則電解過程中轉移的電子的物質的量為 。
②若X、Y分別為鐵和銅,a仍為CuSO4溶液,則Y極的電極反應式為
③若用此裝置電解精煉銅, 做陽極,電解液CuSO4的濃度 (填“增大”、“減小”或“不變”)。
④若用此裝置在鐵制品上鍍銅,鐵制品做 ,電鍍液的濃度 (填“增大”、“減小”或“不變”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com