
分析 已知Fe+2Fe3+═3Fe2+,根據反應可知Fe應為負極,失電子被氧化,正極可為C、Cu等,正極上Fe3+得電子生成Fe2+,電解質溶液含有Fe3+.
解答 解:已知Fe+2Fe3+═3Fe2+,根據反應可知Fe應為負極,失電子被氧化,負極反應為Fe-2e-═Fe2+,正極可為C、Cu等,碳棒為正極,正極上Fe3+得電子生成Fe2+,其電極反應為:2Fe3++2e-═2Fe2+,電解質溶液含有Fe3+,則電解質可為FeCl3,裝置圖為 ,
,
答:Fe為負極,碳棒為正極,正極反應為2Fe3++2e-═2Fe2+,負極反應為Fe-2e-═Fe2+,電解質為,FeCl3,裝置圖為 .
.
點評 本題考查了原電池的設計和工作原理的探究,為側重于基礎知識的考查,題目難度不大,注意把握原電池的組成和原理,學習中注意基礎知識的積累.


科目:高中化學 來源: 題型:填空題
 向100mlMgCl2 和 AlCl3的混合溶液,逐滴加入1mol/LNaOH溶液,如圖:
向100mlMgCl2 和 AlCl3的混合溶液,逐滴加入1mol/LNaOH溶液,如圖:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有①② | B. | 只有①③ | C. | 只有②③ | D. | 只有③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
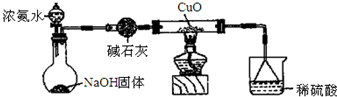
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1種 | B. | 2種 | C. | 3種 | D. | 4種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 可用FeCl3溶液鑒別化合物I和II | |
| B. | 物質I在NaOH醇溶液中加熱可發生消去反應 | |
| C. | 物質II中所有原子可能位于同一平面內 | |
| D. | 物質III與足量H2加成所得產物分子中有2個手性碳原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
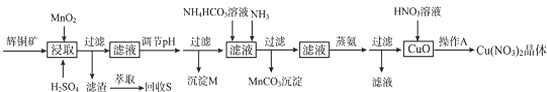
| 離子 | 開始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔點/K | 993 | 1539 | 183 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com