
(16分)輝銅礦是冶煉銅的重要原料。
(1)工業上冶煉粗銅的某種反應為:Cu2S+O2=2Cu+SO2
①當產生標況下11.2L氣體時,轉移電子數目為 ;
②將粗銅進行電解精煉,粗銅應與外電源的 極相接;若精煉某種僅含雜質鋅的粗銅,通電一段時間后測得陰極增重ag,電解質溶液增重bg,則粗銅中含鋅的質量分數為 ;
(2)將輝銅礦、軟錳礦做如下處理,可以制得堿式碳酸銅:
①銅單質放置于潮濕空氣中,容易生成堿式碳酸銅,反應化學方程式是 ;
②步驟Ⅱ中,碳酸氫銨參與反應的離子方程式為 ;
③步驟Ⅰ中發生如下3個反應,已知反應i)中生成的硫酸鐵起催化作用。請寫出反應iii)的化學方程式。
i)Fe2O3+3H2SO4 =Fe2(SO4)3+3H2O
ii) Cu2S+ Fe2(SO4)3 =CuSO4+CuS+2FeSO4
iii)
④步驟Ⅱ中調節pH后的溶液中,銅離子濃度最大不能超過 mol/L。
(已知Ksp[(Cu(OH)2)]=2×10-a)
(1)3NA (2)正 ③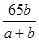 (2)①2Cu+O2+CO2+H2O=Cu2(OH)2CO3 ②HCO3-+H+=H2O+CO2↑
(2)①2Cu+O2+CO2+H2O=Cu2(OH)2CO3 ②HCO3-+H+=H2O+CO2↑
③iii)MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O ④2×1021-a
解析試題分析:(1)①根據反應Cu2S+O2=2Cu+SO2可知,反應中氧元素化合價和銅元素化合價降低,只有硫元素的化合價從-2價升高到+4價,失去6個電子,所以當產生標況下11.2L氣體即0.5mol二氧化硫時,轉移電子物質的量是0.5mol×6=3mol,其數目為3NA。
②將粗銅進行電解精煉,粗銅應與外電源的正極相接;若精煉某種僅含雜質鋅的粗銅,通電一段時間后測得陰極增重ag,增加的質量即為析出的銅,電解質溶液增重bg,設參加反應的鋅和銅的質量分別是mg、ng,則m+n-a=b,根據電子守恒可知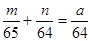 ,解得m=65b,則粗銅中含鋅的質量分數為
,解得m=65b,則粗銅中含鋅的質量分數為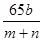 =
=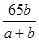 。
。
(2)①銅單質放置于潮濕空氣中,容易與氧氣、水、二氧化碳等結合生成堿式碳酸銅為生銹,反應化學方程式是2Cu+O2+CO2+H2O=Cu2(OH)2CO3。
②步驟Ⅱ是調節溶液pH的,因此碳酸氫銨與氫離子反應,則反應的離子方程式為HCO3-+H+=H2O+CO2↑。
③硫酸鐵起催化作用,則第二步中生成的硫酸亞鐵需要在第三步中重新被氧化生成硫酸鐵,因此反應的化學方程式為MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O。
④溶液的pH=3.5,則溶液中氫氧根濃度是10-10.5mol/L,所以根據氫氧化銅的溶度積常數可知,銅離子的濃度不能超過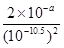 =2×1021-a mol/L。
=2×1021-a mol/L。
考點:考查氧化還原反應計算、粗銅精煉的計算、物質制備實驗條件控制以及溶度積常數的應用


科目:高中化學 來源: 題型:單選題
向物質的量濃度均為1 mol·L-1的AlCl3和鹽酸的混合溶液中逐滴滴入NaOH溶液,如圖中[n表示Al(OH)3的物質的量、V表示NaOH溶液的體積]能正確表示這個反應過程的是 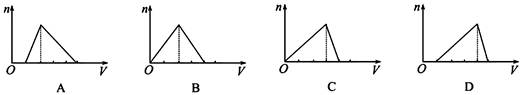
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化合物甲是由短周期元素組成的陶瓷材料,是一種以共價鍵相連的物質,具有耐高溫、抗沖擊、導熱性好等優良性質。乙是制備這種材料的起始原料,也是鋁土礦的主要成分。制備時采取碳熱還原氮化法,即把乙與炭粉按一定比例混合,在流動N2氣氛中加熱到一定溫度即可得到甲和可燃性氣體丙,二者原子個數之比均為1:1。8.2g甲與足量的氫氧化鈉溶液混合可以得到無色溶液丁,并產生標準狀況下4.48L氣體戊。
(1)乙的化學式為 ,寫出它的一種用途 。
(2)甲的晶體類型為 ,寫出碳熱還原氮化法制甲的化學方程式 。
(3)工業制備甲的過程中可能含有的雜質有 。
(4)氣體戊的結構式為 ,寫出甲與足量的氫氧化鈉溶液反應的化學方程式為 ,驗證溶液丁中溶質的實驗方法為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(8分)將稀硝酸逐滴加入盛有鋁鐵合金的容器中,當固體恰好完全溶解時,產生標準狀況下NO 40.32L,將反應后的溶液平均分成三等份,分別進行如下實驗:
(1)第一份溶液中逐滴加入2 mol·L-1NaOH溶液,至恰好達到最大沉淀,不考慮空氣中O2的氧化,則需加入NaOH溶液的體積為________________。
(2)第二份溶液中邊加入NaOH溶液,邊在空氣中充分攪拌,至恰好達到最大沉淀量,將產生的沉淀過濾、洗滌、干燥、稱量比第一份重5.1g,則該過程中消耗O2的物質的量為_______________。
(3)第三份溶液中逐滴加入4 mol·L-1NaOH溶液,至Al(OH)3沉淀恰好溶解,消耗NaOH溶液500mL,計算原合金中鋁的質量。(寫出解題過程)(4分)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
100毫升含HNO3、H2SO4的稀溶液中,加入9.6克銅充分反應,銅全溶,產生2.24升NO(標準狀況)。同體積的混合酸恰好與250毫升2mol/L的NaOH完全中和。
計算原混合酸中HNO3的物質的量濃度的取值范圍_________________________
H2SO4的物質的量濃度的取值范圍_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
我國化工專家侯德榜,改進氨堿法設計了“聯合制堿法”,為世界制堿工業作出了突出貢獻。生產流程如下: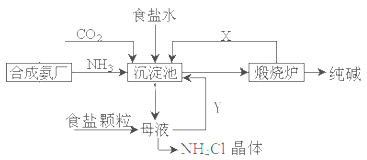
(1)完成有關反應的化學方程式
①沉淀池: NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl
②煅燒爐:
(2)聯合制堿法的優點表述中,不正確的是___________
A.生產原料為:食鹽、NH3、CO2
B.副產物氯化銨可做氮肥
C.生產過程中可循環利用的物質只有CO2
D.原料利用率高
某實驗小組,利用下列裝置模擬“聯合制堿法”的第一步反應。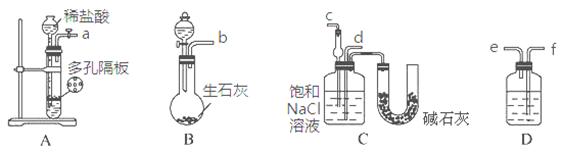
(3)上述裝置中接口連接順序為 ;
A.a接c;b接f、e接d B.a接d;b接f、e接c
C.b接d;a接e、f接c D.b接c;a接f、e接d
(4)D中應選用的液體為 。
為測定產品純堿的成分和含量,做如下實驗。假設產品純堿中只含NaCl、NaHCO3雜質。
(5)檢驗產品純堿中是否含有NaCl,可取少量試樣溶于水后,再滴加 試劑。
(6)滴定法測定純堿產品中NaHCO3含量的方法是:準確稱取純堿樣品W g,放入錐形瓶中加蒸餾水溶解,加1~2滴酚酞指示劑,用c mol/L的HCl溶液滴定至溶液由紅色變為無色(指示CO32- +H+=HCO3-反應的終點),所用HCl溶液體積為V1 mL,再加1~2滴甲基橙指示劑,繼續用HCl溶液滴定至溶液由黃色變為橙色,所用HCl溶液總體積為V2 mL。則純堿樣品中NaHCO3質量分數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)已知X、Y、Z、M、G、Q是六種短周期元素,原子序數依次增大。X、Z、Q的單質在常溫下呈氣態;Y的原子最外層電子數是其電子層數的2倍;X與M同主族;Z、G分別是地殼中含量最高的非金屬元素和金屬元素。
請回答下列問題:
(1)Y、Z、M、G四種元素原子半徑由大到小的順序是(寫元素符號) 。
(2)Z在元素周期表中的位置為 。
(3)上述元素的最高價氧化物對應的水化物酸性最強的是(寫化學式) 。
(4)X與Y能形成多種化合物,其中既含極性鍵又含非極性鍵,且相對分子質量最小的物質是(寫分子式) ,在實驗室中,制取該物質的反應原理是(寫化學方程式) 。
(5)M2Z的電子式為 。MX與水反應可放出氣體,該反應的化學方程式為 。
(6)常溫下,不能與G的單質發生反應的是(填序號) 。
a.CuSO4溶液 b.Fe2O3 c.濃硫酸 d.NaOH溶液 e.Na2CO3固體
工業上用電解法制G的單質的化學方程式是 ,若以石墨為電極,陽極產生的混合氣體的成分是(寫化學式) 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鎂、鋁、鐵及其化合物在生產、生活中有著廣泛的應用
I:實驗室采用MgCl2、AlCl3的混合溶液與過量氨水反應制備MgAl2O4,主要流程如下: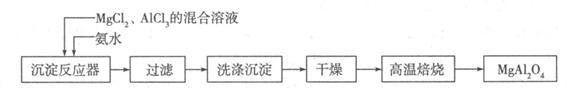
(1)已知25℃時Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34,該溫度下向濃度均為0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成 沉淀(填化學式)。
(2)高溫焙燒時發生反應的化學方程式 ,洗滌沉淀時的方法是 。
(3)常溫下如果向AlCl3飽和溶液中不斷通人HCl氣體,可析出AlCl3·6H2O晶體,結合化學平衡移動原理解釋析出晶體的原因: 。
Ⅱ:某興趣小組的同學發現將一定量的鐵與濃硫酸加熱時,觀察到鐵完全溶解,并產生大量氣體。為此,他們設計了如下裝置驗證所產生的氣體。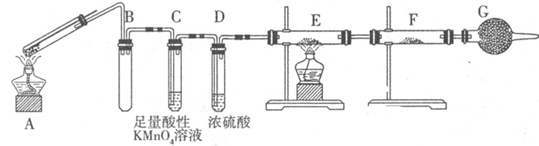
(1)G裝置的作用是 。
(2)證明有SO2生成的現象是 ,為了證明氣體中含有氫氣,裝置E和F中加入的試劑分別為 、 。
(3)若將鐵絲換成銅絲,反應后的溶液沒有出現預計的藍色溶液,而出現了大量白色固體,原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業上常用鐵質容器盛裝冷濃硫酸。為研究鐵質材料與熱濃硫酸的反應,某學習小組進行了以下探究活動:
(1)將已去除表面氧化物的鐵釘(碳素鋼)放入冷濃硫酸中,10分鐘后移入硫酸銅溶液中,片刻后取出觀察,鐵釘表面無明顯變化,其原因是 。
(2)另稱取鐵釘6.0g放入15.0ml濃硫酸中,加熱,充分應后得到溶液X并收集到氣體Y。
①甲同學認為X中除Fe3+外還可能含有Fe2+。寫出生成Fe2+所有可能的離子反應方程式: 。若要確認其中有Fe2+,應選用 (選填序號)。
a.KSCN溶液和氯水 b.鐵粉和KSCN溶液
c.濃氨水 d.酸性KMnO4溶液
②乙同學取336ml(標準狀況)氣體Y通入足量溴水中,發生反應的化學方程式為: 。然后加入足量BaCl2溶液,經適當操作后得干燥固體2.33g。由于此推知氣體Y中SO2的體積分數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com