
 HCO3-+OH-(2分)
HCO3-+OH-(2分) CO2↑+H2O(2分)
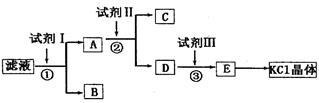
CO2↑+H2O(2分) HCO3-+OH-,溶液呈堿性,PH>7;(2)要除掉雜質離子硫酸根和碳酸根,應先加入過量的氯化鋇溶液,碳酸根和硫酸根與鋇離子反應生成硫酸鋇和碳酸鋇沉淀,離子方程式為:SO42-+Ba2+=BaSO4↓,CO32-+Ba2+=BaCO3↓;(3)要除掉多余的鋇離子,需加入過量碳酸鉀溶液,碳酸鉀和氯化鋇反應生成碳酸鋇沉淀,離子方程式為CO32-+Ba2+=BaCO3↓;(4)要除掉多余的碳酸根,要滴加適量的鹽酸,碳酸根離子和鹽酸反應生成二氧化碳和水,離子方程式為CO32-+2H+=CO2↑+H2O。
HCO3-+OH-,溶液呈堿性,PH>7;(2)要除掉雜質離子硫酸根和碳酸根,應先加入過量的氯化鋇溶液,碳酸根和硫酸根與鋇離子反應生成硫酸鋇和碳酸鋇沉淀,離子方程式為:SO42-+Ba2+=BaSO4↓,CO32-+Ba2+=BaCO3↓;(3)要除掉多余的鋇離子,需加入過量碳酸鉀溶液,碳酸鉀和氯化鋇反應生成碳酸鋇沉淀,離子方程式為CO32-+Ba2+=BaCO3↓;(4)要除掉多余的碳酸根,要滴加適量的鹽酸,碳酸根離子和鹽酸反應生成二氧化碳和水,離子方程式為CO32-+2H+=CO2↑+H2O。

科目:高中化學 來源:不詳 題型:填空題
| 混合物 | 分離或提純方法 |
| (1)除去Fe(OH)3膠體中的Cl- | ______ |
| (2)除去乙醇溶液中的NaCl | ______ |
| (3)分離飽和Na2CO3溶液和乙酸乙酯 | ______ |
| (4)分離碘和NaCl固體 | ______ |
| (5)除去CaO中的CaCO3 | ______ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
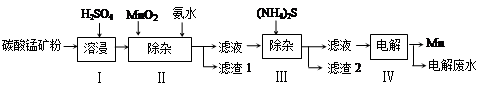
| 物質 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.乙醇 | B.苯 | C.四氯化碳 | D.直餾汽油 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 、CH3CH2OH、CH3CH2Br、NH4Cl溶液四種無色液體,只用一種試劑就能把 它們鑒別開,這種試劑是( )
、CH3CH2OH、CH3CH2Br、NH4Cl溶液四種無色液體,只用一種試劑就能把 它們鑒別開,這種試劑是( )| A.溴水 | B.NaOH溶液 |
| C.Na2SO4溶液 | D.Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| | 物 質 | 除雜試劑 | 分離方法 |
| A | 硝酸銅溶液(硝酸銀) | 銅粉 | 結晶 |
| B | NaCl溶液(CuCl2) | NaOH溶液 | 萃取 |
| C | 乙醇(水) | —— | 分液 |
| D | 鎂粉(鋁粉) | NaOH溶液 | 過濾 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
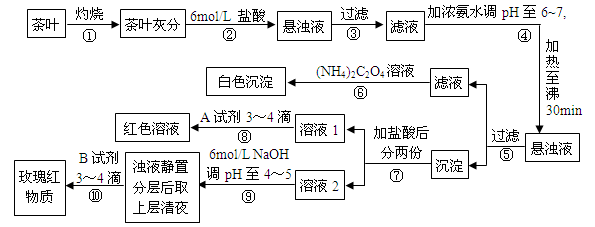
| A.步驟②加入6mol/L鹽酸的主要目的是為了將茶葉灰分中的鈣、鐵、鋁難溶性化合物轉化為可溶性氯化物 |
| B.步驟⑤所得濾液中溶質的主要成分為:CaCl2、NH3·H2O |
| C.步驟⑥可以檢出鈣元素存在,離子反應方程式為Ca2++C2O42- = CaC2O4↓ |
D.步驟⑧中A試劑為KSCN溶液,離子反應方程式為Fe3++3SCN- Fe(SCN)3 Fe(SCN)3 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

| 物質 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com