
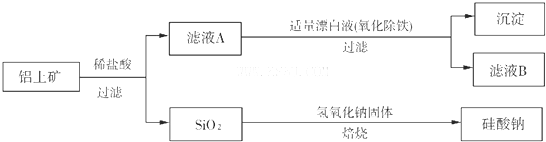
鋁土礦(主要成分為Al2O3,還含有SiO2、Fe2O3)是工業上制備氧化鋁的主要原料。工業上提取氧化鋁的工藝流程如下圖所示,請回答有關問題:
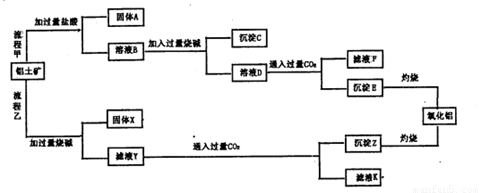
(1)流程乙加入燒堿后發生反應的離子方程式: .
(2)溶液D到沉淀E發生的離子方程式: 。
(3)驗證濾液B含Fe3+,可取少量濾液并加入 。
(4)濾液K中溶質的主要成份是 (填化學式)。
(1)Al2O3+2OH-+3H2O=2[Al(OH)4]-;SiO2+2OH-=SiO32-+H2O
(2)[Al(OH)4]-+CO2=HCO3-+ Al(OH)3↓(3)KSCN (4)NaHCO3
【解析】
試題分析:(1)氧化鐵和氫氧化鈉溶液不反應,氧化鋁和二氧化硅與氫氧化鈉溶液反應,所以有關反應的離子方程式是Al2O3+2OH-+3H2O=2[Al(OH)4]-、SiO2+2OH-=SiO32-+H2O。
(2)溶液B中含有鋁離子,和過量的氫氧化鈉溶液反應生成偏鋁酸鈉,然后再通入CO2則又生成氫氧化鋁白色沉淀,反應的離子方程式是[Al(OH)4]-+CO2=HCO3-+ Al(OH)3↓。
(3)檢驗溶液中鐵離子的試劑是KSCN溶液。
(4)由于濾液Y生成濾液K的試劑是過量的CO2氣體,所以濾液K中溶質的主要成份是碳酸氫鈉。
考點:考查鋁土礦提取氧化鋁的有關判斷以及方程式的書寫
點評:該題是高考中的常見題型,屬于中等難度的試題。試題綜合性強,難易適中,側重對學生基礎知識的鞏固與訓練,同時也注重對學生答題能力的培養和方法指導。該題不僅可以考查學生對化學知識的熟悉理解程度,更重要的是培養學生的綜合分析能力和思維方法。


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

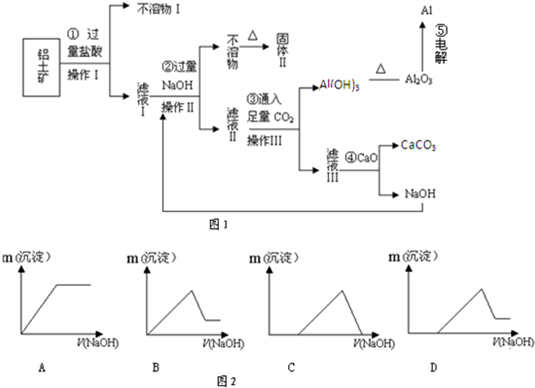
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||


| △ |

查看答案和解析>>
科目:高中化學 來源: 題型:
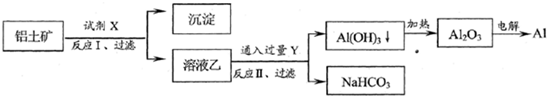
| A、試劑X為稀硫酸 | B、反應II中生成Al(OH)3的反應為:CO2+AlO2-+2H2O→Al(OH)3↓+HCO3- | C、結合質子(H+)的能力由強到弱的順序是:OH->AlO2->CO32- | D、Al2O3熔點很高,工業上還可采用電解熔融AlCl3冶煉Al |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com