
用NA表示阿伏加德羅常數的值。下列敘述正確的是( )
A. 1molCl2與Fe粉完全反應時轉移電子數為2NA
B. 過氧化鈉與水反應時,每生成1molO2,轉移4mol電子
C. 標準狀況下,11.2L氟化氫中含有氟原子的數目為0.5NA
D. 0.1 mol·L-1NaHSO4溶液中,陽離子數目之和為0.3NA
科目:高中化學 來源:2017屆陜西省高三上學期第二次模考化學試卷(解析版) 題型:填空題
實驗室可由軟錳礦(主要成分為MnO2)制備KMnO4,方法如下:軟錳礦與過量固體KOH和KClO3在高溫下反應,生成錳酸鉀(K2MnO4)和KCl;用水溶解,濾去殘渣,濾液酸化后,K2MnO4轉變為MnO2和KMnO4;濾去MnO2沉淀,濃縮濾液,結晶得到深紫色的針狀KMnO4。請回答:
(1)軟錳礦制備K2MnO4的化學方程式是_______________________;
(2)K2MnO4制備KMnO4的離子方程式是_______________;
(3)若用2.5g軟錳礦(含MnO2 80%)進行上述實驗,KMnO4的理論產量為_______________。
(4)KMnO4能與熱的經硫酸酸化的Na2C2O4溶液反應生成Mn2+和CO2,該反應的化學方程式是________________________;
(5)上述制得KMnO4產品0.165g,恰好與0.335g Na2C2O4反應完全,該KMnO4的純度為___。
查看答案和解析>>
科目:高中化學 來源:2017屆浙江省高三3月選考化學試卷(解析版) 題型:選擇題
下列關于能源的說法不正確的是
A. 植物通過光合作用,將太陽能轉化為生物質能
B. 在農村推廣建造沼氣池,是對生物質能的有效利用
C. 天然氣的主要成分是甲烷,是一種可再生的清潔能源
D. 氫能是重要的清潔能源,在藍綠藻、微生物和太陽光作用下使水分解制氫是目前科學家研究的新方法之一
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:選擇題
鎂鋁合金4.08 g溶于250 ml 2mol/L的鹽酸中,標準狀況下放出氣體的體積為4.48 L,向反應后的溶液中加入500 ml NaOH溶液,充分反應后最終產生白色沉淀。下列有關說法不正確的是( )
A. 4.08 g鎂鋁合金中含有鎂和鋁的質量分別為1.92g、2.16g
B. 生成沉淀的最大質量為10.88 g
C. 若白色沉淀只有Mg(OH)2,該NaOH溶液的濃度至少為0.96mol/L
D. 溶解4.08 g鎂鋁合金時,剩余鹽酸的物質的量為0.1 mol
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:選擇題
下列關于合金的敘述中正確的是( )
A. 日常生活中用到的五角硬幣屬于銅合金
B. 低碳鋼比中碳鋼強度高
C. 合金在任何情況都比單一金屬性能優良
D. 合金是由兩種或多種金屬熔合而成的
查看答案和解析>>
科目:高中化學 來源:2016-2017學年新疆哈密地區第二中學高二上學期期末考試化學試卷(解析版) 題型:填空題
已知25℃、101kPa時,一些物質的燃燒熱為:
化學式 | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
ΔH/(kJ/mol) | -283.0 | -285.8 | -726.51 | -890. 31 |
請回答下列問題:
(1)根據蓋斯定律完成下列反應的熱化學方程式:
CO(g)+2H2(g)==CH3OH(l) ΔH=_________。
(2)現有H2和CH4的混合氣體112 L(標準狀況),使其完全燃燒生成CO2(g)和H2O(l),共放出熱量3 242.5 kJ,則原混合氣體中H2和CH4的物質的量之比是:____________。
A.1:1 B.1:3 C.1:4 D.2:3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年新疆哈密地區第二中學高二上學期期末考試化學試卷(解析版) 題型:選擇題
對于反應2NO2(g) N2O4(g) ΔH<0,達到平衡后縮小容器體積,下列說法正確的是
N2O4(g) ΔH<0,達到平衡后縮小容器體積,下列說法正確的是
A. 平衡逆向移動 B. 混合氣體顏色比原來深
C. 混合氣體顏色比原來淺 D. 混合氣體的平均相對分子質量變小
查看答案和解析>>
科目:高中化學 來源:2016-2017學年新疆哈密地區第二中學高二上學期期末考試化學試卷(解析版) 題型:選擇題
一定量的鹽酸跟過量鋅粉反應時,為了減緩反應速率但又不影響生成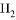 的總量,可采取的措施是( )
的總量,可采取的措施是( )
A. 加入少量 固體 B. 加入少量
固體 B. 加入少量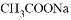 固體
固體
C. 加入少量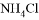 固體 D. 加入少量
固體 D. 加入少量 固體
固體
查看答案和解析>>
科目:高中化學 來源:2017屆貴州省貴陽市高三2月適應性考試(一)理綜化學試卷(解析版) 題型:實驗題
納米ZnO的顆粒直徑介于1~100nm之間,具有許多特殊的性能,可用于制造變阻器、圖像記錄材料、磁性材料和塑料薄膜等。一種利用粗ZnO(含FeO、Fe2O3、CuO)制備納米ZnO的生產工藝流程如下圖所示:
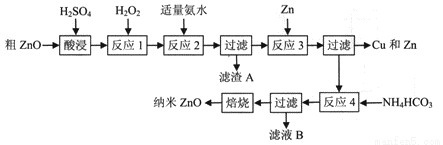
已知:① 生成氫氧化物沉淀時溶液的pH如下表:
物質 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
開始沉淀時pH | 6.34 | 1.48 | 6.2 | 5.2 |
完全沉淀時pH | 9.7 | 3.2 | 8.0 | 6.4 |
② 25℃時,Fe(OH)3的溶度積常數Ksp=4.0×10-38。
請回答以以下問題:
(1)酸浸時,為了提高浸出率,可采取的措施有________(填寫兩種);
(2)反應1中發生反應的離子方程式為______________,一種雙氧水的質量分數為34.0 % (密度為1.13g/cm3) ,其濃度為_______mol/L;
(3)反應2中加適量氨水的目的是_________,此時所需pH的范圍為_________,當調節溶液pH=5時,溶液中的c(Fe3+)=__________;
(4)反應3的離子方程式為__________,反應類型為__________;
(5)從濾液B中可回收的主要物質是__________;
(6)經檢驗分析,反應4 所得固體組成為Zna(OH)bCO3,稱取該固體22.4g,焙燒后得固體16.2g,則a=_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com