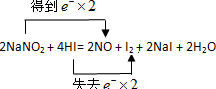
(2009?泰安模擬)某研究性學習小組對過量炭粉與氧化鐵反應的氣體產物成分進行研究.
(1)提出假設:該反應的氣體產物全部是二氧化碳.
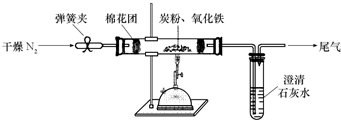
(2)設計方案:如圖所示,將一定量的氧化鐵在隔絕空氣的條件下與過量炭粉完全反應,測定參加反應的碳元素與氧元素的質量比.
(3)查閱資料:氮氣不與碳、氧化鐵發生反應.實驗室可以用氯化銨飽和溶液和亞硝酸鈉(NaNO
2)飽和溶液混合加熱反應制得氮氣.請寫出該反應的離子方程式
NH4++NO2-=N2↑+2H2O
NH4++NO2-=N2↑+2H2O
.
(4)實驗操作及實驗現象:
①按上圖連接裝置,并檢查裝置的氣密性,稱取3.20g氧化鐵與2.00g炭粉混合均勻,放入48.48g的硬質玻璃管中;
②加熱前,先通一段時間純凈干燥的氮氣;
③停止通入N
2后,夾緊彈簧夾,加熱一段時間,澄清石灰水變渾濁;
④待反應結束,再通一段時間的氮氣,然后冷卻至室溫,稱得硬質玻璃管和固體總質量為52.24g.
(5)數據處理:經計算,參加反應的碳元素質量為0.48g,氧元素質量為0.96g.得出原假設不成立,理由是
反應后的氣體中碳、氧原子的物質的量之比為2:3,與二氧化碳中碳、氧原子的物質的量比不相符
反應后的氣體中碳、氧原子的物質的量之比為2:3,與二氧化碳中碳、氧原子的物質的量比不相符
.
(6)得出結論:根據數據處理結果判斷,反應產生的氣體是,該實驗中發生反應的化學方程式為
CO和CO
2;2C+Fe
2O
32Fe+CO↑+CO
2↑
CO和CO
2;2C+Fe
2O
32Fe+CO↑+CO
2↑
.
(7)實驗優化:根據實驗得出的結論應對該實驗裝置進一步完善,請你從下圖所示裝置中選取必要裝置,對實驗加以改進
在原裝置最后連接上C裝置
在原裝置最后連接上C裝置
.




 閱讀快車系列答案
閱讀快車系列答案