
 硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g)
硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g)| 催化劑 | △ |
| 催化劑 |
| △ |
| 0.162 |
| 0.042×0.02 |


科目:高中化學 來源: 題型:閱讀理解
(14分)I.科學家一直致力于“人工固氮”的新方法研究。
(1)根據最新“人工固氮”的研究報道,在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發生下列反應:2N2 (g)+6H2O (l)4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
進一步研究NH3生成量與溫度的關系,常壓下達到平衡時測得部分實驗數據如下表:
| 溫度 T/K | 303 | 313 | 323 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
① 此合成反應的a 0 (填“>”“<”或“=”)
② 已知:
N2 (g) + 3H2(g)2NH3 (g) ΔH=-92.4 kJ·mol-1,
2H2 (g)+ O2 (g)===2H2O (l) ΔH=-571.6 kJ·mol-1,
則2N2 (g) + 6H2O (l)4NH3 (g) + 3O2 (g) ΔH= ;
(2)用水稀釋0.1 mol·L-1氨水,溶液中隨著水量的增加而減小的是 (填字母標號)
II.工業生產中產生含SO2的廢氣,經石灰吸收和氧化后制成硫酸鈣,硫酸鈣是一種用途非常廣泛的產品,可用于生產硫酸、水泥等。
(1)硫酸生產中,SO2催化氧化成SO3的熱化學方程式為:
2SO2 (g) + O2(g)2SO3 (g) ΔH=-196.0 kJ·mol-1
① 容器體積不變時,為了提高SO2的轉化率,可采用的措施是 (填字母標號)
A.加入V2O5作催化劑 B.使用過量SO2 C.高溫 D.通入過量空氣
② 某溫度時,在一個容積為10L的密閉容器中充入4.0 molSO2和2.0 molO2,半分鐘后達到平衡,并放出352.8kJ的熱量。此時SO2的轉化率是 ,該溫度下的平衡常數K= ;
(2)已知25℃時,Ksp(CaSO4)=7.10×10-5。向0.100 L 含CaSO4固體的溶液中加入2.22 gCaCl2 粉末充分攪拌,假設溶液的體積變化忽略不計,則溶液中CaSO4固體的質量將 (填“增大”、“減小”或“不變”,下同),Ksp(CaSO4)將 。
查看答案和解析>>
科目:高中化學 來源:2011屆山東省日照市高三第一次模擬考試(理綜)化學部分 題型:填空題
(14分)I.科學家一直致力于“人工固氮”的新方法研究。
(1)根據最新“人工固氮”的研究報道,在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發生下列反應:2N2 (g)+6H2O(l) 4NH3 (g)+3O2 (g) ΔH=a kJ·mol-1
4NH3 (g)+3O2 (g) ΔH=a kJ·mol-1
進一步研究NH3生成量與溫度的關系,常壓下達到平衡時測得部分實驗數據如下表:
| 溫度T/K | 303 | 313 | 323 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
 ”“<”或“=”)
”“<”或“=”) 2NH3 (g) ΔH=-92.4kJ·mol-1,
2NH3 (g) ΔH=-92.4kJ·mol-1, 4NH3 (g) + 3O2 (g) ΔH= ;
4NH3 (g) + 3O2 (g) ΔH= ;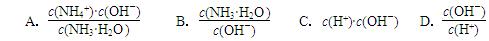
 2SO3 (g) ΔH=-196.0kJ·mol-1
2SO3 (g) ΔH=-196.0kJ·mol-1| A.加入V2O5作催化劑 | B.使用過量SO2 | C.高溫 | D.通入過量空氣 |
查看答案和解析>>
科目:高中化學 來源:2011-2012學年河北省魏縣一中高二上學期期中考試化學試卷 題型:填空題
(8分)硫酸生產中,SO2催化氧化成SO3的熱化學方程式為:
2 SO2 (g)+ O2(g) 2 SO3(g) △H =" —196.0" kJ.mol-1
2 SO3(g) △H =" —196.0" kJ.mol-1
①容器體積不變時,為了提高SO2的轉化率,可采用的措施是_____(填字母標號)。(2分)
| A.加入V2O5做催化劑 | B. 使用過量SO2 使用過量SO2 | C.高溫 | D.通入過量空氣 |
查看答案和解析>>
科目:高中化學 來源:2010-2011學年山東省日照市高三第一次模擬考試(理綜)化學部分 題型:填空題
(14分)I.科學家一直致力于“人工固氮”的新方法研究。
(1)根據最新“人工固氮”的研究報道,在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發生下列反應:2N2 (g)+6H2O (l) 4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
進一步研究NH3生成量與溫度的關系,常壓下達到平衡時測得部分實驗數據如下表:
|
溫度 T/K |
303 |
313 |
323 |
|
NH3生成量/(10-6 mol) |
4.8 |
5.9 |
6.0 |
① 此合成反應的a 0 (填“>”“<”或“=”)
② 已知:
N2 (g) + 3H2(g) 2NH3 (g) ΔH=-92.4 kJ·mol-1,
2NH3 (g) ΔH=-92.4 kJ·mol-1,
2H2 (g) + O2 (g)===2H2O (l) ΔH=-571.6 kJ·mol-1,
則2N2 (g) + 6H2O (l) 4NH3 (g) + 3O2 (g) ΔH=
;
4NH3 (g) + 3O2 (g) ΔH=
;
(2)用水稀釋0.1 mol·L-1氨水,溶液中隨著水量的增加而減小的是 (填字母標號)

II.工業生產中產生含SO2的廢氣,經石灰吸收和氧化后制成硫酸鈣,硫酸鈣是一種用途非常廣泛的產品,可用于生產硫酸、水泥等。
(1)硫酸生產中,SO2催化氧化成SO3的熱化學方程式為:
2SO2 (g) + O2(g) 2SO3 (g) ΔH=-196.0 kJ·mol-1
2SO3 (g) ΔH=-196.0 kJ·mol-1
① 容器體積不變時,為了提高SO2的轉化率,可采用的措施是 (填字母標號)
A.加入V2O5作催化劑 B.使用過量SO2 C.高溫 D.通入過量空氣
② 某溫度時,在一個容積為10L的密閉容器中充入4.0 molSO2和2.0 molO2,半分鐘后達到平衡,并放出352.8kJ的熱量。此時SO2的轉化率是 ,該溫度下的平衡常數K= ;
(2)已知25℃時,Ksp(CaSO4)=7.10×10-5。向0.100 L 含CaSO4固體的溶液中加入2.22 gCaCl2 粉末充分攪拌,假設溶液的體積變化忽略不計,則溶液中CaSO4固體的質量將 (填“增大”、“減小”或“不變”,下同),Ksp(CaSO4)將 。
查看答案和解析>>
科目:高中化學 來源:同步題 題型:填空題

 2NH3(g) △H<0,其化學平衡常數K與溫度t的關系如下表:
2NH3(g) △H<0,其化學平衡常數K與溫度t的關系如下表: 
 N2(g)+3H2(g)的化學平衡常數的值為___
N2(g)+3H2(g)的化學平衡常數的值為___ 2SO3(g) △H<0某溫度下,SO2的平衡轉化率(a)與體系總壓強(p)的關系如下圖所示。根據圖示回答下列問題:
2SO3(g) △H<0某溫度下,SO2的平衡轉化率(a)與體系總壓強(p)的關系如下圖所示。根據圖示回答下列問題: 
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com