
【題目】磷化氫(![]() )、氧硫化碳(COS)均可作儲糧害蟲殺劑。請回答下列問題:
)、氧硫化碳(COS)均可作儲糧害蟲殺劑。請回答下列問題:
(1)磷原子的核外電子排布式______________,核外有______種不同能量的電子;其最外層有____種運動狀態不同的電子,這些電子占據的軌道數為____個。
(2)氧硫化碳中,元素的非金屬性最強的元素在周期表中的位置是______;已知COS與![]() 的結構相似,試寫出COS的電子式______________,COS屬于_____分子(填“極性”或“非極性”)。
的結構相似,試寫出COS的電子式______________,COS屬于_____分子(填“極性”或“非極性”)。
氧硫化碳水解及部分應用流程如下(部分產物已略去):
COS![]() H2S
H2S![]() Na2S
Na2S![]() M溶液+H2
M溶液+H2
(3)寫出反應Ⅱ的離子方程式:_____________________;
(4)硫酸工業生產中接觸室內發生的反應方程式為___________;在實際生產中,操作溫度選定400~500℃、壓強通常采用常壓的原因分別是____________。
【答案】1s22s22p63s23p3 5 5 4 第二周期第VIA族 ![]() 極性 H2S+ 2OH- →S2- + 2H2O 2SO2 + O2
極性 H2S+ 2OH- →S2- + 2H2O 2SO2 + O2![]() 2SO3 催化劑在400~500℃時,活性最大,在常壓下及400~500℃時,二氧化硫的轉化率已經很高,若加壓會增加設備、投資和能量消耗
2SO3 催化劑在400~500℃時,活性最大,在常壓下及400~500℃時,二氧化硫的轉化率已經很高,若加壓會增加設備、投資和能量消耗
【解析】
(1)磷的質子數為15,原子的核外電子排布式1s22s22p63s23p3,核外有5種不同能量的電子;各電子的運動狀態不同,其最外層有5 個電子,所以5種運動狀態不同的電子,這些電子占據的軌道數為1+3=4個;
(2)氧硫化碳中,元素的非金屬性最強的元素是氧元素,在周期表中的位置為第二周期第ⅥA族;碳原子與氧原子、硫原子形成2對共用電子對,COS分子電子式為![]() ,COS分子中正負電荷中心不重合;
,COS分子中正負電荷中心不重合;
(3)II是硫化氫與氧氧化鈉反應生成硫化鈉和水;
(4)從溫度對催化劑催化活性影響及壓強增大后都設備的要求分析。
(1)磷的質子數為15,原子的核外電子排布式1s22s22p63s23p3,核外有5種不同能量的電子;各電子的運動狀態不同,其最外層有5 個電子,所以5種運動狀態不同的電子,這些電子占據的軌道數為1+3=4個;
(2)氧硫化碳中,同周期從左到右元素的非金屬性增強,同主族從上到下元素的非金屬性減弱,元素的非金屬性最強的元素是氧元素,O在周期表中的位置為第二周期第ⅥA族;碳原子與氧原子、硫原子形成2對共用電子對,COS分子電子式為![]() ,COS分子中正負電荷中心不重合,所以是極性分子;
,COS分子中正負電荷中心不重合,所以是極性分子;
(3)II是硫化氫與氧氧化鈉反應生成硫化鈉,硫化氫是弱電解質,反應的離子方程式為:H2S+2OH-→S2-+2H2O;
(4)硫酸工業中,接觸室中二氧化硫與氧氣催化氧化生成三氧化硫,反應方程式為:2SO2+O2![]() 2SO3;由于催化劑在400~500℃時,活性最大,且在常壓下及400~500℃時,二氧化硫的轉化率已經很高,若加壓會增加設備、投資和能量消耗,所以在實際生產中,操作溫度選定400~500℃、壓強通常采用常壓。
2SO3;由于催化劑在400~500℃時,活性最大,且在常壓下及400~500℃時,二氧化硫的轉化率已經很高,若加壓會增加設備、投資和能量消耗,所以在實際生產中,操作溫度選定400~500℃、壓強通常采用常壓。


 智趣暑假溫故知新系列答案
智趣暑假溫故知新系列答案科目:高中化學 來源: 題型:
【題目】1-溴丁烷(密度1.2758 g/mL)是重要的有機合成中間體及有機溶劑,可以在實驗室里用溴化鈉、濃硫酸和1-丁醇為原料,經過如圖六步制得。
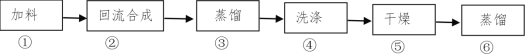
完成下列填空:
(1)通過步驟②獲得粗產品,反應的化學方程式是___。此時產品往往呈紅棕色,原因是____。實驗室里有下列常用試劑,請根據實驗需要為與步驟④相關的(2)(3)小題選擇試劑,并用試劑編號填空:
a.NaOH溶液 b.NaHCO3溶液 c.NaHSO3 溶液 d.NaBr溶液
(2)產品的紅棕色可用___除去(填寫試劑編號),相應的離子方程式為___。
(3)選用濃硫酸洗去未反應的1-丁醇和有機副產物,然后除酸。最適宜的除酸試劑是__(填寫試劑編號)。
(4)用濃硫酸(密度1.84g/mL)洗滌時,采用___(填寫儀器名稱)分離出___(填寫“上”或“下”)層產物。
(5)檢驗產物中含有溴元素的實驗方法是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D都是中學化學中常見物質,其中A、B、C均含有同一種元素,在一定條件下相互轉化關系如下(部分反應中的水已略去)。根據題意回答下列問題:

(1)若A、B、C的焰色反應均為黃色,C為廚房中的用品,D的過度排放會造成溫室效應。
①A的化學式______________、B的俗名____________;
②反應II的離子方程式是__________________________________。
(2)若A、D均為單質,且A為氣體,D元素的一種紅棕色氧化物常用作顏料。
①反應II的離子方程式是_____________________________;
②反應Ⅲ的離子方程式是_____________________________;
③檢驗B中陽離子最好的方法是_____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關有機物說法不正確的是( )
A. 等質量的苯乙烯和聚苯乙烯燃燒耗氧量相同
B. 四苯基乙烯(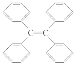 )中所有碳原子一定處于同一平面
)中所有碳原子一定處于同一平面
C. 1 mol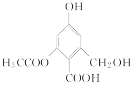 分別與足量的Na、NaOH溶液、NaHCO3溶液反應,消耗這三種物質的物質的量分別是3 mol、4 mol、1 mol
分別與足量的Na、NaOH溶液、NaHCO3溶液反應,消耗這三種物質的物質的量分別是3 mol、4 mol、1 mol
D. 1molβ紫羅蘭酮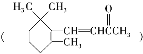 與1molBr2發生加成反應可得3種產物
與1molBr2發生加成反應可得3種產物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮元素的單質和常見的化合物在工、農業生產中用途廣泛。
(1)工業上利用分離空氣的方法得到氮氣.空氣各主要成分的沸點如下:
N2 | O2 | Ar | CO2 |
-196℃ | -183℃ | -186℃ | -78℃ |
現將空氣深度冷卻液化,然后緩慢升溫,則最先分離出來的氣體是______.
(2)雷雨時空氣中的N2轉化為NO,生成物NO是______色的氣體,______(填“易”或“難”)溶于水;NO在空氣中很容易被氧化成NO2,NO2能與水發生化學反應,寫出NO2與水反應的化學方程式為__________________.
(3)實驗室可用固體NH4Cl與固體Ca(OH)2加熱反應制取氨氣;
①制取氨氣的化學方程式為__________________;
②要制取標準狀況下4.48L的氨氣,至少需要稱取固體NH4Cl的質量為______g;
(4)已知:4NH3+6NO![]() 5N2+6H2O化學研究性學習小組的同學在技術人員的指導下,按下列流程,探究不同催化劑對NH3還原NO反應的催化性能;
5N2+6H2O化學研究性學習小組的同學在技術人員的指導下,按下列流程,探究不同催化劑對NH3還原NO反應的催化性能; ![]()
若控制其他實驗條件均相同,在催化反應器中裝載不同的催化劑,將經催化反應后的混合氣體,通過一定體積滴有酚酞的稀硫酸溶液(溶液的體積、濃度均相同);
①NH3與稀硫酸溶液反應的離子方程式為__________________;
②為了比較不同催化劑的催化性能,需要測量并記錄的數據是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組探究氨基甲酸銨(![]() )分解的化學平衡和水解反應速率。將一定量純凈的氨基甲酸銨置于固定容積為100mL的密閉真空溶液A中,在恒定溫度下使其達到分解平衡。實驗測得不同溫度下的平衡數據列于下表:
)分解的化學平衡和水解反應速率。將一定量純凈的氨基甲酸銨置于固定容積為100mL的密閉真空溶液A中,在恒定溫度下使其達到分解平衡。實驗測得不同溫度下的平衡數據列于下表:
溫度(℃) | 20.0 | 25.0 | 30.0 | 35.0 |
平衡氣體總物質的量(mol) | 0.34 | 0.48 | 0.68 | 0.94 |
①氨基甲酸銨分解的化學方程式為![]() ,若25.0℃時達到平衡所用時間為8min,根據數據計算
,若25.0℃時達到平衡所用時間為8min,根據數據計算![]() 的平均生成速率為________________。
的平均生成速率為________________。
②可以判斷該分解反應已經達到化學平衡的是_________。
A.2υ(NH3)正=υ(CO2)逆 B.密閉容器中總壓強不變
C. 密閉容器中混合氣體的密度不變 D. 密閉容器中氨氣的體積分數不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關熱化學方程式的敘述中,正確的是 ( )
A.含20.0gNaOH的稀溶液與足量的稀硫酸完全中和,放出28.7kJ的熱量,則表示中和熱的熱化學方程式為:2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) H=-114.6kJ/mol
B.已知熱化學方程式: SO2(g)+![]() O2(g)
O2(g) ![]() SO3(g) H=-98.32kJ/mol,在容器中充入2mol SO2和1mol O2充分反應,最終放出的熱量為196.64kJ
SO3(g) H=-98.32kJ/mol,在容器中充入2mol SO2和1mol O2充分反應,最終放出的熱量為196.64kJ
C.已知2H2(g)+O2(g) =2H2O(g)H=-483.6kJ/mol,則H2的燃燒熱為241.8kJ/mol
D.用稀氨水與稀鹽酸進行中和熱的測定實驗,計算得到的中和熱的H偏大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣的無害化處理已成為當今汽車工業的一項重要課題,其基本原理是實現2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)的反應。關于該反應,下列說法正確的是( )
N2(g)+2CO2(g)的反應。關于該反應,下列說法正確的是( )
A. 只要使用合理的催化劑及載體,就可完全清除NO和CO
B. 使用催化劑只能改變反應的速率不能改變反應的平衡常數
C. 假設該反應在密閉容器中進行,一段時間后達到平衡時c(NO)=c(CO)
D. 恒溫恒容條件下,通入惰性氣體可提高NO轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學課外活動小組為了驗證元素非金屬性遞變規律,設計了如圖所示的兩套實驗方案進行實驗探究:
(1)根據方案一裝置![]() 如圖
如圖![]() 回答以下問題:
回答以下問題:
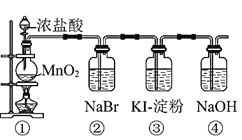
Ⅰ![]() 寫出裝置①中發生反應的化學方程式:______。
寫出裝置①中發生反應的化學方程式:______。
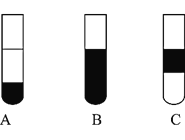
Ⅱ![]() 若將反應后②中的溶液倒入
若將反應后②中的溶液倒入![]() 中,出現的現象與圖中吻合的是______。
中,出現的現象與圖中吻合的是______。![]() 填代號
填代號![]()
Ⅲ![]() 裝置③中的現象是______。
裝置③中的現象是______。
(2)根據方案二裝置![]() 如圖
如圖![]() 回答以下問題:
回答以下問題:

Ⅰ![]() 方案二驗證元素非金屬性遞變的理論依據是:______。
方案二驗證元素非金屬性遞變的理論依據是:______。
Ⅱ![]() 裝置的作用是______,X是______。
裝置的作用是______,X是______。
Ⅲ![]() 能說明碳元素與硅元素非金屬性強弱的實驗現象是______。
能說明碳元素與硅元素非金屬性強弱的實驗現象是______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com