
二氧化鈰(CeO2)是一種重要的稀土氧化物。平板電視顯示屏生產過程中產生大量的廢玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物質)。某課題組以此粉末為原料回收鈰,設計實驗流程如下:
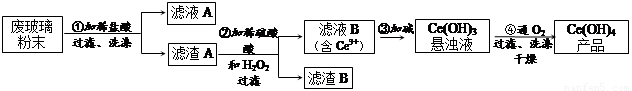
(1)洗滌濾渣A的目的是為了去除 (填離子符號),檢驗該離子是否洗滌的方法是
。
(2)第②步反應的離子方程式是 ,濾渣B的主要成分是 。
(3)萃取是分離稀土元素的常用方法,已知化合物TBP作為萃取劑能將鈰離子從水溶液中萃取出來,TBP (填“能”或“不能”)與水互溶。實驗室進行萃取操作是用到的主要玻璃儀器有 、燒杯、玻璃棒、量筒等。
(4)取上述流程中得到的Ce(OH)4產品0.536g,加硫酸溶解后,用0.1000mol?L-1FeSO4標準溶液滴定終點是(鈰被還原為Ce3+),消耗25.00mL標準溶液,該產品中Ce(OH)4的質量分數為 。
(1)濾渣上附著的Fe3+、Cl-等, 取最后洗滌液少量于試管中,滴加幾滴AgNO3溶液,如無白色沉淀,則洗干凈。
(2)2CeO2+H2O2+6H+ =2Ce3++O2↑+4H2O SiO2
(3)不能 分液漏斗
(4)97.01%
【解析】該反應過程為:①CeO2、SiO2、Fe2O3等中加入稀鹽酸,Fe2O3轉化為FeCl3存在于濾液中,濾渣為CeO2和SiO2,②加入稀硫酸和H2O2,CeO2轉化為Ce3+,濾渣為SiO2,③加入堿后Ce3+轉化為沉淀,④通入氧氣講Ce從+3氧化為+4,得到產品。
Ce(OH)4 ——— FeSO4
n(Ce(OH)4) = n(FeSO4) = 0.1000mol/L×0.025L = 0.0025mol, m = 0.0025mol×208g/mol = 0.52g
0.52÷0.536×100%=97.01%
【考點定位】以工藝流程為基礎,考查化學實驗基本操作、元素及化合物知識、化學計算、氧化還原反應等相關知識。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
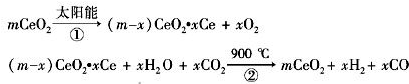
| A、該過程中CeO2沒有消耗 | B、該過程實現了太陽能向化學能的轉化 | C、右圖中△H1=△H2+△H3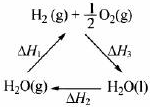 | D、以CO和O2構成的堿性燃料電池的負極反應式為CO+4OH--2e-═CO32-+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
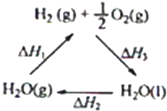 某科學家利用二氧化鈰(CeO2)在太陽能作用下將H2O、CO2轉變成H2、CO.其過程如下:
某科學家利用二氧化鈰(CeO2)在太陽能作用下將H2O、CO2轉變成H2、CO.其過程如下:| 太陽能 |
| ① |
| 900℃ |
| ① |
| A、該過程中CeO2沒有消耗 |
| B、該過程實現了太陽能向化學能的轉化 |
| C、圖中△H1=△H2+△H3 |
| D、以CO和O2構成的堿性燃料電池的負極反應式為CO+4OH--2e-=CO32-+2H2O |
查看答案和解析>>
科目:高中化學 來源:2013-2014學年湖北省孝感市三年級第一次統一考試化學試卷(解析版) 題型:填空題
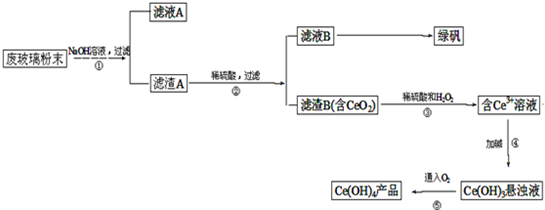
二氧化鈰(CeO2)是一種重要的稀土氧化物。平板電視顯示屏生產過程中產生大量的廢玻璃粉末(含SiO2、Fe2O3、CeO2等物質)。某課題以此粉末為原料,資源回收的工藝流程如下:
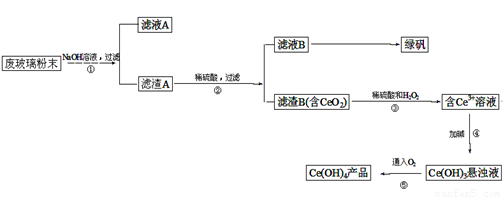
(1)寫出第①步反應的離子方程式 。
(2)洗滌濾渣B的目的是為了除去____(填離子符號),檢驗該離子是否洗凈的方法是 。
(3)寫出第③步反應的化學方程式_____________________________。
(4)制備綠礬(FeSO4·7H2O)時,向Fe2(SO4)3溶液中加入過量鐵屑,充分反應后,經過濾得到FeSO4溶液,再經 、 、過濾、洗滌、干燥等操作步驟得到綠礬。
(5)取上述流程中得到的Ce(OH)4產品(質量分數為97%)1.0g,加硫酸溶解后,用0.1000mol/LFeSO4溶液滴定至終點(鈰被還原成Ce3+),則需準確滴加標準溶液的體積為 mL。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com