
(15分)
請設計實驗:用MnO2與濃鹽酸制備純凈、干燥的Cl2,其他藥品與試劑任選。
(1)寫出該反應的化學方程式 。
(2)在下面方框中,A表示有分液漏斗和圓底燒瓶組成的氣體發(fā)生器,請在虛線框內的A后完成該反應的實驗裝置示意圖(夾持裝置、連接膠管不必畫出,需要加熱的儀器下方用△標出),按氣流方向在每件儀器下方標出字母B、C……;其他可選用的儀器(數量不限)簡易表示如下:
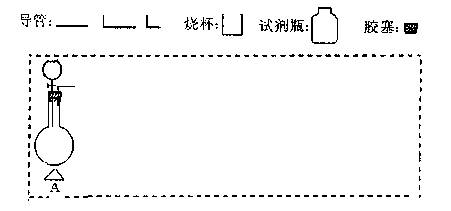
(3)根據方框中的裝置圖,完成下表(若無需填寫,則在表格中寫“無”)
|
儀器符號 |
儀器中所加物質 |
作用 |
|
A |
MnO2、濃鹽酸 |
MnO2與濃鹽酸生成Cl2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(4)KMnO2與濃鹽酸在常溫下反應也可以得到Cl2,請寫出該反應的離子方程式 。
(5)請寫出Cl2在工業(yè)、農業(yè)、醫(yī)療、衛(wèi)生等方面的用途 。(寫出兩種即可)
(6)將Cl2與SO4分別通人品紅溶液,都能使品紅褪色。簡述用褪色的溶液區(qū)別二者的實驗方法。
科目:高中化學 來源:山東省聊城市“四縣六校”2012-2013學年高一下學期期末聯考化學試題 題型:043
下表為元素周期表的一部分,請參照元素①-⑨在表中的位置,回答下列問題:
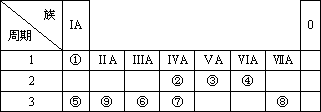
(1)由①、②兩種元素組成的相對分子質量為28的有機物的空間構型是________,
該物質與溴水發(fā)生加成反應的化學方程式是________.
(2)用電子式表示④的簡單氫化物的形成過程如下:________;
(3)請設計實驗比較元素⑥與⑨金屬性的相對強弱:________;
(4)用①元素的單質與④元素的單質可以制成電池,電池中裝有KOH濃溶液,將多孔的惰性電極甲和乙浸入KOH溶液中,在甲極通入①的單質,乙極通入④的單質,則甲極的電極反應式為:________.
(5)由表中①、③、④、⑥、⑧元素形成的常見物質X、Y、Z、M、N可發(fā)生以下反應:

X溶液與Y溶液反應的離子方程式為________,工業(yè)上常用單質⑥冶煉難熔的金屬,寫出氧化鐵和單質⑥在高溫下反應的化學方程式________.
查看答案和解析>>
科目:高中化學 來源: 題型:
下表為元素周期表的一部分,請參照元素①-⑨在表中的位置,
回答下列問題:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑨ | ⑥ | ⑦ | ⑧ | |||
(1)由①、②兩種元素組成的相對分子質量為28的有機物的空間構型是 ,
該物質與溴水發(fā)生加成反應的化學方程式是 。
(2)用電子式表示④的簡單氫化物的形成過程如下: ;
(3) 請設計實驗比較元素⑥與⑨金屬性的相對強弱: _;
(4) 用①元素的單質與④元素的單質可以制成電池,電池中裝有KOH濃溶液,將多孔的惰性電極甲和乙浸入KOH溶液中,在甲極通入①的單質,乙極通入④的單質,則甲極的電極反應式為: 。
(5)由表中①、③、④、⑥、⑧元素形成的常見物質X、Y、Z、M、N可發(fā)生以下反應:

X溶液與Y溶液反應的離子方程式為 ,工業(yè)上常用單質⑥冶煉難熔的金屬,寫出氧化鐵和單質⑥在高溫下反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源:2015屆山東省聊城市四縣六校高一下學期期末聯考化學試卷(解析版) 題型:填空題
下表為元素周期表的一部分,請參照元素①-⑨在表中的位置,
回答下列問題:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
⑨ |
⑥ |
⑦ |
|
|
⑧ |
|
(1)由①、②兩種元素組成的相對分子質量為28的有機物的空間構型是 ,
該物質與溴水發(fā)生加成反應的化學方程式是 。
(2)用電子式表示④的簡單氫化物的形成過程如下: ;
(3) 請設計實驗比較元素⑥與⑨金屬性的相對強弱: _;
(4) 用①元素的單質與④元素的單質可以制成電池,電池中裝有KOH濃溶液,將多孔的惰性電極甲和乙浸入KOH溶液中,在甲極通入①的單質,乙極通入④的單質,則甲極的電極反應式為: 。
(5)由表中①、③、④、⑥、⑧元素形成的常見物質X、Y、Z、M、N可發(fā)生以下反應:

X溶液與Y溶液反應的離子方程式為 ,工業(yè)上常用單質⑥冶煉難熔的金屬,寫出氧化鐵和單質⑥在高溫下反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源:2015屆江西省撫州市高一下學期期末考試化學試卷(解析版) 題型:填空題
下表為元素周期表的一部分,請參照元素①-⑨在表中的位置,
回答下列問題:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
⑨ |
⑥ |
⑦ |
|
|
⑧ |
|
(1)由①、②兩種元素組成的相對分子質量為28的有機物的空間構型是 ,
該物質與溴水發(fā)生加成反應的化學方程式是 。
(2)用電子式表示④的簡單氫化物的形成過程如下: ;
(3) 請設計實驗比較元素⑥與⑨金屬性的相對強弱: _;
(4) 用①元素的單質與④元素的單質可以制成電池,電池中裝有KOH濃溶液,將多孔的惰性電極甲和乙浸入KOH溶液中,在甲極通入①的單質,乙極通入④的單質,則甲極的電極反應式為: 。
(5)由表中①、③、④、⑥、⑧元素形成的常見物質X、Y、Z、M、N可發(fā)生以下反應:

X溶液與Y溶液反應的離子方程式為 ,工業(yè)上常用單質⑥冶煉難熔的金屬,寫出氧化鐵和單質⑥在高溫下反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:
(08南昌市三模)(15分)某校化學課外小組為了鑒別碳酸鈉和碳酸氫鈉兩種白色固體,用不同的方法做了以下實驗。
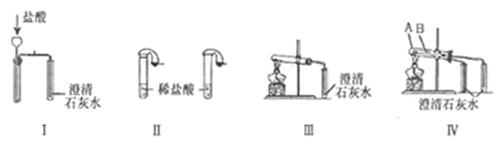
(1)只根據圖I、II所示實驗,能夠達到實驗目的的是(填裝置序號) ;
(2)圖III、IV所示實驗均能鑒別這兩物質,其反應的化學方程式為 ;與實驗III相比,實驗IV的優(yōu)點是(填選項序號) 。
A.IV比III復雜 B.IV比III安全 C.IV比III操作簡便
D.IV可以做到一套裝置同時進行兩個對比實驗,而III不能
(3)若用實驗裝置IV驗證碳酸鈉和碳酸氫鈉的穩(wěn)定性,則試管B中裝入的固體最好是
;
(4)將碳酸氫鈉溶液與澄清石灰水混合并充分反應:
①當石灰水過量時,其離子方程式是 ;
②當碳酸氫鈉與氫氧化鈣物質的量之比為2:1時,所得溶液中溶質的化學式為
,請設計實驗檢驗所得溶液中溶質的陰離子
。
(5)若碳酸鈉樣品中含有少量氯化鈉;為測定樣品中碳酸鈉的質量分數;該小組同學稱取樣品mg,按下圖裝置進行實驗,根據實驗原理
①請在圖中方框內補充必要的儀器,并注明所用試劑名稱。
②實驗結束時量筒中試劑體積Vml(標況)則ω(Na2CO3)= (用含m、V的數學表達式表示)
|
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com