
| A. | R的最高價氧化物對應的水化物的酸性比X的弱 | |
| B. | 非金屬性:Y>X | |
| C. | 原子半徑的大小順序:X>Z | |
| D. | Z元素最高價氧化物對應的水化物具有兩性 |
分析 X、Y、Z、R是短周期主族元素,X原子最外層電子數是次外層的兩倍,最外層電子數不超過8個,則其K層為次外層,最外層電子數為4,則X是C元素;Y元素在地殼中的含量最多,則Y是O元素;Z元素的化合物的焰色反應呈黃色,則Z是Na元素;R原子的核外電子數是X原子與Z原子的核外電子數之和,則R的核外電子數是17,所以R是Cl元素,據此解答.
解答 解:X、Y、Z、R是短周期主族元素,X原子最外層電子數是次外層的兩倍,最外層電子數不超過8個,則其K層為次外層,最外層 電子數為4,則X是C元素;Y元素在地殼中的含量最多,則Y是O元素;Z元素的化合物的焰色反應呈黃色,則Z是Na元素;R原子的核外電子數是X原子與Z原子的核外電子數之和,則R的核外電子數是17,所以R是Cl元素.
A.非金屬性R(Cl)>X(C),故酸性:高氯酸>碳酸,故A錯誤;
B.同一周期元素,元素非金屬性隨著原子序數增大而減弱,所以非金屬性O>C,故B正確;
C.同周期自左而右原子半徑減小、同主族自上而下原子半徑增大,故原子半徑Z(Na)>X(C),故C錯誤;
D.Z為Na元素,其最高價氧化物的水化物是NaOH,屬于強堿,故D錯誤,
故選:B.
點評 本題考查原子結構與元素周期律,推斷元素是解題的關鍵,注意對元素周期律的理解掌握,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 當一個可逆反應達到平衡狀態時,這就是這個反應所能達到的限度 | |
| B. | 當一個可逆反應達到平衡狀態時,各組分濃度不變,v(正)=v(逆)=0 | |
| C. | 任何可逆反應的進程都有一定的限度,只是不同的反應限度不同 | |
| D. | 化學反應的限度可以通過改變條件而改變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 植物油不能使溴的四氯化碳溶液褪色( ) | |
| B. | 甲烷和氯氣反應生成一氯甲烷與苯和硝酸反應生成硝基苯的反應類型不同 | |
| C. | 乙醇、乙酸和乙酸乙酯能用飽和Na2CO3溶液鑒別 | |
| D. | 苯不能使KMnO4溶液褪色,因此苯不能發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 日常生活中無水乙醇常用于殺菌消毒 | |
| B. | 棉、麻、絲、毛及合成纖維完全燃燒都只生成CO2和H2O | |
| C. | 加熱能殺死流感病毒式因為病毒的蛋白質受熱變性 | |
| D. | 人造纖維、合成纖維和光導纖維都是有機高分子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
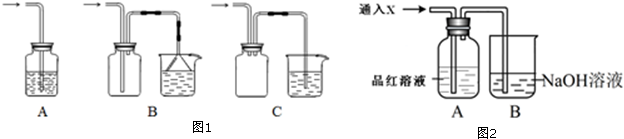
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,0.1 mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | 常溫下,0.1 mol•L-1HA溶液與0.1 mol•L-1 NaOH溶液正好完全反應時,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) | |
| C. | 常溫下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)=0.1 mol•L-1:c(Na+)=c(CH3COOH)>c(CH3COO-)>c(H+)=c(OH-) | |
| D. | 常溫下,向0.1 mol•L-1CH3COOH 溶液加水稀釋,當溶液的pH從3.0升到4.0時,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原來的10倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
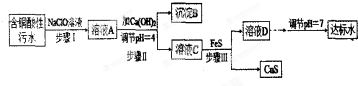
| l離子 | H+ | Cu2+ | Fe3+ | Fe2+ |
| 濃度/(mol•L-1) | 0.1 | 0.05 | 0.04 | 0.002 |
| 物質 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | FeS | CuS |
| Ksp | 4.0×10-22 | 8.0×10-16 | 2.2×10-20 | 6.4×10-12 | 6.0×10-26 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學反應速率越快,反應現象越明顯 | |
| B. | 需要加熱才能進行的化學反應不一定是吸熱反應 | |
| C. | 僅由非金屬元素組成的化合物中可能含離子鍵 | |
| D. | ⅠA族金屬元素是同周期中金屬性最強的元素 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com