
【題目】在80℃時,將0.4mol的四氧化二氮氣體充入2L已抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:
時間(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0. 20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺。
(1)該反應的化學方程式為__________________________,表中b_________c(填“<”、“=”、“>”)。
(2)20s時,N2O4的的濃度為__________________mol·L-1,0~20s內N2O4的平均反應速率為________________;
(3)該反應的平衡常數表達式K=___________________
在80℃時該反應的平衡常數K值為:______________(保留到小數點后2位)。
(4)在其他條件相同時,該反應的K值越大,表明建立平衡時____________。
A.N2O4的轉化率越高 B.NO2的產量越大
C.N2O4與NO2的濃度之比越大 D.正反應進行的程度越大
【答案】(每空2分,共12分)(1)N2O4![]() 2NO2,吸熱
2NO2,吸熱
(2)0.14, 0.003 mol/(L·s) (3)0.54 (4)ABD
【解析】試題分析:(1)N2O4分解生成NO2,反應的化學方程式是N2O4![]() 2NO2。根據表中數據可知,反應進行到60s時,物質到濃度不再發生變化,說明反應達到平衡狀態。當反應進行到反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺,這說明降低溫度反應寫逆反應方向移動,因此正反應是吸熱反應。
2NO2。根據表中數據可知,反應進行到60s時,物質到濃度不再發生變化,說明反應達到平衡狀態。當反應進行到反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺,這說明降低溫度反應寫逆反應方向移動,因此正反應是吸熱反應。
(2)20s時,四氧化二氮的濃度為a
N2O4 ![]() 2NO2
2NO2
1mol/L 2mol/L
(0.20-a)mol/L 0.12mol/L
解得a=0.14mol/L
則反應的N2O4濃度為(0.2-0.14)mol/L=0.06mol/L
則反應速率v(N2O4)=0.06mol/L÷20s=0.003 mol/(L·s)
(3)平衡時NO2當濃度是0.22mol/L,則N2O4的濃度是0.2mol/L-0.11mol/L=0.09mol/L
所以根據反應的方程式可知,平衡常數K=![]()
(4)根據化學平衡常數知,K越大,生成物的濃度越大,反應物的濃度越小,N2O4的轉化率大、NO2的產量越大、N2O4與NO2的濃度之比越小、正反應進行的程度越大,即選項ABD正確,答案選ABD。


科目:高中化學 來源: 題型:
【題目】羰基硫(COS)可作為一種糧食熏蒸劑,能防止某些昆蟲、線蟲和真菌的危害。在恒容密閉容器中,將CO和H2S混合加熱并達到下列平衡: CO(g)+H2S(g)![]() COS(g)+H2(g) ,K=0.1,反應前CO的物質的量為10mol,平衡后CO物質的量為8mol,下列說法正確的是
COS(g)+H2(g) ,K=0.1,反應前CO的物質的量為10mol,平衡后CO物質的量為8mol,下列說法正確的是
A. 升高溫度,H2S濃度增加,表明該反應的△H>0
B. 隨著反應的進行,混合氣體的密度逐漸減小
C. 反應前H2S物質的量為7mol
D. CO的平衡轉化率為80%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是 ( )
A.電解質溶液在通電時才可以電離
B.金屬氧化物一定都是堿性氧化物
C.非金屬氧化物都是酸性氧化物
D.堿性氧化物一定都是金屬氧化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“2015·8·12”天津港爆炸中有一定量的氰化物泄露。氰化物多數易溶于水,有劇毒,易造成水污染。已知部分弱酸的電離平衡常數如下表:
弱酸 | HCOOH | HCN | H2CO3 |
電離平衡常數(25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
(1)根據價鍵規則,寫出H2CO3的結構式__________。
(2)下列能用于判斷氮、碳兩種元素非金屬性強弱的是_________(填序號)
a. 氣態氫化物的穩定性強弱 b. 最高價氧化物對應水化物酸性強弱
c. Al2O3+N2+3C=2AlN+3CO d. 比較在周期表中的位置
(3)0.01mol/L的NaCN溶液pH=9,用離子方程式表示呈堿性的原因_______。 請判斷該溶液中:c(CN-)__c(OH-)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大,處理該污水時,可在催化劑TiO2作用下用NaClO將CN-氧化成CNO-。CNO-在酸性條件下繼續被NaClO氧化生成N2與CO2。某環保部門用下圖裝置進行實驗,以證明該處理方法的有效性并測定CN-被處理的百分率。

將濃縮后含CN-的廢水與過量NaClO溶液的混合液(其中CN-濃度為0.05mol/L)200mL倒入甲中,塞上橡皮塞,一段時間后,打開活塞,使溶液全部放入乙中,關閉活塞。
①甲中反應的離子方程式為___________,乙中反應的離子方程式為________。
②上述實驗是通過測定CO2的量來確定CN-的處理效果。若丙中的試劑是飽和食鹽水,且丙、丁都是除雜裝置,則乙中產生的氣體除CO2、N2外,還可能含有的雜質氣體是__________,戊中盛有足量的石灰水,若實驗后戊中生成0.9g沉淀,則CN-被處理的百分率為_________。
(5)裝置中堿石灰的作用是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對充有氖氣的霓虹燈管通電,燈管發出紅色光。產生這一現象的主要原因
A. 電子由激發態向基態躍遷時以光的形式釋放能量
B. 電子由基態向激發態躍遷時吸收除紅光以外的光線
C. 氖原子獲得電子后轉變成發出紅光的物質
D. 在電流的作用下,氖原子與構成燈管的物質發生反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與社會、生活密切相關。對下列現象或事實的解釋不正確的是
選項 | 現象或事實 | 解釋或對應的離子方程式 |
A | 用熱的純堿溶液洗去油污 | CO32-+H2O 溶液呈堿性,溫度升高堿性增強 |
B | 酸雨樣品在空氣中放置pH減小 | 亞硫酸被氧化為硫酸 2H2SO3+O2=2H2SO4 |
C | “84”消毒液具有漂白性 | ClO-+CO2+H2O=HClO+HCO3- |
D | 用加熱法除去NaCl固體中混有的NH4Cl固體 | NH4Cl固體可以完全分解成為氣體而除去 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對四組無色透明溶液進行離子檢驗,四位同學各鑒定一組,他們的實驗報告的結論如下,其中可能正確的是
A. MnO4—、K+、S2—、Na+ B. Mg2+、NO3—、OH—、Cl—
C. K+、H+、Cl—、CO32— D. Na+、OH—、Cl—、NO3—
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.一定溫度下,在2 L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示:
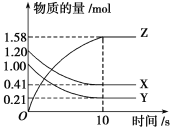
(1)從反應開始到10 s時,用Z表示的反應速率為_____________________________。
(2)該反應的化學方程式為__________________________________________________。
Ⅱ.在恒溫恒容的密閉容器中,當下列物理量不再發生變化時:①混合氣體的壓強,②混合氣體的密度,③混合氣體的總物質的量,④混合氣體的平均相對分子質量,⑤混合氣體的顏色,⑥各反應物或生成物的反應速率之比等于化學計量數之比
(1)一定能證明2SO2(g)+O2(g)![]() 2SO3(g)達到平衡狀態的是_______(填序號,下同)。
2SO3(g)達到平衡狀態的是_______(填序號,下同)。
(2)一定能證明I2(g)+H2(g)![]() 2HI(g)達到平衡狀態的是 ____________。
2HI(g)達到平衡狀態的是 ____________。
(3)一定能證明A(s)+2B(g)![]() C(g)+D(g)達到平衡狀態的是_________。
C(g)+D(g)達到平衡狀態的是_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com