
為測定某有機化合物A的結構,進行如下實驗:
I.分子式的確定:
(1)將一定量有機物A置于氧氣流中充分燃燒,實驗測得:生成3.6g H2O和8.8g CO2,消耗氧氣5.6L(標準狀況下),則該物質中各元素的原子個數比是_______________。
(2)用質譜儀測定該有機化合物的相對分子質量,得到如圖①所示質譜圖,由此確定該物質的分子式是______________。
(3)根據價鍵理論,預測A的可能結構有________種。
II.結構式的確定:
(4)核磁共振氫譜能對有機物分子中不同化學環境的氫原子給出不同的峰值(信號),根據峰值(信號)可以確定分子中氫原子的種類和數目。例如:甲基氯甲基醚(ClCH2OCH3)有兩種氫原子如圖②。經測定,有機物A的核磁共振氫譜示意圖如圖③,則A的結構簡式為_________________。

科目:高中化學 來源:2015-2016學年湖南省洞口縣高二下學期期末化學試卷(解析版) 題型:選擇題
四種短周期主族元素W、X、Y、Z的原子序數依次增大,W、X的簡單離子具有相同電子層結構,X的原子半徑是短周期主族元素原子中最大的,W與Y同族,Z與X形成的離子化合物的水溶液呈中性。下列說法正確的是
A. W與X形成的化合物溶于水后溶液呈堿性
B. 簡單離子半徑:W<X<Z
C. 氣態氫化物的熱穩定性:W<Y
D. 最高價氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化學 來源:2015-2016學年福建省晉江市高一下學期期末化學試卷(解析版) 題型:選擇題
重水(D2O)是重要的核工業原料,下列說法錯誤的是
A. 氘(D)原子核外有1個電子
B. 1H與D互稱同位素
C. H2O與D2O互稱同素異形體
D. 1H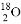 與D
與D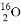 的相對分子質量相同
的相對分子質量相同
查看答案和解析>>
科目:高中化學 來源:2015-2016學年福建省晉江市高二下學期期末化學試卷(解析版) 題型:選擇題
下列對相關有機物的描述不正確的是
A.用灼燒的方法可以區分蠶絲和人造纖維
B.蛋白質遇重金屬離子會變性
C.α-氨基丙酸與α-氨基苯丙酸混合物脫水成肽,只生成2種二肽
D食用油反復加熱會產生稠環芳香烴等有害物質
查看答案和解析>>
科目:高中化學 來源:2015-2016學年福建省晉江市高二下學期期末化學試卷(解析版) 題型:選擇題
1 mol某烴在氧氣中充分燃燒,需要消耗氧氣179.2 L(標準狀況),它在光照條件下與氯氣反應能生成3種不同的一氯代物。則該烴的結構簡式是
A.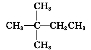
B.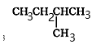
C.CH3CH2CH2CH2CH3
D.
查看答案和解析>>
科目:高中化學 來源:2015-2016學年安徽省高二下學期期末化學試卷(解析版) 題型:選擇題
下圖表示在催化劑作用下將X和Y合成具有生物活性的物質Z,W是中間產物(R1、R2均為烴基)。
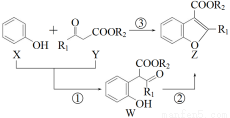
則下列有關敘述一定正確的是 ( )
A.反應①屬于加成反應
B.1molZ完全加成需要3molH2
C.X與W屬于同系物
D.X、Y、Z、W都能與NaOH溶液反應
查看答案和解析>>
科目:高中化學 來源:2015-2016學年安徽省高二下學期期末化學試卷(解析版) 題型:選擇題
下表所示為部分短周期元素的原子半徑及主要化合價,根據表中信息判斷下列敘述不正確的 ( )
元素代號 | A | B | C | D | E | N | G |
原子半徑/nm | 0.182 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
主要化合價 | +1 | +2 | +2 | +3 | +6、-2 | -1 | -1 |
A.穩定性:HG>HN;熔沸點:HG>HN
B.工業上常用電解熔融DN3的方法冶煉D單質
C.B、C原子的價電子數相同
D.0.1mol/L的最高價氧化物的水化物溶液的pH:A≠N
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧省高一6月月考化學試卷(解析版) 題型:選擇題
下列熱化學方程式數學正確的是(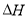 的絕對值均正確)
的絕對值均正確)
A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—1367.0 kJ/mol(燃燒熱)
B. NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和熱)
C.S(s)+O2(g)===SO2(g);△H= —269.8kJ/mol(反應熱)
D. 2NO2==O2+2NO;△H=+116.2kJ/mol(反應熱)
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一下期末化學試卷(解析版) 題型:實驗題
鹵塊的主要成分是MgCl2,此外還含Fe3+、Fe2+和Mn2+等離子。若以它為原料按下圖所示工藝流程進行生產,可制得輕質氧化鎂(已知其中有一種中間產物是MgCO3)。
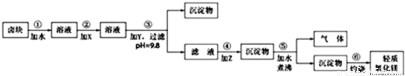
若要求產品盡量不含雜質,而且生產成本較低,根據表1和表2提供的資料,填寫空白:
表1生成氫氧化物沉淀的pH
物質 | 開始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
表2原料價格表
物質 | 價格/元?噸-1 |
漂液(含25.2%NaClO) | 450 |
雙氧水(含30%H2O2) | 2400 |
已知:Fe2+氫氧化物呈絮狀,不易從溶液中除去,常將它氧化為Fe3+,生成Fe(OH)3沉淀除去。
(1)在步驟②中加入的試劑X,最佳的選擇是______,其反應的離子方程式是 。
(2)在步驟③中如要控制pH=9.8,其目的是______;在步驟④中加入的試劑Y應是______;
(3)在步驟⑤中發生的化學方程式是______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com